Етіологія ішемічного інсульту
Серед захворювань, що призводять до розвитку інфаркту мозку , перше місце належить атеросклерозу. Нерідко атеросклероз поєднується з цукровим діабетом.
Рідше основним захворюванням, ускладненої інфарктом, є гіпертонічна хвороба, ще рідше — ревматизм. При ревматизмі основною причиною ішемічеcкого інсульту є кардіогенна емболія мозкових судин, значно рідше тромбоваекуліти. Серед інших захворювань, які можуть ускладнюватися ішемічним інсультом, слід згадати артеріїти інфекційної та інфекційно-алергічної природи, захворювання крові (еритремія, лейкози). Аневризми церебральних артерій після їх розриву можуть ускладнитися спазмом і викликати розвиток інфаркту мозку.
Патогенез ішемічного інсульту
Інфаркт мозку формується в основному внаслідок причин, що викликають локальний дефіцит артеріального кровотоку. З факторів, безпосередньо викликають зниження мозкового кровотоку і розвиток інфаркту мозку, слід зазначити стеноз і оклюзію екстракраніальних і інтракраніальних судин мозку. Стеноз і оклюзія при ангіографії виявляються в мозкових судинах рідше, ніж в екстракраніальних, проте клініко-анатомічні повідомлення з цього питання не є однозначними. Деякі автори констатують більш часте ураження окклюзірующего процесом сонних артерій [Шмідт Є. В., 1963, Колтовер А. І., 1975], інші — внутрішньочерепних судин [Левін Г. 3., 1963].
Можна вважати доведеним, що не існує безпосередній кореляції між частотою веріфіцированного стенозу і оклюзії екстра-та інтракраніальних артерій і частотою розвитку ішемічного інсульту. Про це свідчать ангиографические і клініко-морфологічні дані про відносно частому виявленні безсимптомних стенозов і оклюзії.
Таким чином, очевидно, що атеросклеротичні зміни в екстра-та інтракраніальних судинах не обов'язково тягнуть за собою розвиток інфаркту мозку, і навіть при виникненні останнього далеко не завжди встановлюється безпосередня причинно-наслідковий і тимчасова зв'язок (з розвитком атеросклерозу).
Істотна роль в компенсації дефіциту кровообігу при стенозі і оклюзії екстра-та інтракраніальних артерій належить колатерального кровообігу, ступінь розвитку якого індивідуальна.
[ Рис.1 ] [ Рис.2 ] [ Рис.3 ] [ Рис.4 ] [ Рис.5 ]
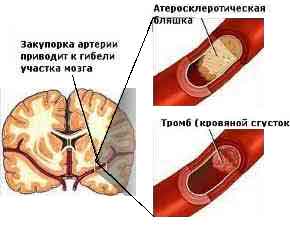
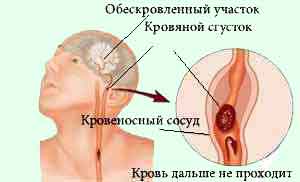
[Рис. 2] Закупорка судини тромбом і атеросклеротичної бляшкою.
Оклюзія судини може бути викликана тромбом, емболом або обумовлена облітерацією його . При наявності повної закупорки судини (екстракраніального, інтракраніальних або интрацеребрально) інфаркт мозку може не розвинутися, якщо добре розвинене колатеральний кровообіг і що особливо важливо, якщо колатеральна мережу швидко включилася з моменту оклюзії судини. Іншими словами розвиток інфаркту мозку при наявності повної оклюзії судини залежить від ступеня розвитку і темпу включення колатеральногокровообігу.
При розвитку стенозу екстракраніальних або інтрацеребральних судин створюються також умови для локальної ішемії речовини мозку , якщо раптово падає АТ . Падіння тиску може бути викликане інфарктом міокарда, кровотечею і т. Д. Крім цього при стенозі судин створюються умови для турбулентного руху крові, що сприяє склеюванню формених елементів крові — еритроцитів і тромбоцитів і утворенню клітинних агрегатів — мікроемболіі, що можуть закрити просвіт дрібних судин і бути причиною припинення кровотоку до відповідної ділянки мозку. Крім того, високий артеріальний тиск (200 / / 100 мм рт. Ст. І вище) розцінюється як несприятливий фактор, що сприяє постійної микротравматизации інтими артерій і відриву емболіческіх фрагментів ізстенозіроваяних ділянок.
Крім тромбозу, емболії, гемодинамічних чинників, а також артеріо-артеріальних емболій, в розвитку інфаркту мозку певну роль відіграють реакція судинної системи мозку і формених елементів крові на дефіцит мозкового кровообігу, а також енергетичні запити тканини мозку .
Реакція судинної системи мозку на зменшення локального мозкового кровотоку різна. Так, в одних випадках ішемія змінюється надмірною кровотоком, що призводить до фільтраційного перифокальний набряку, в інших — зону ішемії оточують розширені судини, але не заповнені кров'ю (феномен «непоновлення» кровотоку). Механізм настільки різної реакції мозкових судин у відповідь на ішемію до кінця не ясний. Можливо це залежить від різного ступеня гіпоксії і змінюються в зв'язку з цим гідродинамічних властивостей крові. Якщо в разі максимального розширення судин з розвиваються регіонарним набряком, що виникають після ішемії, можна думати про зрив нормальних ауторегуляціонних механізмів самих мозкових судин в зоні локальної ішемії, то феномен «непоновлення» кровотоку можна пояснити реакцією тільки одних судин мозку. У механізмі появи порожніх капілярів і артеріол в зоні локального дефіциту кровообігу, мабуть, певну роль відіграють зміни функціональних властивостей клітинних елементів крові, які втрачають здатність в зоні ішемії нормально просуватися по микроциркуляторному руслу.
Відомо, що капілярний кровообіг залежить від агрегаційну властивостей еритроцитів і тромбоцитів, від здатності еритроцитів змінювати свою форму при просуванні через вузькі капіляри, а також від в'язкості крові. Еритроцити крові, мають діаметр, що перевищує діаметр вузьких капілярів, в умовах нормального кровообігу легко змінюють свою форму (деформуються) і подібно амебі просуваються по капілярному руслу. У хворих з судинними захворюваннями здатність змінювати форму у еритроцитів зменшується, вони стають більш жорсткими. Ще більше зниження деформованості червоних кров'яних тілець розвивається в гіпоксичних осередках будь-якої локалізації, де змінюється осмотичний тиск. Значне зниження еластичності еритроцита не дозволить йому пройти через капіляр, діаметр якого менше еритроцита. Отже, збільшення жорсткості еритроцитів, а також збільшення агрегації тромбоцитів і еритроцитів в зоні локальної ішемії мозку можуть бути одним з головних чинників, що перешкоджають притоку крові по розширеним судинах при феномені «непоновлення» кровотоку . Таким чином, якщо причина, яка викликала локальну ішемію мозку, зникає, то країни, що розвиваються після ішемії регіонарний набряк або патологічний феномен «непоновлення» кровотоку можуть привести до порушення нормальної життєдіяльності нейронів і розвитку інфаркту мозку.
Зі сказаного ясно, що як в розвитку оклюзії судин, що живлять мозок (тромбом, емболом, мікроембола) ,. так і при ішемії, що виникла внаслідок гемодинамічних порушень (падіння артеріального тиску, обумовлене різними причинами), важлива роль належить не тільки змін судин, але і фізико-хімічними властивостями крові, від зміни яких залежить результат порушення мозкового кровообігу, т. е. розвиток інфаркту мозку .
У патогенезі церебральних ишемий домінуючу роль серед факторів, що викликають оклюзію, грають тромбози і емболії мозкових судин , розмежування яких представляє значні труднощі не тільки в клініці, але і на аутопсії. Тромб нерідко є субстратом, емболізірующім артерії мозку, що знайшло відображення в широкому використанні терміна «тромбоемболія».
Формуванню тромбу в ураженому посудині сприяють (за існуючими в даний час уявленням) додаткові, або «реалізують тромбоз», чинники. Основними з них слід вважати зміни функціональних властивостей тромбоцитів і (активності біологічно активних моноаминов, порушення рівноваги згортають і противосвертиваючих факторів крові, а також зміни гемодинамічних показників.
Зміни функціонального стану тромбоцитів (підвищення їх агрегаційної і адгезивної здатності, пригнічення дезагрегации) чітко спостерігаються вже в початковій стадії атеросклерозу. Достовірно підвищується агрегація в міру прогресування атеросклерозу з появою минущих порушень мозкового кровообігу і при стенотичних процесах в магістральних артеріях голови. Локальна схильність до агрегації, склеювання, а потім розпаду (віскозному метаморфозу) тромбоцитів на ділянці, де пошкоджена інтиму, пояснюється тим, що саме в цьому місці розвивається ланцюгова реакція, що залежить від ряду гуморальних і гемодинамічних факторів.
Порушення цілісності інтими і оголення колагенових волокон знижують негативний електричний заряд судинної стінки і відповідно зменшують адсорбцію плазмового фібриногену на цій ділянці. Накопичення фібриногену в свою чергу знижує електричний потенціал тромбоцитів і створює умови для їх прилипання до пошкодженої інтимі і швидкого руйнування. При цьому вивільняється ряд прокоагулянтних факторів пластинок, що сприяють прискоренню перетворення протромбіну в тромбін, фібриногену в фібрин і ретракції фібрину. Одночасно має місце пригнічення місцевої фібринолітичної активності плазми, локальна поява тромбіну. Для масивного тромбоутворення, різко обмежує просвіт судини і опиняється причиною ішемічного інсульту, недостатньо тільки тромбогенної активності розпалися тромбоцитарних агрегатів. Вирішальне значення має порушення нормального співвідношення плазмових тромбогенних і антітромбогенних факторів, що утворюються в ураженій ділянці судини.
Безпосередньо в першу добу розвитку ішемічного інсульту виникає підвищення згортання крові в мозковому кровотоці , яке свідчить про утруднення мікроциркуляції і освіті оборотних микротромбов в артеріолах і прекапиллярах мозку. В подальшому наступає захисна протизгортальна реакція, яка, однак, виявляється недостатньою для подолання швидко розвивається генералізованої гіперкоагуляції по всьому судинного русла.
В одночасно протікають процеси тромбоутворення і тромболізису бере участь складний багатоступінчастий комплекс коагулянтной і антикоагулянтних факторів, і в залежності від підсумкового превалювання одного з них в ураженому відрізку судини спостерігаються різні ступені і наслідки тромбоутворення. Іноді процес обмежується стенозом, частковим відкладенням тромбоцитів і фібрину, а іноді-утворюються щільні конгломерати, повністю обтурирующие просвіт судини і поступово збільшуються за довжиною його.
Збільшенню «зростання тромбу» крім гіперкоагулянтності крові сприяють уповільнення кровотоку і турбулентні, вихрові, руху (кров'яних пластинок. Відносна гипокоагуляция робить більш пухкою структуру тромбів, що може з'явитися причиною для утворення клітинних емболій і, мабуть, виявляється чинником, що грає істотну роль в спонтанної реканалізації тромбів. Тромботічеекіе поразки зкстракраніальних і великих інтракраніальних артерій є одним з джерел артеріо-артеріальних емболій судин мозку.
Джерелом емболії мозкових судин може послужити також ураження різних органів і систем. Найбільш часті кардіогенний емболії, що розвиваються внаслідок відриву пристінкових тромбів і бородавчатих нашарувань при клапанних вадах серця, при зворотному ендокардиті, при вроджених вадах серця і під час операцій з приводу вроджених або придбаних пороках серця. Кардіогенний емболії мозкових судин можуть розвиватися при інфарктах міокарду, при гострих постінфарктних аневризмах серця з утворенням пристінкових тромбів і тромбоемболії.
Джерелом емболій можуть з'явитися пристінкові тромби, що утворилися у розпадається атерооклеротіческой бляшки при атеросклерозі аорти та магістральних судин голови. Причиною кардіогенний емболії є різні ураження, що викликають миготливу аритмію і зниження скорочувальної здатності серця (ревматизм, атероаклеротіческій або постінфарктний кардіосклероз, постінфарктний аневризми), а також свіжі інфаркти міокарда, що супроводжуються тромбоендокардіта.
Частота виявлення емболів в артеріальній системі мозку коливається за даними різних авторів від 15 до 74% [Шеффер Д. Г. та ін., 1975, Ziilch, 1973]. Наведені дані зайвий раз свідчать на користь великих труднощів диференціальної діагностики тромбозів і емболій не тільки прижиттєво, а й на аутопсії.
Певне значення в патогенезі ішемічних інсультів мають психоемоційні стрес-фактори , що призводять і зростаючої секреції катехоламінів, в нормальних умовах є своєрідними каталізаторами симпатико-адреналової системи, що підтримує гомеостатическое рівновагу. Стосовно до розглянутої проблеми слід зауважити, що катехоламіни є потужними активаторами агрегації тромбоцитів. Якщо у здорових осіб катехоламіни лише стимулюють агрегацію тромбоцитів, то у хворих на атеросклероз (при швидкому викиді їх в судинне русло) вони викликають різко підвищену агрегацію і руйнування тромбоцитів, що призводить до значного виходу серотоніну, головним переносником якого є тромбоцити [Haft, 1972], і внутрисосудистому тромбоутворення. Гиперпродукцию катехоламінів багато дослідників розглядають як сполучна ланка між психогенними факторами — хронічним або гострим емоційним напруженням і атеросклеротичними змінами судинної стінки [Haft, 1972, Fani, 1973].
В компенсації дефіциту мозкового кровообігу грає роль не тільки індивідуально розвинена мережа колатеральногокровообігу, а й вікові особливості енергетичних запитів тканини мозку. У міру старіння організму і появи біохімічних і клінічних ознак атеросклерозу зменшується маса мозку і інтенсивність мозкового кровообігу. До 60 років інтенсивність мозкового кровотоку, споживання мозком кисню і глюкози зменшується на 20-60% в порівнянні з показниками у здорових молодих людей і при цьому може не виникати помітних порушень функції [Quandt, 1971]. Відносна компенсація церебральної гемодинаміки без появи неврологічної симптоматики може спостерігатися у хворих на атеросклероз при досить значному дефіциті (Кровообігу, в умовах хронічної ішемії, яка характеризується зменшенням загального кровотоку до 36,4 мл (с / 100 г мозку) при нормі 58 мл (с / 100 г ) і споживання кисню до 2,7 мл (замість 3,7 мл). в окремих спостереженнях неврологічні симптоми виявляються оборотними навіть в умовах зниження рівня метаболізму нервових клітин на 75-80% [Quandt, 1974].
Жвава дискусія ведеться при обговоренні ролі спазму церебральних судин в генезі ішемічеокого інсульту і ПНМК. Можливість ангиоспазма мозкових артерій і артеріол в даний час не викликає сумнівів. У нормальних умовах ангіоспазм є звичайною компенсаторну реакцію у відповідь на зниження мозкового кровотоку, на підвищений вміст кисню і знижену концентрацію вуглекислоти в крові. Відповідно до сучасних уявлень, центральний ангіоспазм викликається багатьма гуморальними механізмами. З гуморальних факторів спазмогенну властивості мають катехоламіни, адренокортикотропний гормон, продукти розпаду тромбоцитів. Спазмогенну дією володіють простогландини, переважно фракція Е, що вивільняється головним чином із зруйнованих тромбоцитів.
Ангіоспазм мозкових судин — важлива ланка системи ауторегуляції мозкового кровообігу. Більшість дослідників висловлюють сумніви тому, що до останнього часу ніхто не почув прямих доказів ролі нейрогенного спазму в розвитку інфаркту мозку. Винятком може слугувати спазм, що ускладнює перебіг субарахноїдального крововиливу, який розвивається у відповідь на розрив судинної стінки і призводить до розвитку інфаркту мозку. Однак розвиток спазму артерій при субарахноїдальний крововилив пов'язують з безпосереднім впливом вилилась крові на симпатичні сплетення артерій.
Патологічна анатомія ішемічного інсульту
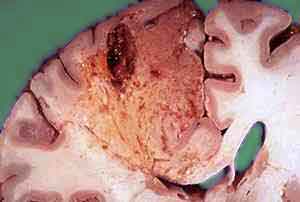
При ішемічному інсульті утворюються інфаркти, т. Е. Осередки некрозу мозку, обумовлені недостатнім притоком крові. У ранні терміни ішемічного інсульту морфологічно виявляється область побледнения і набухання речовини мозку, нечітка структура перифокальною зони.
Межі інфаркту недостатньо рельєфні. Мікроскопічні дослідження виявляють явища набряку мозку і некротичні зміни в нервових клітинах. Нейрони набряклі, погано пофарбовані клітини різко змінені. Залежно від інтенсивності аноксии в більшій чи меншій мірі уражаються макро- і мікроглії, що служить підставою до виділення неповного або повного некрозу мозкової тканини. У більш пізні терміни в області інфаркту виявляється розм'якшення — сіра, кришаться маса.
Клініка ішемічного інсульту
Ішемічний інсульт розвивається найбільш часто у осіб похилого та середнього віку, але іноді може спостерігатися і у більш молодих людей. Розвитку інфаркту мозку нерідко передують ПНМК, які проявляються нестійкими осередковими симптомами. ПНМК частіше локалізуються в тому ж судинному басейні, в якому пізніше розвивається інфаркт мозку.
Ішемічний інсульт може розвиватися в будь-який час доби . Нерідко він виникає під час вона або відразу після нього. В окремих випадках ішемічний інсульт розвивається -після фізичного навантаження, прийому гарячої ванни, вживання алкоголю, рясного прийому їжі. Нерідко спостерігається виникнення ішемічного інсульту після психоемоційного перенапруження.
Найбільш характерно для ішемічного інсульту поступовий розвиток вогнищевих неврологічних симптомів , яке відбувається, як правило, протягом 1-3 ч і значно рідше протягом 2-3 доби. Іноді спостерігається мерехтливий тип розвитку симптомів, коли ступінь вираженості їх то посилюється, то слабшає або на короткий період часу зникає зовсім.
Крім типового, повільного, поступового розвитку вогнищевих симптомів інфарктів мозку в 1/3 випадків спостерігається гострий, раптове, блискавичне (апоплектиформное, їх виникнення, характерне для гострої закупорки великої артерії, при цьому, як правило, вогнищеві симптоми відразу ж максимально виражені і поєднуються з загальмозкові симптоматикою. Значно рідше спостерігається псевдотуморозная розвиток, коли осередкові симптоми інфаркту мозку посилюються протягом декількох тижнів, що обумовлено наростанням окклюзірующего процесу в судинах мозку.
Характерною особливістю ішемічного інсульту є переважання вогнищевих симптомів над загальномозковими. Загальмозкові симптоми — головний біль, блювота, сплутана свідомість спостерігаються найчастіше при апоплектиформна розвитку і можуть наростати в міру збільшення набряку мозку, що супроводжує обширний інфаркт мозку. Осередкові симптоми залежать від локалізації мозкового інфаркту. На підставі клінічного оімлтомокомплекса можна судити про величину, локалізації інфаркту та про судинному басейні, в руслі якого він розвивається. Найбільш часто інфаркти мозку виникають в басейні внутрішніх сонних артерій. Частота інфарктів в системі внутрішніх сонних артерій перевищує частоту інфарктів в вертебробазилярном басейні в 5-6 разів.
Інфаркти в басейні внутрішньої сонної артерії.
Внутрішня сонна артерія часто уражається атеросклеротичним процесом, причому атеросклеротический стеноз і тромбоз частіше виникає в області біфуркації каротид, в синусі внутрішньої сонної артерії або в області сифона. Рідше оклюзія розвивається в загальній сонній або зовнішньої сонної артерії.Стеноз і навіть повна закупорка внутрішньої сонної артерії може не супроводжуватися розвитком інфаркту мозку, якщо оклюзія локалізується екстракраніального, на шиї. В цьому випадку повноцінний артеріальний коло великого мозку здійснює заместительное кровообіг з внутрішньої сонної артерії іншої сторони або з хребетних артерій. При дефектності колатеральногокровообігу стенозуючих поразку екстракраніального відділу внутрішньої сонної артерії в початковому періоді протікає нерідко у вигляді ПНМК, клінічно виражаються короткочасної слабкістю в кінцівках, онімінням в них, афатічеекімі розладами, зниженням зору на одне око.
При интракраниальной оклюзії (тромбозі) внутрішньої сонної артерії, що протікає з роз'єднанням артеріального кола великого мозку, розвиваються геміплегія і грубо виражені загальномозкові симптоми — розлад свідомості, головний біль , блювота, з подальшим порушенням вітальних функцій, обумовленим сдавленней і зміщенням ствола бурхливо розвиваються набряком мозку. Інтракраніальна оклюзія внутрішньої сонної артерії нерідко закінчується летально.
У зоні васкуляризації передньої мозкової артерії великі інфаркти розвиваються рідко. Вони можуть спостерігатися при закупорці основного стовбура передньої мозкової артерії після відходження від неї передній сполучної артерії.
Клінічна картина при інфарктах в басейні передньої мозкової артерії характеризується спастичним геміпарез протилежних кінцівок з переважним розвитком парезу в проксимальному відділі руки і дистальному відділі ноги. Може відзначатися затримка сечі. З патологічних стопного рефлексів з великою постійністю викликаються рефлекси сгибательного типу — Россолимо, Бехтерева, а також спостерігаються хапальний рефлекс і рефлекси орального автоматизму. Іноді виявляються негрубі розлади чутливості на паралізованою нозі. Внаслідок ішемії додаткової мовної зони на медіальної поверхні півкулі можливий розвиток дизартрії, афонії і моторної афазії.
При осередках інфаркту в басейні передньої мозкової артерії відзначаються порушення психіки, зниження критики, пам'яті, елементи невмотивованого поведінки. Зазначені вище порушення психіки грубіше виражені при двосторонніх осередках інфарктів в басейні передніх мозкових артерій.
Найчастіше в басейні передніх мозкових артерій розвиваються невеликі інфаркти, зумовлені ураженням гілок передньої мозкової артерії. Так, при оклюзії парацентральной гілки розвивається монопарез стопи, що нагадує периферичний парез, а при ураженні околомозолістой гілки виникає лівостороння апраксія. Поразка премоторной області з провідними шляхами в цій зоні викликає грубе підвищення м'язового тонусу, значно перевершує ступінь парезу, і різке підвищення сухожильних рефлексів з патологічні рефлекси сгибательного типу.
Найбільш часто інфаркти розвиваються в басейні середньої мозкової артерії , яка може бути уражена в області основного стовбура до атхожденія глибоких гілок, після їх відгалуження і в області окремих гілок, що і визначає клінічну картину інфаркту в кожному конкретному випадку.
При оклюзії основного стовбура середньої мозкової артерії спостерігається обширний інфаркт, що приводить до розвитку геміплегії, гемігіпестезія в протилежних вогнища інфаркту кінцівках і гемианопсии. При ураженні лівої середньої мозкової артерії, т. Е. При левополушарной локалізації інфаркту, розвивається афазія, частіше тотальна, при правопівкульних інфарктах в зоні васкуляризації середньої мозкової артерії спостерігається анозогнозия (неусвідомлення дефекту, ігнорування паралічу та ін.).
Інфаркт в басейні глибоких гілок середньої мозкової артерії викликає спастическую геміплегію, іноді з порушенням чутливості і моторну афазію при осередках в лівій півкулі.
Поразка корково-підкіркових гілок призводить до розвитку геміпарезу з переважним порушенням рухів в руці, розладу всіх видів чутливості, гемианопсии, а також сенсорно-моторної афазії, порушення письма, рахунку, читання, праксису (при левополушарной локалізації інфаркту) і анозогнозии і розладу схеми тіла при локалізації інфаркту в правій півкулі.
У басейні задніх гілок середньої мозкової артерії інфаркт проявляється синдромом ураження тім'яно-вісочнозатилочвой області — гемігіпестезіей, порушенням глибокої чутливості, Астереогноз, аферентним парезом кінцівок, гемианопсией, а при левополушарной локалізації процесу -Сенсорний афазією, аграфією, акалькулией і апраксией.
Інфаркти в басейні окремих гілок середньої мозкової артерії виражаються менш грубою симптоматикою: при ураженні роландовой артерії спостерігається гемипарез з переважанням слабкості в руці, при інфаркті в руслі задньої тім'яної артерії відзначається гемігіпестезія всіх видів чутливості з розвитком аферентного парезу, а в басейні прецентральной артерії — парез ніжнеміміческой мускулатури, мови і слабкість в кисті, моторна афазія (при ураженні домінантної півкулі).
При порушенні кровообігу в судинах вертебробазилярного басейну спостерігаються системне запаморочення, порушення слуху і зору, напади раптового падіння, вегетативні розлади, іноді виникають кома, тетраплегія, порушення дихання і серцевої діяльності, дифузна гіпотонія або горметония.
Інфаркт при оклюзії хребетної артерії призводить до розвитку симптомів з боку довгастого мозку, мозочка і частково шийного відділу спинного мозку. Вогнища інфаркту при закупорці хребетної артерії можуть розвиватися не тільки в області мозочка і довгастого мозку, а й на віддалі, в області середнього мозку, в зоні суміжного кровообігу, двох судинних систем — хребетного і каротидного басейнів. Інфаркти в зоні суміжного кровообігу більш характерні для оклюзії екстракраніального відрізка хребетної артерії. Можливий розвиток згаданих вище нападів раптового падіння з втратою м'язового тонусу (drop attace), а також вестибулярних порушень (запаморочення, атаксія, ністагм), мозочкових розладів координації та статики, окорухових розладів, рідко — зорових порушень.
Для оклюзії интракраниального відділу хребетної артерії характерні синдроми Валленберга-Захарченко, Бабинського-Нажотта і інші синдроми ураження нижніх відділів стовбура. Інфаркти в басейні гілок хребетної артерії, що живлять довгастий мозок і мозочок, супроводжуються найчастіше розвитком синдрому Валленберга-Захарченко, обумовленого ураженням нижньої задньої мозочкової артерії -найвищої великої гілки хребетної артерії.
Клінічно на стороні інфаркту відзначаються параліч м'язів глотки, м'якого піднебіння, гортані (внаслідок чого розвиваються дисфагія і дисфонія), мозочкова атаксія (динамічна і статична зі зниженням м'язового тонусу), синдром Горіера (внаслідок ураження гіпоталамоспінального симпатичного шляху), гіпестезія больової і температурної чутливості на половині обличчя, що відповідає за поразки, і на протилежній половині тулуба, обумовлена поразкою спинального спадного корінця трійчастого нерва і спіноталаміческого шляху.
Симптоми ураження пірамідного шляху, як правило, відсутні або виражені слабо. Частими симптомами оклюзії нижньої мозочкової артерії є запаморочення, блювота, ністагм, пов'язані з ураженням вестибулярних ядер. Існує кілька варіантів синдрому Валленберга-Захарченко, обумовлених різною кількістю гілок задньої нижньої артерії мозочка, а також індивідуальними особливостями колатеральногокровообігу.
При окклюзирующих процесах в хребетних артеріях розвивається близький до синдрому Валленберга-Захарченко синдром Бабинського-Нажотта (параліч піднебінної фіранки при схоронності функції голосових зв'язок, перехресний геміпарез з гемігіпестезіей диссоциированного характеру і мозочкова атаксія на боці вогнища).
Інфаркти в області моста мозку можуть бути викликані окклюзией як гілок основної артерії, так і головного її стовбура. Інфаркти в області гілок основної артерії відрізняються великим поліморфізмом клінічних проявів, геміплегія контралатеральних кінцівок поєднується з центральним паралічем лицьового і під'язикового нервів і з мостовим паралічем погляду або з паралічем відвідного нерва на стороні поразки. Може спостерігатися на стороні вогнища і периферичний парез лицьового нерва (альтернирующий синдром Фовіля). Можлива альтернирующая гемігіпестезія-порушення больової і температурної чутливості на обличчі на стороні інфаркту і на протилежній половині тулуба.
Двосторонні інфаркти в області моста викликають розвиток тетрапареза, псевдобульбарного синдрому і мозочкових симптомів.
Оклюзія основної артерії призводить до розвитку обширного інфаркту з симптомами ураження моста мозку, мозочка, середнього мозку і гіпоталамуса, а іноді і корковими симптомами з боку потиличних часток мозку.
Гостро виникла закупорка основної артерії призводить до розвитку симптомів перш за все з боку середнього мозку і моста мозку — розвиваються розлад свідомості, окорухові порушення, обумовлені ураженням III, IV , VI пар черепних нервів, тетраплегія, порушення м'язового тонусу, двосторонні патологічні рефлекси, тризм нижньої щелепи, гіпертермія та порушення вітальних функцій. У переважній кількості випадків оклюзія основної артерії закінчується летально.
Середній мозок кров'ю артеріями, що відходять від задніх мозкових і основний артерій. При інфаркті в басейні цих артерій спостерігається нижній синдром червоного ядра — параліч окорухового нерва на стороні вогнища, атаксія і интенционное тремтіння в контралатеральних кінцівках за рахунок ураження верхньої мозочкової ніжки поблизу червоного ядра (на ділянці від перехрещення Вернекінга до червоного ядра) або самого червоного ядра. При ураженні передніх відділів червоного ядра можуть бути відсутні симптоми з боку окоруховогонерва, але спостерігатися хореоформний гиперкинез.
При інфаркті в басейні четверохолмной артерії розвивається параліч погляду вгору і парез конвергенції (синдром Паріно), іноді поєднується з ністагмом. Інфаркт в області ніжки мозку викликає розвиток синдрому Вебера.
Інфаркт в басейні задньої мозкової артерії виникає як у зв'язку з оклюзією самої артерії або її гілок, так і при ураженні основної або хребетної артерій. Ішемія в басейні кірки про — під кор ков и х гілок задньої мозкової артерії може захопити потиличну частку, III і частково II скроневі звивини, базальні і медіально-базальні звивини скроневої частки (зокрема, гіппокамповой звивину). Клінічно розвивається гомонимная гемианопсия з збереженням макулярного (центрального) зору, ураження кори потиличної області (поля 18, 19) може привести до зорової агнозии і явищ метаморфопсії. При л евополушарних інфарктах ib басейні задньої мозкової артерії можуть спостерігатися алексія і легко виражена сенсорна афазія. При поширенні ішемії на гіппокамповой звивину і маміллярних тіла виникають розлади пам'яті типу корсаковского синдрому з переважним порушенням короткочасної пам'яті на поточні події, при збереженні пам'яті на віддалені минулі події.
Поразка задненіжніх відділів кори тім'яної області на кордоні з потиличної призводить до порушення оптико-просторового Гнозис, дезорієнтація в місці і часу. Можливий розвиток і емоційно-афективних порушень у вигляді тривожно-депресивного синдрому, стану психомоторного збудження з нападами страху, гніву, люті.
При формуванні постішеміческіх вогнищ судомної активності розвивається скронева епілепсія, що характеризується поліморфізмом епілептичних пароксизмів, спостерігаються великі епілептичні припадки, абсанси, психічні еквіваленти та ін.
При інфаркті в басейні глибоких гілок задньої мозкової артерії (a. thalamogeniculata) розвивається таламический синдром Дежерина-Русею — гемианестезия, гиперпатия, тимчасовий геміпарез, геміавопеія, гемиатаксия, а інфаркт в басейні a. thalamoperforata клінічно характеризується розвитком важкої атаксії, хореоатетоз, «таламической руки» і интенционного тремору в контралатеральних кінцівках. При ураженні дорсомсдіалиюго ядра зорового бугра іноді розвивається акінетичний мутизм. У перші дні ішемічного інсульту температурної реакції і суттєвих зрушень в периферичної крові, як правило, не спостерігається. Однак при великих інфарктах з вираженим набряком мозку з залученням в процес мозкового стовбура можливий розвиток гіпертермії і лейкоцитозу, а також підвищення вмісту цукру і сечовини в периферичної крові.
З боку системи згортання і протівоовертивающей системи крові у більшості хворих на ішемічний інсульт відзначається зрушення в бік гіперкоагуляції крові. Підвищення фібриногену, протромбіну, толерантності плазми до гепарину, поява фібриногену В при зниженою або нормальною фібрінолітічеокой активності зазвичай виражено в перші 2 тижні захворювання. У ряді випадків можлива зміна гіперкоагуляції крові гіпокоагуляцією. При цьому відзначається (раптове падіння рівня фібриногену в крові, зменшення протромбінового індексу і зниження кількості тромбоцитів. Перераховані плазмові (фиб «ріноген, протромбін) і клітинні фактори згортання крові споживаються на внутріеоеудістое згортання, а позбавлена факторів, що згортають кров проникає через судинну стінку, викликаючи геморагічні ускладнення. Розвиваються поширені геморагічні ускладнення, які є наслідком внутрішньосудинного згортання (синдром споживання, тромбогеморрагіческій синдром, синдром діесемінірованного внутрішньосудинного згортання).
У хворих з ішемічним інсультом в гострому періоді відзначається достовірно висока агрегація і адгезивність тромбоцитів. На найбільш високих цифрах вона тримається протягом 10-14 днів, повертаючись до субнормальний показниками на 30-й день інсульту. Спинномозкова рідина зазвичай прозора з нормальним вмістом білка і клітинних елементів. Можливе невелике збільшення білка і лімфоцітарвого цитоза при осередках інфаркту, що межують з лікворних простором і викликають реактивні зміни в епендими шлуночків і мозкових оболонках.
Ехоенцефалографія при ішемічному інсульті зазвичай не вказує зміщення серединного М-еха сигналу. Однак при великих інфарктах в зв'язку з розвитком набряку і зміщенням стовбура мозку можуть спостерігатися зміщення М-еха вже до кінця першої доби з моменту розвитку інфаркту. Ультразвукова флюорометрія (метод Доплера) дозволяє виявити оклюзію і виражені стенози магістральних артерій голови. Важливу інформацію дає ангіографія, яка виявляє у хворих на інфаркт мозку наявність або відсутність окклюзірующего і стенозирующего процесів в екстра-та інтракраніальних судинах головного мозку, а також функціонують шляху колатерального кровообігу. На ЕЕГ виявляються міжпівкульна асиметрія і іноді вогнище патологічної активності. Характерні зміни при інфаркті мозку виявляє комп'ютерна томографія, яка виявляє вогнище зниженої щільності паренхіми мозку в зоні інфаркту та периинфарктной області на відміну від змін, які виявляються при крововиливі в мозок, коли томографія виявляє протилежні зміни — вогнище підвищеної щільності.
Діагноз ішемічного інсульту
У більшості випадків діагностувати інсульт не представляє великих труднощів. Гостре розвиток вогнищевих і загальномозкових симптомів у пацієнтів зрілого та похилого віку, які страждають на атеросклероз або гіпертонію, а також у молодих осіб на тлі системного судинного захворювання або хвороби крові, як правило, вказує на гостре порушення мозкового кровообігу — інсульт або ПНМК. Однак завжди слід мати на увазі захворювання, що викликають церебральні порушення, які не є наслідком ураження судинної системи, з якими необхідно диференціювати інсульт.
До їх числа відносяться:
- черепно-мозкова травма в гострому періоді (контузія мозку , травматичні подоболочечние крововиливи),
- інфаркт міокарда, що супроводжується порушенням свідомості,
- пухлини головного мозку з апоплектиформна розвитком, обумовленим крововиливом в пухлину,
- епілепсія, при якій розвиваються постпріпадочной паралічі,
- гіпер- або гіпоглікемічна кома,
Особливо скрутний диференційний діагноз в тих випадках, коли у хворого є розлад свідомості. Якщо хворий виявлено в ситуації, при якій можна припускати травму, він повинен бути ретельно оглянутий з метою встановлення саден на голові і на тілі, після чого необхідна термінова рентгенографія черепа, ехоенцефалографія і дослідження спинномозкової рідини. При епі- і субдуральних гематомах травматичного походження порушення цілості кісток черепа, зміщення серединного сигналу М-еха, домішки крові в спинномозковій рідині та наявність безсудинного вогнища на ангиограмме дозволяють повністю визначити не тільки характер, але і топіку ураження.
Слід також мати на увазі, що при гострої серцевої слабкості іноді спостерігається порушення свідомості, обумовлене різким зниженням об'ємного мозкового кровотоку і вторинною гіпоксією мозкової тканини. При цьому крім спутаного свідомості відзначаються порушення дихання, блювота, падіння артеріального тиску. Вогнищевих симптомів ураження півкуль і стовбура головного мозку не виявляється, за винятком тих випадків, коли інфаркт міокарда поєднується з розвитком мозкового інфаркту.
Нерідко (особливо в осіб похилого віку) виникають труднощі при диференціації пухлини мозку, ускладненої крововиливом, і судинного процесу. Мультиформні сповгіобластоми можуть протікати деякий час латентно, і перші прояви їх виникають в результаті крововиливу в пухлину. Лише подальший перебіг з наростанням симптомів ураження головного мозку дозволяє розпізнати пухлину. Діагноз епілепсії, гіпер- або гіпоглікемічної коми, а також уремії підтверджується або відкидається на підставі уточнених анамнестичних відомостей, кількості вмісту цукру і сечовини в крові, аналізу сечі і показників ЕЕГ.
Таким чином, дані анамнезу, клінічних особливостей, дослідження спинномозкової рідини, очного дна, луна і електроенцефалографії, ЕКГ, показники вмісту цукру і сечовини крові, а також рентгенографічні дослідження — краніографія, ангіографія дозволяють правильно диференціювати інсульт від інших апоплектіформ але протікають захворювань.
Відрізнити інфаркт мозку від геморагічного інсульту в ряді спостережень представляє великі труднощі. Проте визначення характеру інсульту необхідно для проведення диференційованого лікування. При цьому слід визнати, що немає окремих (Симптомів, суворо патогномонічних для крововиливи або інфаркту мозку. Раптовий розвиток інсульту, характерне для крововиливи, спостерігається нерідко при оклюзії великої судини, що приводить до розвитку гострого інфаркту мозку. І в той же час при крововиливах, особливо диапедезного характеру, симптоми ураження речовини мозку можуть наростати протягом декількох годин, поступово, що вважається найбільш характерним для розвитку інфаркту мозку.
Добре відомо, що під час сну розвивається, як правило, інфаркт мозку, проте хоча і багато рідше, але і крововиливи в мозок можуть відбуватися вночі. Виражені загальномозкові симптоми, такі характерні для крововиливи в мозок, нерідко спостерігаються при великих інфарктах мозку, що супроводжуються набряком. Артеріальна гіпертонія частіше ускладнюється крововиливом, однак супутній гіпертонії атеросклероз нерідко є причиною розвитку інфаркту, спостерігається часто у хворих, які страждають на атеросклероз з артеріальною гіпертензією. Високі цифри артеріального тиску в момент інсульту не завжди слід розглядати як його причину, підвищення артеріального тиску може бути і реакцією стволового судинного центру на інсульт.
З наданого видно, що окремі симптоми мають відносну діагностичну цінність для визначення характеру інсульту. Однак певні поєднання симптомів з даними додаткових досліджень дозволяють правильно розпізнати характер інсульту в переважній більшості випадків. Так, розвиток інсульту уві сні або відразу після сну на тлі серцевої патології, особливо що супроводжується порушенням ритму серцевої діяльності, інфаркт міокарда в анамнезі, помірна артеріальна гіпертонія — характерні для ішемічного інсульту. А початок інсульту з гострого головного болю, повторних рвот днем, особливо в момент емоційного напруження у хворого, який страждає на гіпертонічну хворобу, порушення свідомості найбільш характерні для крововиливи в мозок. При цьому необхідно врахувати, що лейкоцитоз із зсувом вліво, з'явився в першу добу інсульту, підвищення температури тіла і наявність крові або ксантохроміі в спинномозковій рідині, зміщення М-еха і наявність вогнища підвищеної щільності при комп'ютерній томографії вказують на геморагічний характер інсульту.
Приблизно в 20% спостережень макроскопически спинномозкова рідина при крововиливі буває прозорою і безбарвною. Однак мікроскопічне дослідження у цій категорії хворих дозволяє виявити еритроцити, а спектрофотометром виявляють пігменти крові (білірубін, окси- і метгемоглобін). При інфаркті рідина безбарвна, прозора, можливе підвищення вмісту білка. Дані коагулограми, а також ЕЕГ і РЕГ достовірно не підтверджують характер інсульту. Інформативним методом слід визнати ангіографію, проте артеріографіческіе дослідження через небезпеку ускладнень рекомендують проводити в тих випадках, коли є доцільність хірургічного лікування. В даний час найбільшою значущістю при визначенні характеру інсульту мають дані комп'ютерної томографії, що дозволяє виявити осередки різної щільності при інфаркті мозку і крововилив в мозок.
Геморагічний інфаркт відноситься до числа найбільш важко діагностованих станів. Щодо механізму розвитку геморагічних інфарктів серед патоморфології і патофізіологів поки немає єдності поглядів. При геморагічному інфаркті спочатку розвивається ішемічне ураження, а потім (або одночасно) з'являється крововилив в інфарктну зону.
Геморагічні інфаркти відрізняються від іншої форми порушення мозкового кровообігу — геморагічного диапедезного просочування як за механізмом розвитку, так і по морфологічних змін [Колтовер А. Н., 1975]. Найчастіше геморагічні інфаркти локалізуються в сірій речовині, корі головного мозку, підкіркових гангліях і зоровому горбі. Розвиток геморрагий в осередку ішемії більшість дослідників пов'язують з раптовим наростанням кровотоку в ішемічної зоні через швидке припливу крові в цю область за коллатералям.
Геморагічні зміни частіше бувають при великих, швидко формуються інфарктах мозку.
За розвитком захворювання і клінічними проявами геморагічний інфаркт нагадує геморагічний інсульт — крововилив в мозок по типу гематоми або по типу геморагічного диапедезного просочування, тому геморагічний інфаркт діагностується за життя значно рідше, ніж на розтині.
Лікування ішемічного інсульту
Система лікування будується на підставі тих уявлень про патогенез мозкового інсульту, які склалися за останні роки. Вона включає комплекс лікувальних заходів невідкладної допомоги хворим з мозковим інсультом, незалежно від його характеру (недиференційована допомогу) і диференційоване лікування інфаркту мозку.
Недиференційована терапія спрямована на нормалізацію життєво важливих функцій — дихання і серцевої
діяльності. До неї відносяться — боротьба з набряком мозку, гіпертермією, а також профілактика ускладнень інсульту. Перш за все необхідно забезпечити вільну прохідність дихальних шляхів за допомогою спеціальних відсмоктувачів, ротових та носових воздуховодов, протирання ротової порожнини хворого, утримування нижньої щелепи. У разі, якщо заходи, спрямовані на усунення закупорки дихальних шляхів, виявляються неефективними, виробляють інтубацію і трахеостомию.
Інтубацію або трахеостомию використовують при раптовій зупинці дихання, прогресуючому розладі дихання, при бульбарної і псевдобульбарной симптоматиці, коли є небезпека аспірації . При раптовій зупинці дихання і відсутності апарату необхідно робити штучне дихання з рота в рот, з рота в ніс.
При супутньому набряку легенів показані кардиотоники: вводять 1 мл 0,06% розчину коргликона або 0,5 мл 0,05% розчину строфантину в / в. Крім вищевказаних коштів рекомендується вдихання кисню з парами спирту через кисневий інгалятор або апарат Боброва з метою зменшення піноутворення в альвеолах. Інгаляції парів спирту тривають протягом 20-30 хв, потім повторюються після 20-хвилинної перерви.
Піднімають головний кінець ліжка з метою надання піднесеного положення хворому. Призначають фуросемід (лазикс) в / м, димедрол, атропін. При різкому падінні артеріального тиску призначають 1 мл 1% розчину мезатону, 1 мл 0,06% розчину коргликона, 1 мл 0,1% розчину норадреналіну, 0,05 г гідрокортизону з 5% розчином глюкози або розчином бікарбонату натрію в / в крапельно зі швидкістю 20-40 крапель в хвилину. Інфузійну терапію слід проводити під контролем показників кислотно-лужної рівноваги та електролітного складу плазми.
Компенсація водно-електролітного балансу і корекція кислотно-лужної рівноваги проводяться у хворих, що знаходяться в несвідомому стані. Необхідно вводити парентерально рідини в обсязі 2000-2500 мл на добу в 2-3 прийоми.
Вводять ізотонічний розчин хлориду натрію, розчин Рінгера-Локка, 5% розчин глюкози. Так як порушення кислотно-лужної рівноваги часто супроводжується дефіцитом калію, то необхідно застосовувати нітратну сіль калію або хлорид калію в кількості до 3-5 г на добу. Для усунення ацидозу поряд зі збільшенням легеневої вентиляції і оксигенотерапией, а також заходами, що збільшують серцевий викид, вводять в / в 4-5% розчин бікарбонату натрію (200-250 мл).
Заходи, спрямовані на боротьбу з набряком мозку, проводять при великих мозкових інфарктах. У цих випадках призначають фуросемід (лазикс), 1-2 мл ib / m або всередину в таблетках по 0,04 г один раз в день, 5-10 мл 5% розчину аскорбінової кислоти з метою зменшення проникності судинної стінки. Протинабрякову дію мають гідрокортизон і преднізолон, які доцільно призначати протягом перших 2-3 днів в залежності від вираженості набряку мозку. Хороший протинабряковий ефект може бути отриманий при використанні маннита, що є осмотичним діуретиком. Менш бажано застосування сечовини, так як наступає слідом за потужним протинабрякову ефектом викарное розширення судин мозку може привести до повторного ще більш грубому набряку і можливого кровотечі в паренхіму мозку. Дегидратирующим дію має гліцерин, що підвищує осмотичний тиск крові, що не порушує електролітного балансу.
Необхідно застосування засобів, спрямованих на попередження та усунення гіпертермії. При температурі тіла 39 ° С і вище призначають 10 мл 4% розчину амідопірину або 2-3 мл 50% розчину анальгіну в / м. Знижують температуру суміші, що складаються з димедролу, новокаїну, амидопирина. Рекомендується також регіонарна гіпотермія великих судин (бульбашки з льодом на область сонних артерій на шиї, в пахвові і пахові області).
З метою попередження пневмонії необхідно вже з першої доби інфаркту повертати хворого в ліжку через (кожні 2 год, на грудну клітку слід ставити кругові банки, чергуючи їх через день з гірчичниками. При підозрі на розвиток пневмонії призначають сульфаніламідні препарати і антибіотики. Необхідний контроль за діяльністю сечового міхура і кишечника. При затримці сечі показана катетеризація 2 рази на добу з промиванням сечового міхура антисептичними засобами. Щоб уникнути пролежнів, необхідно стежити за чистотою білизни, станом ліжку — усувати складки простирадлом, нерівності матраца, протирати тіло камфорним спиртом.
При лікуванні інфаркту мозку необхідно спрямувати всі зусилля на поліпшення порушеного церебрального кровообігу і спробувати усунути розвинулася ішемію. Це певною мірою вдається зробити за рахунок посилення серцевої діяльності і поліпшення венозного відтоку крові, тому доцільно застосування кардіотонічних засобів, що збільшують ударний і хвилинний об'єм серця, а також поліпшують відтік венозної крові з порожнини черепа (строфантину або коргликона в / в).
Сосудорасширяющие препарати доцільно призначати у вигляді підшкірних або внутрішньом'язових ін'єкцій в тих випадках, коли необхідно добитися гіпотензивного ефекту, знизити дуже високий артеріальний тиск, уникнути небезпеки розвитку геморагічного ускладнення в зоні інфаркту мозку. Уявлення про те, що сосудорасширяющими препаратами можна досягти поліпшення мозкового кровообігу і збільшення локального мозкового кровотоку, в останні роки піддається перегляду. Деякі дослідники висловлюють точку зору про недоцільність і навіть шкідливість застосування вазодилататорів при інфаркті мозку. Ці висловлювання засновані на тому, що в експерименті, а також при ангіографічної вивченні стану судинної системи головного мозку і при дослідженні локального мозкового кровотоку за допомогою радіоактивного ксенону у хворих отримані дані про те, що судини в області ішемії або зовсім не реагують на подразники, або реагують слабо, а іноді навіть парадоксально. Тому звичайні церебральні вазодилататори (папаверин та ін.) Ведуть до розширення лише непостраждалих судин, відтягують на себе кров з області інфаркту. Це явище отримало назву феномена внутрімоз-кового обкрадання.
Судини периинфарктной зони, як правило, бувають максимально розширені (зокрема, внаслідок місцевого ацидозу), а розширення судин непораженной області під впливом судинорозширювальних засобів може зменшити тиск в розширених колатералей і тим самим зменшити кровопостачання ішемізованої області [Olesen, 1974].
З рекомендаціями деяких клініцистів — застосовувати судинорозширювальні засоби в тих випадках, коли в якості основної причини інфаркту передбачається ангіоспазм, важко погодитися, так як причинний залежність інфаркту мозку від ангиоспазма ще не доведена, а на викликає інфаркт мозку ангіоспазм після розриву аневризми папаверин і інші вазоактивні препарати не діють [Кандель Е '1975, Flamm, 1972].
Для поліпшення колатерального кровообігу і мікроциркуляторного ланки в зоні інфаркту мозку доцільно призначати лікарські засоби, що зменшують в'язкість крові і знижують агрегаційні властивості її формених елементів. З цією метою в / в вводять 400 мл низькомолекулярного декстрану — реополіглюкіну. Препарат вводять крапельно, з частотою 30 крапель в хвилину, щодня, протягом 3-7 днів.
Введення реополіглюкіну покращує локальний мозковий кровотік, призводить до антітромбогенному дії. Ефект реополіглюкіну найбільш виражений в артеріолах, прекапиллярах, капілярах.
В результаті різкого зниження агрегації еритроцитів і тромбоцитів зменшується інтенсивність мікроциркуляторного синдрому осадження, що виражається низьким перфузійним тиском, уповільненням кровотоку, підвищеною в'язкістю крові, агрегацією і стазом кров'яних елементів, утворенням тромбів. Через відомого гіперволемічна і гіпертензивної дії реополіглюкіну необхідний контроль за АТ, причому тенденція до артеріальної гіпертензії може бути відрегульована зниженням частоти крапель розчину, що вводиться. Антиагрегаційний ефект реополіглюкіну спостерігається протягом 4-6 год, тому доцільно в інтервалах між введенням реополіглюкіну і після припинення його ін'єкцій рекомендувати перорально аспірин, монобромістую камфору, трентал та ін.
антиагрегаційних ефект може бути досягнутий в / в введенням 10 мл 24% розчину еуфіліну, а також 2 мл 2% розчину папаверину. Похідні аминофиллина, так само як і папаверин, чинять інгібуючу дію на фосфодіестеразу, в силу чого накопичується циклічна, аденозінмонофосфорной кислота в клітинах крові, що є потужним інгібітором агрегації. Регулярний прийом інгібіторів агрегації клітинних елементів крові перорально після п'ятиденного або тижневого застосування їх у вигляді ін'єкцій дозволяє протягом усього гострого періоду інфаркту домогтися надійного попередження тромбоутворення в усій судинній системі в цілому. Прийом інгібіторів агрегації доцільно продовжувати протягом двох років, що є небезпечним періодом для розвитку повторних інфарктів. Застосування антиагрегантів клітинних елементів крові дозволило в останні роки в значній мірі зменшити використання антикоагулянтів, що вимагають для свого застосування регулярного контролю за згортанням крові і протромбінового індексом. У випадках же тромбоемболічного синдрому, на тлі якого розвинувся інфаркт мозку, показано застосування фібринолітичних препаратів з антикоагулянтами.
Антикоагулянтная терапія починається з застосування антикоагулянту прямої дії — гепарину. Гепарин призначають в / в або в / м в дозі 5000-10 000 ОД 4-6 разів на день протягом 3-5 днів. При в / в введенні дія гепарину настає негайно, при в / м — через 45-60 хв. Спочатку вводять в / в 10 000 ОД гепарину, потім через кожні 4 год гепарин вводять в / м по 5000 ОД.
Лікування гепарином слід проводити під контролем часу згортання крові. Оптимальним вважається подовження згортання в 2.5 рази. За 3 дні до відміни гепарину призначають непрямі антикоагулянти — фенилин всередину (або синкумар, омефін тощо.) В дозі 0,03 г 2-3 рази на день, одночасно знижуючи добову дозу гепарину на 5000 ОД. Лікування анти «коагулянтами непрямої дії проводять під контролем протромбіновото індексу, який не слід знижувати більш ніж до 40%.
Для тромболітичної ефекту застосовують фибринолизин. Призначення фибринолизина показано в першу добу і навіть годинник від початку інфаркту. Фибрино лізин необхідно вводити одночасно з гепарином.
У комплексному лікуванні інфаркту мозку в останні роки використовують кошти, що резистентність мозкових структур до гіпоксії. Доцільність застосування антигіпоксантів визначається тим, що порушення обмінних процесів в клітинах мозкової паренхіми зазвичай передують за часом грубому ураження мозку в формі набряку і, крім того, є однією з провідних причин набряку.
Висловлено припущення , що ні набряк мозку, а саме метаболічні зрушення і енергетичний дефіцит, якщо вони виникають на великій території мозку або при швидко розвивається ішемії, є чинником, що визначає порушення свідомості та інші загальномозкові симптоми при ішемічному інсульті. У зв'язку з цим антигипоксическая терапія може вважатися більш перспективною, ніж лікування розвиненого набряку мозку. Доцільність призначення антігіпокоіческой терапії визначається і тим, що в умовах гостро настав дефіциту мозкового кровопостачання і дезорганізації метаболізму вигідніше тимчасово знизити енергетичні потреби мозку і тим самим в якійсь мірі підвищити його резистентність до гіпоксії.
Відповідно вважається виправданим призначення ліків, що володіють інгібуючим дією на енергетичний баланс. З цією метою застосовують антипіретичні препарати і реґіонарну гіпотермію, нові синтетичні засоби, які надають гальмівну дію на ферментативні процеси і метаболізм у мозку, а також речовини, що підвищують енергопродукцію в умовах гіпоксії. До таких речовин відносяться похідні метілфеназіна, деривати сечовини — гутімін і пірацетам (ноотропіл), які призначають по 5 мл в / в або по 1 мл 3 рази на день в / м. Ця група антигипоксантов робить позитивний вплив на процеси тканинного дихання, фосфорилювання і гліколізу. З позитивного боку зарекомендував себе фенобарбітал, чітко знижує споживання кисню мізкам і підвищує пережіваемость мозку шляхом зменшення метаболічних процесів і уповільнення накопичення внутрішньоклітинної рідини.