Клітини статевих залоз виділяють багато активних речовин. У нормі в яєчниках у жінок і в яєчках у чоловіків виробляється особливу хімічну сполуку — ингибирующая субстанція Мюллера (Антимюллерів гормон, АМГ).
За будовою АМГ є протеїном з вуглеводним компонентом. Молекулярна маса гормону становить близько 140 кДа. Під час активації від основної частини інгібуючої субстанції відділяється фермент з молекулярною вагою 25 кДа. Гормон відносять до групи? -трансформірующіх Факторів клітинного росту.
У геномі людини інформація про структуру АМГ зберігається в 19 хромосомі.
Дослідження, які довели існування інгібуючої субстанції Мюллера були проведені в середині двадцятого століття.
Вчені виявили, що під час внутрішньоутробного розвитку яєчко у плоду чоловічої статі виділяє особливий фактор, що провокує регресію ембріонального протоки-попередника матки, труб і піхви. Це речовина отримала назву антімюллерова гормону.
Довгий час роль АМГ у дівчат і жінок була невідома. В останні роки отримані переконливі дані про дію субстанції на репродуктивну функцію. Тоді ж було запропоновано використовувати АМГ як маркер здоров'я статевої сфери у жінок.
У практичній медицині Антимюллерів гормон оцінюють гінекологи, андрологи, репродуктологи. Цей показник є одним з важливих показників функціональної активності і резервів жіночої статевої системи.
АМГ у чоловіків
Антимюллерів гормон виділяється у чоловіків клітинами Cертолі. Ці тільця розташовані в насінних канальцях. Клітини Сертолі підтримують функціонування статевого апарату чоловіки. Вони є частиною гематологічного бар'єру між організмом і гаметамі.
Клітини Сертолі активно виділяють АМГ з моменту формування тестикул у плоду чоловічої статі. Вже на 8-10 тижні цей інгібуючий фактор виконує одну зі своїх основних біологічних ролей — провокує регресію протоки попередника-матки. Це сприяє правильному формуванню чоловічих внутрішніх і зовнішніх статевих органів.
Антимюллерів гормон залишається високим до моменту народження дитини і в ранньому дитинстві. З пубертатного періоду концентрація речовини починає досить різко знижуватися. Мінімальні значення досягаються показником у людей старше 40 років.
Якщо через генетичних особливостей у плоду чоловічої статі не виробляється повноцінний Антимюллерів проток або порушено його сприйняття тканинами на рівні рецепторів, то розвивається синдром персистенції. Анатомічно чоловіки з цією патологією відрізняються збереженням частини ембріонального протоки-попередника матки і труб. У дорослому віці пацієнти мають явища крипторхізму, безпліддя. У них досить часто формуються пахові грижі.
Синдром персистенції Мюллерова проток є однією з форм чоловічого помилкового гермафродитизму. Диференціація тестикулярной тканини у чоловіків з цим синдромом в нормі. Порушення репродуктивної здатності може бути викликано тривалим крипторхізм. Якщо потрібну операцію провели пізно, то ризик атрофії насіннєвихканальців високий. Це в свою чергу веде до нестачі синтезу тестостерону та інших андрогенів.
Фізіологія гормону у жінок
у нормі АМГ в невеликих кількостях виділяється у плодів жіночої статі з 32 36 тижні вагітності. У дитячому і підлітковому віці рівень антімюллерова гормону поступово зростає. Найбільша концентрація фіксується у віці від 20 до 30 років. Далі секреція гормону трохи падає і зберігається на стабільному рівні до моменту виснаження яєчників (через вікову менопаузи або з інших причин).
Антимюллерів гормон виробляється клітинами гранульози. Ця частина зростаючих фолікулів володіє власною ендокринної секрецією.
гранулезе виділяє АМГ тільки в преантральной і антральной стадії росту фолікула. Коли горбок з яйцеклітиною досягає розміру 8 мм Антимюллерів гормон перестає секретироваться, зате зростає продукція естрогенів. Вважається, що АМГ захищає тканину гранулези від надлишкової стимуляції гонадотропіном (ФСГ).
Протягом менструального циклу рівень антімюллерова гормону в нормі залишається стабільним. Невеликі коливання концентрації цього інгібітора пов'язані з овуляцією. Пік АМГ фіксують за 4 дні до виходу зрілої яйцеклітини. Найменші значення виявляють на 3-4 день після овуляції.
АМГ як маркер жіночого здоров'я
Концентрація АМГ відображає у жінки резерви і активність репродуктивної системи.
Гормон є маркером:
- овариального резерву,
- овариального старіння,
- оваріальної відповіді в нормі,
- овариальной дисфункції.
Низький Антимюллерів гормон у жінок репродуктивного віку говорить про виснаження яєчників, безплідді яичникового генезу, початку пременопаузальних змін.
Високий АМГ спостерігається при синдромі полікістозних яєчників. Значне підвищення показника буває при пухлинах з клітин гранульози.
Коли здають АМГ?
Здавати Антимюллерів гормон в педіатричній практиці рекомендують при уповільненому або передчасному статевому розвитку. Крім того, цей аналіз може бути призначений новонародженому для встановлення статі в сумнівних випадках (гермафродитизм).
Чоловікам андрологи і урологи рекомендують здавати АМГ для оцінки чоловічої статевої функції, при лікуванні з приводу безпліддя, при діагностиці крипторхізму і анорхізму.
Жінкам необхідно здати цей аналіз при безплідді, в менопаузу. Крім того, при контролі лікування раку яєчників іноді потрібно дослідження АМГ. Гормон можна здавати в будь-який день репродуктивного циклу.
Планування ЕКО в ряді випадків також вимагає діагностики рівня антімюллерова гормону. Це дослідження включено в протоколи в рамках розширеного EFORT-тесту.
Норма АМГ залежить від віку і статі. У дорослих чоловіків гормон в середньому знаходиться на рівні 4,2 ± 0,6 нг / мл. У хлопчиків АМГ в нормі дорівнює 47-65 нг / мл. У підлітковому періоді показник швидко знижується до 6-7 нг / мл.
У жінок середина норми для АМГ в дитинстві 3,5 ± 1,8 нг / мл. У репродуктивному періоді рівень гормону вище і досягає 2,1-7,3 нг / мл. Падіння концентрації АМГ до 1,1-0,8 нг / мл говорить про зниження оваріального резерву.
Симптоми надлишку естрогенів
Статеві гормони беруть участь у формуванні первинних і вторинних репродуктивних ознак, підтримують функціональну активність яєчників і яєчок, нормальне сексуальне поведінку.
Жіночі статеві гормони — це естрогени з різним ступенем активності. До цієї групи біологічно активних речовин відносять естріол, естрон, естрадіол.
За хімічною будовою ці гормони відносяться до групи стероїдів. Їх попередниками є тестостерон і андростендіон. Гормони утворюються з цих речовин під впливом ферменту ароматази.
Найсильніший естроген — естрадіол. Його високі концентрації виявляються у жінок дітородного віку. Активність естрону і естріолу значно нижче.
Статеві стероїди секретируются в основному фолікулярним апаратом яєчників. У вагітних певну кількість гормонів виділяє в кров плацента. Невелика кількість неактивних статевих стероїдів виробляється корою наднирників. У чоловіків ці речовини виробляються тестикулярной тканиною.
Функції статевих стероїдів у жінок
жіночі стероїди впливають на органи-мішені через рецепторний апарат.
Чутливість до гормонів виявляють клітини:
- матки,
- піхви,
- уретри,
- молочної залози,
- печінки,
- гіпофіза,
- гіпоталамуса.
Рецептори в цих тканинах утворюють з естрогенами стійкий комплекс. Його поява передає внутрішньоклітинним структурам певний імпульс. Під дією естрогенів посилюється синтез білків, факторів росту, цитокінів.
У гіпофізі і гіпоталамусі гормони надають регулюючу дію на вироблення рилізинг-факторів і гонадотропінів (за принципом зворотного зв'язку).
Статеві стероїди чинять на організм фемінізірующее вплив.
Ефекти гормонів:
- розвиток внутрішніх статевих органів (матки і маткових труб),
- підтримка регулярного менструального циклу,
- розвиток зовнішніх статевих органів (піхви),
- формування молочної залози,
- формування вторинних статевих ознак за жіночим типом,
- зниження атерогенних властивостей крові,
- зменшення резорбції кісткової тканини,
- підвищення коагуляції крові.
Нормальні значення жіночих стероїдів крові
Рівень естрогенів в крові в нормі залежить від статі і віку. У хлопчиків і чоловіків цих гормонів мінімальна кількість. У дівчаток до пубертату естрогенів виділяється помірна кількість. У жінок репродуктивного віку рівень естрогенів дуже високий.
Якщо жінка не вагітна, то концентрація гормонів змінюється протягом менструального циклу. У початковий період першої фази рівень естрогенів повільно наростає. Максимум за цим показником спостерігається перед овуляцією. Після виходу дозрілої яйцеклітини естрогени крові знижуються. У другу фазу фіксується невеликий підйом концентрації гормонів на 4-7 день після овуляції. Далі настає спад, який зберігається до початку менструації.
у вагітної жінки статеві стероїди в крові вище середніх значень. Підвищення рівня біологічно активних речовин починається з перших тижнів після зачаття. З моменту включення ендокринної активності плаценти (другий триместр) і до початку пологів концентрація естрогену прогресивно зростає.
Після появи дитини на світ у жінки швидко знижується рівень статевих гормонів крові. Естрогени наближаються до початкових значень вже на 3-5 день після пологів.
Після 30-35 років у жінок спостерігається поступове зниження гормональної функції яєчників. Статеві стероїди виробляються в менших кількостях. Після менопаузи жіночих статевих гормонів стає порівняно мало. В яєчниках синтез стероїдів блокується, а кора наднирників виробляє тільки малоактивний естрон.
У чоловіків і жінок рівень естрогенів приблизно однаковий.
Симптоми надлишку жіночих стероїдів
Якщо в організмі виробляється надмірна кількість жіночих статевих гормонів, то клінічні прояви залежать від концентрації естрогенів, віку і статі пацієнта.
У дітей така патологія призводить до раннього статевого розвитку. У дівчаток воно протікає по ізосексуальним типу. Формуються вторинні статеві ознаки, молочні залози, починаються менструації. У хлопчиків відзначається набухання грудних залоз, перерозподіл жирової тканини.
У чоловіків надлишок естрогенів є причиною фемінізації.
Хворих турбує:
- зменшення потенції,
- імпотенція,
- безпліддя,
- уповільнення росту волосся на обличчі,
- зменшення м'язової сили,
- підвищення маси тіла.
У жінок репродуктивного віку надлишок естрогенів тривалий час непомітний.
Перші симптоми гіперестрогенії:
- біль в молочних залозах перед менструацією,
- тривалі менструації,
- рясна кровотеча в менструації,
- маткові кровотечі,
- нервозність і лабільність настрою.
згодом надлишок жіночих статевих гормонів призводить до мастопатії, гіперплазії ендометрію, онкологічних захворювань репродуктивних органів.
Причини гіперестрогенії
Симптоми надлишку естрогенів з'являються з різних причин.
Найбільш небезпечні стану:
- злоякісні і доброякісні пухлини яєчників,
- гіпертекоз,
- патологія надниркових залоз,
- кіста яєчників,
- аденома гіпофіза.
Крім того, підвищення статевих стероїдів в крові фіксується при гіпотиреозі, полікістоз яєчників, депресії, захворюваннях печінки і органів шлунково-кишкового тракту .
До модифікується факторів, що підвищують жіночі стероїди крові, відносять:
- куріння,
- ожиріння,
- алкоголізм,
- гіподинамію,
- нестача вітамінів і мікроелементів.
гормон естрадіол
Статеві гормони відповідають за формування характерних ознак чоловічої і жіночої організмів. Джерелом цих речовин є гонади (яєчка або яєчники) і наднирники. У жінок виробляються переважно естрогени, а у чоловіків — андрогени. Ці гормони близькі за хімічною будовою, але їх дія діаметрально противоположенное.
Жіночі гормони
Естроген у людини представлені трьома гормонами: естрадіолу, естрону, естріолом. Високу біологічну активність демонструє перший з них. Естрон і естріол — другорядні естрогени. На перший план вони виходять тільки в період після згасання функціональної діяльності яєчників (після клімаксу).
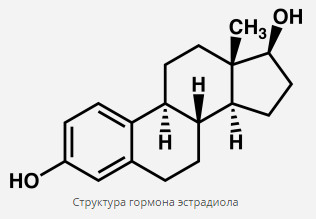
Синтез естрадіолу
Гормон утворюється в гранулезной тканини фолікулярного апарату яєчників. Він синтезується шляхом складної ферментативної реакції з андрогену-попередника (тестостерону).
У дорослих жінок до настання вагітності на рівень естрадіолу крові впливають гонадотропіни (фоллікулотропін і лютеотропін). Ці стимулюючі фактори виробляються в гіпофізі за принципом зворотного зв'язку.
У першу фазу менструального циклу гонадотропіни сприяють підвищенню синтезу естрадіолу в яєчниках. Концентрація гормону стаємаксимальною до моменту виходу зрілої яйцеклітини з фолікула.
У другу фазу репродуктивного циклу рівень естрадіолу прогресивно падає. Мінімальні значення фіксуються в дні менструації.
Якщо вагітність настала, то синтез естрадіолу і інших естрогенів різко підвищується. Протягом всього терміну гестації концентрація цих гормонів в десятки разів вище середніх цифр. Рівень естрадіолу зростає від перших тижнів до початку родової діяльності.
Біологічна роль естрадіолу
Гормон естрадіол надає непрямий вплив на весь організм у вагітних і невагітних жінок. Найбільшому впливу піддаються органи-мішені.
Рецептори до естрадіолу знайдені:
- в матці,
- в фаллопієвих трубах,
- в яєчниках,
- в молочних залозах,
- в структурах вульви і піхви,
- в центральній нервовій системі,
- в печінці та ін.
Клітини цих органів реагують навіть на невеликі коливання концентрації естрадіолу.
Роль естрадіолу у вагітних:
- підготовка ендометрію до імплантації яйцеклітини,
- попередження самовільних абортів ,
- підвищення маточного кровотоку,
- попередження значної крововтрати під час пологів.
Роль естрадіолу у невагітних жінок:
- розвиток первинних і вторинних статевих ознак,
- регулярний менструальний цикл,
- сексуальний потяг,
- розподіл жирової тканини за жіночим типом,
- зниження атерогенних властивостей крові,
- підвищення мінеральної щільності кісток.
Естрадіол відповідає за затримку рідини в тканинах, підвищену згортання крові, зміни настрою. Надмірна або низький рівень гормону провокує різні порушення.
Норма естрадіолу крові
у жінок дітородного віку в нормі концентрація естрадіолу залежить від дня циклу. В першу (фолікулярну) фазу значення гормону укладаються в межі від 55 до 225 пг / мл. До овуляції концентрація естрадіолу наростає і становить від 125 до 475 пг / мл. До другої (лютеїнізуючого) фазу рівень гормону знову знижується до 75-225 пг / мл.
У вагітних норма естрадіолу залежить від терміну гестації. У перший триместр хороші показники гормону знаходяться в межах від 210 до 3120 пг / мл. У другому триместрі цільовий рівень естрадіолу укладається в проміжок від 2700 до 14000 пг / мл. В останні місяці перед пологами кордону нормальних значень за даним показником відповідають рівню від 10000 до 27000 пг / мл.
У жінок після менопаузи відзначається природне зниження концентрації естрадіолу в крові. Норма з аналізу залежить від віку жінки. Зазвичай цільовим значенням прийнято вважати естрадіол від 19,5 до 82 пг / мл.
Для чоловіків норма гормону змінюється з віком. Зазвичай у дорослих референсними значеннями вважають значення від 15 до 70 пг / мл.
Причини відхилень від норми
Естрадіол може бути підвищений з ряду функціональних або патологічних причин.
Основні чинники, що збільшують концентрацію гормону:
· естрогенсекретірующіе пухлини статевої системи,
· функціональна кіста яєчників,
· печінкова недостатність,
· хвороби щитовидної залози,
· ендометріоз,
· надлишкова маса тіла.
Рівень гормону в крові відповідає і на лікарські впливу. Концентрацію естрадіолу підвищують карбамазепін, кломифен, анаболічні стероїди, комбіновані протизаплідні таблетки і інші засоби.
Зниження естрадіолу нерідко спостерігається у жінок дітородного віку.
Причини зниження рівня гормону:
- куріння,
- незбалансована дієта,
- алкоголізм,
- емоційні стреси,
- різке зниження ваги,
- пролактінома,
- гипогонадизм гіпогонадотропний,
- затримці статевого розвитку.
З ліків концентрацію естрадіолу зменшують дексаметазон, октреотид, бусерелін, нандролон і інші.
Ознаки несприятливих змін
Про те, що рівень естрогену в крові знижений або надлишково високий можна здогадатися за певними симптомами. Якщо такі ознаки з'явилися, то необхідно звернутися за медичною допомогою і піти обстеження в ендокринолога та гінеколога.
Симптоми порушень:
- патологія плаценти за даними УЗД,
- загроза мимовільного аборту,
- гінекомастія у підлітків і дорослих,
- затримка статевого дозрівання,
- передчасний статевий розвиток,
- маткові кровотечі,
- підозра на пухлину матки або яєчників,
- остеопороз,
- важкий передменструальний синдром,
- важкий клімактеричний синдром,
- порушення регулярності циклу.
Симптоми нестачі естрогенів
Гормональний баланс жіночого організму знаходиться в стані динамічної рівноваги. Менструальний цикл складається з декількох фаз. Кожна з них характеризується різним рівнем біологічно активних речовин: гонадотропінів, естрогенів, гестагенів. Концентрація кожного гормону змінюється в залежності від впливу яєчників, жовтого тіла, гіпофіза і гіпоталамуса.
Естроген відносять до жіночих статевих стероїдів. Ці гормони у великій кількості виділяються в кров фолікулами яєчників, матково-плацентарних комплексом. Крім того, синтез естрогенів йде і в корі надниркових залоз, і в яєчку у чоловіків.
У людини в організмі виявляють три види жіночих статевих стероїдів:
- естрадіол,
- естріол,
- естрон.
Найбільш активним є естрадіол. Він активно взаємодіє з клітинами-мішенями. Фемінізірующее дію цього гормону надзвичайно високо. Естрадіол виділяється фолікулярним апаратом. На його синтез впливає ФСГ гіпофізу. Попередником естрогену є тестостерон.
Естріол і естрон грають у жінок дітородного віку допоміжну роль. Їх активність досить помірна. Але в постменопаузі саме естрон є основним естрогеном. Цей гормон утворюється в корі наднирника з слабкого андрогену андростендіону.
Дія естрогенів на організм
Естрадіол, естріол і естрон впливають на всі тканини і органи. Особливо чутливі до цих речовин матка, її придатки, піхву, молочна залоза, печінка, центральна нервова система.
У нормі естрогени забезпечують розвиток репродуктивної системи, становлення менструального циклу, регулярні менструації, формування молочної залози. Жіночі гормони впливають не тільки на статеву сферу. Вони також регулюють склад крові, процеси мінералізації кісткової тканини, баланс вегетативної нервової системи.
У жінки дітородного віку з нормальним рівнем естрогенів крові низький ризик розвитку атеросклерозу, а значить, і ішемічної хвороби, інсульту. Саме ці гормони є причиною мінімальної смертності від серцево-судинних захворювань серед представниць слабкої статі у віці до 55-65 років.
Коли можливий дефіцит естрогенів
Відносний і абсолютний дефіцит естрогенів виникає у жінок при зупинці або уповільнення синтезу статевих стероїдів в яєчниках. Фізіологічної причиною цього стану є менопауза. Вікове виснаження фолікулярного апарату яєчників і припинення овуляція заплановано генетично. В середньому остання менструація трапляється в житті жінки у віці 49-52 років. Якщо клімакс наступив дуже рано, то це може негативно позначитися на тривалості життя пацієнтки.
Причини ранньої менопаузи:
- хірургічна кастрація,
- фармакологічна кастрація,
- синдром виснаження яєчників,
- резекція яєчників з приводу синдрому полікістозу,
- аутоімунне ураження яєчників.
Недолік статевих гормонів може бути наслідком неправильної роботи гіпофіза і гіпоталамуса.
Крововилив в зоні центральних відділів ендокринної системи, пухлинний і інфекційний процес або ішемія приводять до розвитку вторинного гіпогонадизму. Цей стан характеризується вкрай низькою продукцією гонадотропінів. Без регулюючого і стимулюючого дії ФСГ і ЛГ в яєчниках перестають дозрівати яйцеклітини і вироблятися естрогени.
Тривалий прийом комбінованих оральних контрацептивів може спровокувати надмірне гальмування в гіпоталамо-гіпофізарної області.
Цей стан супроводжується:
- падінням синтезу гонадотропінів,
- зникненням їх нормальних ритмів секреції.
Функціональне падіння синтезу естрогенів буває при емоційних і фізичних стресах, важких захворюваннях, голодуванні, дефіциті вітамінів і мікроелементів. Гормональні причини гіпоестрогенії:
- гіперпролактинемії,
- вірільний синдром.
Симптоми захворювання
У тканинах людського організму надзвичайно багато рецепторів до статевих стероїдів. Відповідно і зниження їх рівня нижче критичного значення призводить до різноманітної симптоматикою. У кожної пацієнтки клінічна картина захворювання індивідуальна. Переважати і виходити на передній план можуть ті чи інші ознаки нестачі статевих гормонів.
У ранню стадію гіпоестрогенії у пацієнток спостерігаються вегето-судинні, нейроендокринні і психологічні симптоми. Пацієнтки скаржаться на пітливість, відчуття «спека» в тілі, «припливи», стомлюваність, дратівливість, пітливість, безсоння. У цей період у жінки підвищується ризик набрати зайву вагу і зіткнутися з порушеннями вуглеводного обміну.
При тривало існуючому нестачі естрогенів виявляються урологічні, сексуальні порушення, зміни шкіри. Пацієнтки відчувають дискомфорт при сечовипусканні, нетримання сечі, біль при статевому акті через сухість в піхві. Атрофія слизової сечостатевої системи може стати причиною постійного дискомфорту під час сексу. Ці зміни часто є причиною припинення статевого життя. Жінки скаржаться на зниження еластичності і тургору шкіри. На обличчі помітні характерні зміни: птоз м'яких тканин, зменшення чіткості овалу обличчя, сухість шкіри.
Надалі гіпоестрогенія провокує зниження мінеральної щільності кісток, розвиток атеросклерозу, судинної деменції. Пацієнтки звертаються за медичною допомогою через переломи, ішемії міокарда, порушення кровопостачання головного мозку, погіршення пам'яті.
У вагітних жінок недолік естрогенів може стати причиною спонтанного аборту. Загроза переривання вагітності з цієї причини зазвичай виникає в першому триместрі.
Безпліддя також може бути наслідком гіпоестрогенії. Причиною труднощів із зачаттям є або патологія яєчників, або гіпоталамо-гіпофізарної області. Жінці з низькими значеннями естрадіолу крові слід відвідати гінеколога і ендокринолога.
Соматотропний гормон (СТГ)
У головному мозку людини розташовується центральна ланка ендокринної системи — гіпоталамо-гіпофізарна область. Клітини цієї зони виробляють сигнальні речовини, які регулюють діяльність залоз внутрішньої секреції. Також їх гормони впливають на ріст і розвиток організму, обмін речовин, статева поведінка. До групи сигнальних речовин гіпофіза відносять Тропіних.
Тропні функції гіпофіза
Тропіних виробляються за принципом зворотного зв'язку. Ці речовини чутливі до невеликих змін обміну речовин або взаємозалежної залози внутрішньої секреції.
До Тропіних відносять 8 основних гормонів:
- тиреотропний (ТТГ),
- адренокортикотропний (АКТГ),
- фоллікулотропін (ФСГ),
- лютеотропін (ЛГ),
- пролактин,
- ліпотропних,
- меланоцітстімулірующій,
- соматотропний гормон (СТГ, гормон росту).
Будова і секреція гормону росту
СТГ виділяється в кров соматотрофов аденогипофиза. На ці клітини активно впливають біологічно активні речовини гіпоталамуса (соматостатин і соматолиберин). Гормон виділяється в кров імпульсами. Виразність піків більше в дитячому і молодому віці.
Максимальна амплітуда імпульсів фіксується в четверту фазу сну. Після 20 років концентрація СТГ в крові різко знижується. Крім того, пригнічує секрецію гормону росту і вуглеводна їжа.
Сприяють підвищенню концентрації СТГ:
- голодування,
- фізична праця,
- сон,
- падіння рівня цукру крові,
- білкова дієта.
За будовою соматотропний гормон входить в сімейство пептидних. Найбільш близьку до нього хімічну структуру мають пролактин і один з гормонів вагітності (плацентарний лактоген). Основна форма СТГ має в своєму складі 191 амінокислоту. Молекулярна маса цього з'єднання 22124 Так. Гени, що кодують синтез гормону росту, виявлені на 17 хромосомі.
Соматотропний гормон в нормі у чоловіків — до 2 нг / мл, у жінок — до 10 нг / мл.
Ефекти гормону росту
СТГ є основним біологічно активною речовиною, що відповідає за ріст організму. У дорослому віці гормон росту підтримує обмін речовин і функції центральної нервової системи.
Ефекти СТГ:
- стимуляція зростання тіла в довжину (якщо не закриті зони росту),
- підвищення синтезу білків,
- зменшує виведення натрію і калію,
- посилює всмоктування кальцію в кишечнику,
- збільшує утворення глюкози крові,
- сприяє розщепленню ліпідів жирової тканини,
- підсилює потовиділення,
- активізує Т-клітинний імунітет.
Якщо рівень СТГ крові значно вище норми, то всі впливу гормону на тканини стають надмірними. У пацієнта порушується обмін речовин. Соматотропний гормон підвищується при акромегалії (гігантизм), яка найчастіше буває наслідком аденоми гіпофіза.
Вплив СТГ на інші гормони
Гормон росту здійснює свою дію за підтримки інших біологічно активних речовин. Анаболічні ефекти СТГ реалізуються тільки при нормальному рівні інсуліну. Якщо цього гормону мало, то порушується і синтез білка, і лінійний ріст.
Липолиз (руйнування ліпідів жирової тканини) СТГ проводить за підтримки статевих і тиреоїдних гормонів. Крім того, вони необхідні і для анаболічних ефектів соматотропіну.
Противоположение СТГ дію мають гормони кори надниркових залоз. Глюкокортикоїди сприяють зменшенню синтезу білка, підвищують масу тіла, гальмують лінійний ріст тіла.
Патологічні стану
І надмірний, і недостатній синтез гормону росту призводить до серйозних захворювань. Якщо СТГ виділяється занадто мало, то розвивається . Цей стан пов'язують з несприятливою генетикою.
гіпофізарний нанізм діагностують у дітей молодшого віку. Якщо вчасно почати лікування синтетичними аналогами гормону росту, то недостатнє зростання тіла в довжину до дорослого віку можна повністю скорегувати.
У дорослих недолік СТГ проявляється надлишковим жировідкладенням, слабкістю, апатією. Цей стан рідко діагностується і лікується.
Надмірне виділення соматотропного гормону призводить до появи акромегалії і гігантизму. У дітей спостерігається надлишковий ріст в довжину, у дорослих — характерні зміни зовнішності. Акромегалія супроводжується порушеннями жирового, вуглеводного, білкового, водного обміну. Ця хвороба часто ускладнюється серцево-судинними патологіями.
Лікування акромегалії починають з консервативних заходів. Пацієнту призначають синтетичний соматостатин для підготовки до радикального лікування. Далі виконується хірургічна операція або променева терапія. У відновний період і пізніше пацієнт повинен регулярно здавати аналіз на СТГ і ИРФ-1. Якщо ремісія неповна, то в післяопераційному періоді продовжують медикаментозне лікування. Соматостатін рекомендують на тривалий період часу (півроку-рік). Цей препарат має кілька форм випуску. Найбільш зручний для пацієнта — соматостатин для ін'єкцій один раз в 3-4 тижні. Цей препарат має досить високу ціну. На даний момент соматостатин включений в список пільгових лікарських засобів.
Торгові назви препаратів соматостатину:
- стіламін,
- Соматулін,
- Сандостатин Лар (соматостатин з тривалою тривалістю дії),
- Сандостатин (соматостатин з тривалою тривалістю дії),
- Октреотид (соматостатин з тривалою тривалістю дії),
- Модустатін.
Препарати цієї групи використовуються не тільки для лікування акромегалії. Соматостатін потрібен і при панкреатитах, і при гострих кровотечах з судин травного тракту.
антидіуретичний гормон
Баланс рідини і електролітів в організмі людини підтримується декількома механізмами. Один з регулюючих факторів — антидіуретичний гормон (АДГ, вазопресин) гіпоталамуса. Це біологічно активна речовина впливає на нирки, гладку мускулатуру судин і органів, центральну нервову систему.
Структура гормону
АДГ є пептидом за хімічною структурою. У його складі міститься дев'ять залишків амінокислот.
Амінокислоти гормону:
- цистеїн (1 і 6 в ланцюзі),
- тирозин,
- фенілаланін,
- глутамин,
- аспарагин,
- пролин,
- аргінін,
- гліцин.
Молекулярна маса становить близько 1100 Д.
Синтез і секреція
Вазопрессин виробляється з амінокислот в клітинах гіпоталамуса. У нейронах цієї частини головного мозку секретується попередник прогормона. Далі ця хімічна сполука надходить в клітинний апарат Гольджі і модифікується в прогормон. У цьому виді майбутній АДГ з'єднується з нейросекреторну гранулами і транспортується в задню частку гіпофіза. Під час перенесення з гіпоталамуса вазопресин розщеплюється на зрілий гормон і нейрофізін (транспортний білок).
Обидві речовини депонуються в кінцевих розширеннях аксонів в задньої долі гіпофіза. Саме звідти гормон вивільняється в кров при певних стимулах.
Стимуляція секреції
Антидіуретичний гормон реагує на зміну електролітного складу крові.
Стимули секреції вазопресину:
- збільшення рівня натрію в крові,
- підвищення осмотичного тиску позаклітинної рідини.
Синтез і секреція гормону посилюються під дією сигналів від двох типів рецепторів. Перші з них — осморецептори гіпоталамуса. Вони реагують на співвідношення концентрації солей і води в крові. Якщо цей параметр змінюється хоча б на 0,5-1%, то виділення АДГ істотно наростає. Другі — барорецептори передсердь. Вони оцінюють рівень кров'яного тиску. Якщо тиск падає, то синтез і секреція вазопресину ростуть.
У нормі виділення гормону в кров підвищується після:
- рясного потовиділення,
- фізичного навантаження,
- прийому солоної їжі,
- обмеження рідини в раціоні,
- зміни положення тіла (при вставанні).
у вазопресину є певні добові ритми. Гормон більше виробляється і виділяється в нічні години. Особливо добре ця закономірність простежується в положенні лежачи.
Добовий ритм виробництва АДГ формується з віком. У дітей до року не спостерігається суттєвого підвищення концентрації гормону в крові вночі. Далі формується нічний пік секреції. Якщо механізми дорослішання запізнюються, то у дитини може бути діагностований енурез.
Рецептори до АДГ
Антидіуретичний гормон сприймають клітини нирок, гладких м'язових волокон і нейрони. Є два види чутливих до цієї речовини компонентів мембран.
Виділяють:
- рецептори V1,
- рецептори V2.
Затримка води в організмі під дією АДГ відбувається за рахунок рецепторів V2, а підвищення тонусу судин — за рахунок рецепторів V1.
Гени рецепторів АДГ клоновані, ген рецептора типу V2 локалізується на X-хромосомі.
V1 структури знаходять в клітинах гладеньких м'язів судин, печінки, головному мозку. Спорідненість до них вазопресину досить низька. Ефект гормону фіксується тільки при його високих концентраціях.
V2 структури розташовані в нирках. Вони відповідають за основну дію АДГ. Рецептори виявляють на мембранах клітин дистальних канальців і збірних трубочок. Навіть низькі концентрації вазопресину в крові впливають на рецептори.
Генетика гормону і рецепторів
Вазопрессин закодований в гені двадцятої хромосоми (20p13). Він несе інформацію про прогормон і його попередника. Ген має складну структуру: три екзона і два інтрони.
Гени рецепторів до вазопресину клоновані. Доведено, що рецептор типу V2 знаходиться на десятій хромосомі.
Дія АДГ
Вазопрессин надає кілька ефектів. Його основне біологічне дію — антидиуретическое. Якщо АДГ не синтезується, то нирки перестають концентрувати сечу. Її щільність стає такою ж низькою, як у плазми крові. За добу сечі може утворюватися до 20 літрів.
Якщо антидіуретичний гормон присутній в плазмі крові, то він зв'язується з рецепторами в нирках (типу V2). Ця реакція стимулює аденілатциклазу і протеїн А. Потім відбувається експресія гена білка аквапорінов-2. Ця речовина вбудовується в мембрану ниркових канальців і утворює канали для води.
В результаті спостерігається зворотне захоплення води з канальців. Сеча стає більш концентрованою, а її обсяг зменшується.
У плазмі навпаки зменшується осмолярність. Обсяг циркулюючої крові і тканинної рідини зростає.
Інші ефекти АДГ:
- стимуляція синтезу глікогену в печінці,
- підвищення тонусу гладком'язових волокон,
- судинозвужувальний ефект,
- скорочення мезангліальних клітин,
- регуляція агрегації тромбоцитів,
- регуляція виділення адренокортикотропіну, пролактину ендорфінів.
до сих пір до кінця не вивчено вплив вазопресину на центральну нервову систему. Вважається, що гормон частково відповідає за поведінкові реакції (агресію, прихильність до потомству, статева поведінка). АДГ може бути причиною депресії та інших психіатричних захворювань.
Порушення синтезу і секреції АДГ
Недолік синтезу вазопресину або чутливості до нього (рецепторів типу V2) є причиною .
Це захворювання буває двох видів:
- центральна форма,
- ниркова форма.
У пацієнтів з нецукровий діабет розвивається рясний діурез. Обсяг сечі за добу істотно вище норми (1-2 літрів). Скарги пацієнтів пов'язані з зневодненням (гіпотонія, сухість шкіри і слизових, слабкість).
Неадекватна секреція гормону відбувається при іншому захворюванні — синдромі Пархона. Ця рідкісна хвороба має важку клінічну картину: судоми, відсутність апетиту, нудоту, втрату свідомості.
Недостатнє виділення в кров вазопресину ночами спостерігається в дитячому віці. Якщо така ситуація зберігається після 4 років, то можливий розвиток енурезу.
Норма АДГ
Нормальні значення вазопресину залежать від рівня осмолярності плазми. При осмолярності 275-290 мосм / л АДГ повинен бути від 1,5 нг / л до 5 нг / л. Для точної діагностики нецукрового діабету та синдрому Пархона рекомендуються навантажувальні проби.
ГЗСС (секс-стероїд-зв'язуючий глобулін)
Більшість активних хімічних речовин переноситься в крові у зв'язаному вигляді. Це забезпечує їх дію тільки на орган-мішень, а не на весь організм.
Статеві гормони (андрогени і естрогени) транспортуються по судинах саме в такому невільному вигляді.
їх переносить особливий глобулін, що виробляється печінкою. Назва цієї речовини — глобулін, що зв'язує статеві гормони.
Також цей білок називають:
- секс-стероїд-зв'язуючий глобулін,
- тестостерон-естрадіол-зв'язуючий глобулін,
- Sex Hormone Binding Globulin.
Він може приєднуватися до тестостерону, дигидротестостерону, естрадіолу, прогестерону, андростендіон.
Глобулін має більш високу спорідненість до андрогенів. Це означає, що при наявності в крові і естрадіолу, і тестостерону, ГЗСС приєднається до останнього.
Рівень ГЗСС
Концентрація в крові глобуліну залежить від багатьох факторів.
Найбільше значення мають:
- вік пацієнта,
- підлогу,
- рівень андрогенів і естрогенів,
- стан печінки,
- функція щитовидної залози,
- функція надниркових залоз,
- наявність ожиріння,
- лікування андрогенами.
Чим вище рівень ГЗСГ, тим менш доступні тканин статеві стероїди.
Зазвичай з глобуліном пов'язано близько половини всіх андрогенів і естрогенів. Решта статевістероїди слабо пов'язані з іншим білком крові (альбуміном). Діють на клітини органів-мішеней тільки 1-2% андрогенів або естрогенів.
Якщо ГЗСГ вище норми, то є ймовірність того, що вільного тестостерону менше, ніж демонструє тест на вільний тестостерон. У зворотному випадку, при зниженій концентрації глобуліну, є ймовірність надмірного рівня активного тестостерону досить висока.
Норма ГЗСГ:
- для чоловіків 13-71 нмоль / л,
- для жінок 7,2-100 нмоль / л.
Концентрація глобуліну залежить від статі і віку. У дітей значення цього показника можуть бути значно вище 100 нмоль / л. У жінок після клімаксу рівень ГЗСГ поступово падає. У чоловіків цей показник з роками, навпаки, збільшується.
Після 60 років значення концентрації зростає на 1-1,5% на рік. Це відображає швидку порею біологічно активного тестостерону на тлі відносно збереження загальної кількості андрогенів.
Чим вище ГЗСС у літньої людини, тим менше у нього ризики серцево-судинних катастроф (інфаркту міокарда, інсульту, тромбозу).
Як визначають концентрацію глобуліну
Аналіз на ГЗСГ виконується в лабораторіях за допомогою імунохемілюмінесцентного методу. Для оцінки цього параметра спочатку забирають у пацієнта 10 мл венозної крові. Щоб правильно підготуватися до такого дослідження, необхідно протягом 30-60 хвилин відпочити від фізичних та емоційних навантажень, утриматися від куріння.
Коли призначають такий аналіз
Аналіз ГЗСГ в основному використовується андрологами і репродуктологами . Крім того, його можуть призначити ендокринологи, урологи, гінекологи.
Показання для визначення ГЗСГ визначаються клінічною ситуацією. Необхідність в цьому аналізі є тільки у невеликого відсотка пацієнтів. Обстеження на ГЗСГ варто виконувати тільки за рекомендацією лікаря.
Аналіз призначають:
- для оцінки рівня андрогенів,
- при безплідді,
- при імпотенції у чоловіків,
- при зниженні сексуального потягу,
- для діагностики полікістозу яєчників у жінок,
- для визначення балансу репродуктивної системи (спільно з гонадотропінами, андрогенами, естрогенами),
- для обчислення індексу вільних андрогенів,
- для оцінки ризику розвитку гестозу у вагітної.
Дослідження рівня глобуліну доцільно виконувати при підозрі на низький рівень андрогенів у чоловіків, і високий рівень — у жінок. Особливо важливо оцінити цей показник за наявності симптомів патології і нормальних значеннях вільного тестостерону крові.
Найбільш поширені клінічні ситуації, що вимагають призначення ГЗСГ:
- гірсутизм у дівчат і жінок (надлишковий ріст волосся на обличчі й тілі),
- погіршення ерекції у чоловіків.
Патологічні результати аналізу
ГЗСГ може бути як вище норми, так і нижче. Досить часто такі зміни свідчать лише про функціональні порушення і індивідуальні особливості.
Але у ряду пацієнтів патологічні значення концентрації глобуліну є ознакою серйозного захворювання.
Про що може говорити зниження ГЗСС?
Знижені значення зустрічаються при:
- нефротичному синдромі (виражена втрата білка з сечею),
- коллагенозах,
- синдромі полікістозних яєчників ,
- гіперандрогенії,
- гірсутизмі,
- акне,
- резистентності до інсуліну,
- цукровому діабеті 2 типу ,
- зниженні функції щитовидної залози,
- акромегалії,
- хвороби Іценко — Кушинга,
- пролактинома,
- ,
- ураженні печінки (цироз),
- лікуванні андрогенами, глюкостероідамі, соматостатином.
Коли діагностується підвищений ГЗСГ?
Високий показник знаходять:
- при гіперестрогенії,
- спадковості,
- тиреотоксикозі,
- гепатиті (в тому числі і вірусному),
- ВІЛ-інфекції,
- лікуванні комбінованими оральними контрацептивами, фенітоїном.
Якщо виявлений такий патологічний результат (зниження або підвищення), то необхідно проконсультуватися з лікарем. Тільки ендокринолог, андролог або гінеколог можуть дати рекомендації по корекції ГЗСГ.
Досить часто потрібне лікування основного захворювання (патології щитовидної залози, надниркових залоз, гіпофіза, печінки).
В інших випадках може знадобиться терапія дефіциту або надлишку андрогенів (навіть при нормальному рівні вільного тестостерону).
У жінок часто потрібна корекція гіпоестрогенії, тобто нестачі жіночих статевих гормонів.
гормон сну
Все біологічні процеси в клітинах живих організмів підкоряються певним ритмам. Чергування сну і неспання регулює ряд циркадних механізмів.
У епіфізі () виділяється активна хімічна речовина мелатонін. Концентрація цього з'єднання зростає з настанням темного часу доби. Гормон сну сприяє процесам гальмування в центральній нервовій системі.
Структура хімічної сполуки
Мелатонін є похідним від амінокислоти триптофану. Його хімічна формула: N-ацетил-5-метоксітріптамін. По суті гормон сну — це одна з модифікацій нейромедіатора серотоніна. Це індольне речовина утворюється під дією ферментів в нічні години.
У мелатоніну відносно низька молекулярна маса — всього 232 Д. Завдяки цьому речовина легко проникає через бар'єри між тканинами і кров'ю.
У гормону сну короткий період напіврозпаду (45 хвилин).
Синтез і ритм секреції
Мелатонін утворюється в основних клітинах епіфіза (пінеалоцітов). Звідти він потрапляє в кровообіг і спинномозкову рідину. Потім більша частина гормону сну накопичується в гіпоталамусі.
Вироблення мелатоніна змінюється в різний час доби. Епіфіз реагує на освітленість навколишнього простору. У природних умовах пік виділення в кров гормону доводиться на другій годині ночі. Максимальні значення за добу фіксуються з півночі і до п'ятої ранку.
Робота пінеалоцітов залежить від місцевого сонячного часу. Це означає, що на переведення стрілок годинника по декретною законам (зимовий, літній час) синтез мелатоніну не реагує. Зате при переїзді з однієї держави в іншу при зміні часових поясів спостерігається синхронне зміщення піку секреції гормону сну.
За добу у дорослих в кров виділяється близько 30 мкг цієї речовини. Причому концентрація гормону в 30 разів вище з півночі до світанку, ніж в інші години.
Метаболізм
Гормон сну транспортується в крові у зв'язаному вигляді. Його переносить сироватковий білок альбумін.
Вільний мелатонін з'єднується з чутливим структурами клітин-мішеней. Рецептори до цієї речовини є двох видів (мембранні та ядерні).
Мембранні рецептори у людини представлені двома типами (МТ1 і МТ2).
Перший з них зустрічається в гіпофізі, гіпоталамусі і периферичних тканинах. Другий — в інших ділянках мозку, в легенях і сітківці ока.
При приєднанні до рецептора відбувається реакція придушення циклічної аденілатциклази. Взаємодія відбувається через систему G-білків.
Ядерні рецептори до гормону сну виявлені відносно недавно. За будовою їх відносять до підродини ретіноідной RZR / ROR.
Мелатонін руйнується в печінці через реакцію гідролізу. Продукти його розпаду виводяться з організму з сечею. Основний метаболіт — 6-гідроксімелатонін-сульфат. Концентрація цієї речовини в сечі є непрямим показником кількості мелатоніну крові.
Біологічна роль мелатоніну
Мелатонін сприяє настанню і підтримці сну. Механізм цієї дії гормону до кінця не вивчений. Існує кілька теорій, що пояснюють роботу активної речовини. Вважається, що він гальмує процеси в центральній нервовій системі, зменшує синтез інших гормонів, впливає на клітинному рівні на нейрони.
Гормон збільшує тривалість і глибину сну. Мелатонін регулює природну структуру сну по фазах. Він сприяє нормальному засипанню.
У мелатоніну є ще безліч важливих функцій. Так, ця речовина є антагоністом меланостимулирующего гормону. Він викликає освітлення шкірних покривів, підвищення чутливості сітківки ока до сонячного світла.
Інші функції цієї речовини:
- пригнічує гонадотропіни та раннє статеве дозрівання,
- знижує кров'яний тиск,
- знижує частоту серцевих скорочень і витрати кисню в міокарді,
- зменшує синтез гормонів тропів,
- покращує чутливість до гормону росту,
- зменшує кількість вільних радикалів,
- уповільнює процеси старіння,
- підвищує імунітет,
- зменшує в'язкість крові,
- має протипухлинну дію,
- допомагає адаптуватися до змін навколишнього середовища,
- зменшує стреси і депресивні стани,
- нормалізує обмін жирів і вуглеводів,
- знижує надлишкову масу тіла,
- покращує травлення (секрецію ферментів і моторику).
Недостатня секреція
Недолік мелатоніну призводить до розвитку ряду хворобливих станів.
Прямий і непрямий наслідок нестачі цієї речовини:
- безсоння,
- розлади сну (засинання, структури),
- зниження пам'яті та інтелекту,
- розлади харчової поведінки,
- ожиріння,
- цукровий діабет 2 типу,
- артеріальна гіпертонія,
- ішемічна хвороба серця,
- атеросклероз судин головного мозку та ін.,
- раннє старіння організму,
- передчасна менопауза,
- тромбози,
- онкологічні захворювання (в тому числі, в молочної та передміхурової залозах ),
- інфекційні захворювання,
- депресія і інші розлади психіки.
Недолік мелатоніну найчастіше розвивається через порушення режиму сну і неспання. Відомо, що гормон сну синтезується в епіфізі з серотоніну в темний час доби. Сигнал про те, що настала ніч, пінеалоціти отримують від чутливих до світла клітин сітківки.
Якщо людина не спить вночі при електричному світлі, то синтез мелатоніну різко знижується. Зазвичай на час від опівночі до п'ятої ранку доводиться до 70% всього виробництва речовини за добу. При порушенні режиму дня цей показник падає нижче 50%.
Інші причини порушення синтезу мелатоніну:
- недолік триптофану в раціоні харчування,
- ушкодження шишкоподібної залози об'ємним утворенням ,
- руйнування клітин епіфіза вірусами, бактеріями або паразитами,
- крововилив в тканину шишкоподібної залози.
Існує спадкова схильність до нестачі гормону сну. У пацієнтів з таким дефектом спостерігається хронічне порушення засинання, структури сну по фазах.
тироксин
Щитовидна залоза відповідає за швидкість обмінних процесів в організмі, тонус серцево-судинної і нервової систем. Біологічно активні речовини в тиреоцитах утворюються з використанням молекул йоду. Основні — це тироксин (Т4) і трийодтиронін (Т3).
Структура тироксину
Тироксин — похідне від амінокислоти тирозину. Гормон містить в своєму складі чотири атома йоду. Йод в щитовидну залозу надходить з кров'ю. З'єднання цього мікроелемента надзвичайно важливі в раціоні людини. Недолік йодидів у їжі і воді може провокувати ендемічні захворювання (в першу чергу, дифузний і вузловий зоб).
Молекулярна маса тироксину — 777 Д. Приблизно 83% ваги доводиться на атоми йоду. Хімічна формула Т4: 3,5,3,5-тетрайодтіронін.
Синтез гормону проходить в фолікулах щитоподібної залози. Гормон Т4 утворюється у складі білка тиреоглобуліну. Спочатку до тирозину приєднується два атома йоду. Потім з'єднуються два залишку молекул отриманого дііодтірозіна. Від з'єднання відщеплюється аланин.
Далі всередині клітин здійснюється протеоліз даного білка і вивільнення тироксину в кров.
Період напіврозпаду у тироксину досить високий і дорівнює 6-7 дням.
Синтез і секреція
Тироксин є слабким тиреоїдних гормоном. Основна активність щитовидної залози реалізується за рахунок трийодтиронина. Ця речовина утворюється з Т4 в тиреоцитах і в периферичних тканинах (печінці та інших).
Перетворення тироксину в активну форму відбувається за допомогою металлоферментов монодейодази селен-залежної.
У щитовидній залозі утворюється і виділяється в кров переважно гормон Т4. На його частку в нормі припадає 70-80% від загальної кількості біологічно активних речовин.
Тироксин має властивість накопичуватися в тканини щитовидної залози. Далі він у міру необхідності виділяється в кров. Транспорт гормону здійснюється в пов'язаному вигляді. Тільки невелика частина циркулює у вільній формі.
Білки переносники тироксину:
- транстиретин,
- сироватковий альбумін,
- тироксинзв'язуючого глобулін.
Комплекс гормон-глобулін є найбільш стійким з'єднанням.
Вільні форми тироксину постійно виявляються в крові. Їх концентрація залежить від потреби тканин, рівня тиреотропіну і активності щитовидної залози.
Вільний Т4 може проникати через мембрани клітин і надавати свою біологічну дію.
Синтез тиреоїдних гормонів в щитовидній залозі підпорядкований регулюючим впливам гіпофіза і гіпоталамуса.
У центральних ланках ендокринної системи виділяються:
- тиреоліберином гіпоталамуса,
- тіреостатін гіпоталамуса,
- тиреотропин гіпофіза.
У нормі ендокринна система взаємодіє за принципом зворотного зв'язку. Чим більше в крові тироксину, тим менше виділяється стимулюючих факторів (тиреотропіну, тиреоліберином). Навпаки, якщо гормон Т4 синтезується в недостатніх кількостях, то рівень цих речовин зростає.
Біологічна дія
Для тироксину немає власних клітин-мішеней. Він впливає на всі тканини. Ця речовина здатна проникати через мембрану і з'єднується з рецепторами в кожної клітини організму.
Відомо, що спорідненість тиреоїдних рецепторів вище до трийодтироніну. Тому тільки 10% всіх ефектів щитовидної залози реалізується Т4.
Тироксин гормон вважається стимулятором метаболізму для багатьох тканин. Гормон приєднується до ядра клітини і впливає на ДНК-залежну РНК-полімерази. В результаті такої реакції відбувається збільшення інтенсивності синтезу білка.
Біологічно активна речовина може приєднуватися і до мітохондрій клітини. Ці структури несуть свою власну генетичну інформацію. Тироксин стимулює окислювальне фосфорилювання в цих структурах.
Гормон стимулює споживання енергії, підвищене споживання кисню на рівні клітин, посилення синтезу білка, ферментів.
Ефекти Т4
Дія гормону на організм різноманітне.
Основні ефекти:
- бере участь в зростанні і розвитку всіх органів і систем,
- збільшує швидкість метаболізму,
- збільшує витрату калорій,
- збільшує синтез теплової енергії,
- підвищує тканинне дихання,
- стимулює розпад глікогену,
- гальмує утворення глікогену,
- прискорює ритм серця,
- сприяє підвищенню кров'яного тиску,
- підвищує тонус нервової системи,
- прискорює утворення нових клітин крові,
- підвищує реабсорбцію води в ниркових канальцях,
- впливає на жировий обмін.
У нормі баланс тироксину і трийодтироніну сприяє активній життєдіяльності людини. І недолік, і надлишок цих речовин призводить до патології.
Норма гормону
Для точної діагностики захворювань ендокринолог частіше рекомендує аналізи на вільні форми гормонів. Саме ці показники характеризують стан залоз внутрішньої секреції.
Нормальні значення вільного Т4 залежать від статі і віку пацієнта.
У новонароджених цей показник повинен бути від 22 до 49 пмоль / л. Норма для немовлят до 10 тижнів — від 9 до 21 пмоль / л. У віці від 2,5 місяців до 5 років рівень Т4 вільного у дитини в нормі дорівнює 8-20 пмоль / л. У дітей старшого віку цей гормон укладається в межі від 8 до 17 пмоль / л. У дорослих вільний Т4 в нормі від 9 до 22 пмоль / л. У жінок під час вагітності та при лікуванні естрогенами часто спостерігається більш високий рівень тироксину.
Гіпотиреоз і тиреотоксикоз
Недолік тироксину — гіпотиреоз. Його причиною може бути аутоімунний тиреоїдит, ендемічний зоб, оперативне або променеве лікування. Пацієнти з недоліком гормону відзначають слабкість, сонливість, порушення пам'яті, сухість шкіри, задишку, рідкісний пульс. Лікування захворювання проводиться ендокринологом. Хворим призначають синтетичний тироксин.
Надлишок гормонів щитовидної залози призводить до тиреотоксикозу. Цей стан супроводжує дифузний токсичний зоб, вузловий зоб з автономією, токсичну . Скарги хворих зазвичай пов'язані з прискореним серцебиттям, пітливістю, зниженням ваги, тремтінням в пальцях рук, нервозністю і безсонням. Лікування тиреотоксикозу проводиться фахівцями в поліклініках і стаціонарах. Медикаментозне вплив направлено на блокаду синтезу тироксину в клітинах щитовидної залози. Для цього застосовуються тиреостатики.
ФСГ (фолікулостимулюючий) гормон
 У гіпофізі головного мозку виробляються гормони тропів. Вони стимулюють роботу периферичних ендокринних залоз. Одне з таких тропів речовин — фолікулостимулюючий гормон (фолікулотропін, ФСГ).
У гіпофізі головного мозку виробляються гормони тропів. Вони стимулюють роботу периферичних ендокринних залоз. Одне з таких тропів речовин — фолікулостимулюючий гормон (фолікулотропін, ФСГ).
Це складне хімічна сполука впливає на формування, розвиток і функцію статевих органів у жінок і чоловіків .
Будова і секреція гормону
ФСГ — це молекула з двох ланцюжків. У складі гормону 85% амінокислот і 15% вуглеводів.
На виділення в кров цієї речовини впливають три фактори:
- гонадоліберину гіпоталамуса (стимулює),
- ингибин статевих органів (пригнічує),
- естрогени і андрогени (пригнічують).
У дорослих максимальний вплив на гонадотропіни надають естрогени і андрогени. Рівень фоллікулотропіна регулюється статевими стероїдами за принципом зворотного зв'язку. Чим менше андрогенів або естрогенів, тим більше виділяється в гіпофізі ФСГ.
У жіночому організмі рівень фолікулостимулюючого гормону безпосередньо залежить від фази менструального циклу. ФСГ у великій концентрації виділяється в перші два тижні після початку менструації. У фолікулярну фазу його концентрація стає дедалі більше. Пік секреції доводиться на дні перед овуляцією. Потім, коли дозріла яйцеклітина виходить в просвіт маткової труби, рівень ФСГ знижується.
Коли настає вагітність, фолікулостимулюючий гормон залишається пригніченим. Його рівень починає зростати тільки через кілька місяців після пологів.
У жінок після клімаксу концентрація фолікулостимулюючого гормону перестає циклічно змінюватися. Його рівень у крові завжди високий. Це пояснюється тим, що гіпофіз продовжує стимулювати яєчники. Але дозрівання яйцеклітин не відбувається, так як статеві залози після менопаузи втрачають чутливість до ФСГ.
У чоловіків фолікулостимулюючий гормон виробляється рівномірно. Ніяких піків секреції і помітних знижень концентрації гормону не спостерігається. У літньому віці ФСГ у чоловіків підвищується. Це є природною реакцією ендокринної системи на старіння організму.
Дія ФСГ
Фолликулостимулирующий гормон відповідає за здатність людини до розмноження. Він підтримує роботу репродуктивної системи.

Вплив ФСГ на жіночий організм:
- стимулює ріст фолікулів в яєчниках,
- підвищує рівень естрогенів,
- провокує перетворення тестостерону в естрогени,
- сприяє овуляції,
- регулює початок і завершення менструації.
Не менш важливий фолікулостимулюючий гормон і для чоловічої репродуктивної системи.
Його роль:
- сприяє розвитку сім'яних канальців в яєчках,
- стимулює утворення зрілих сперматозоїдів,
- регулює роботу клітин Сертолі в яєчках .
і підвищення, і зниження ФСГ призводить до порушення дітородної функції. Рівень гормону змінюється при захворюваннях статевих залоз (яєчників, яєчок), гіпофіза і гіпоталамуса.
Які фактори призводять до низького або високого ФСГ
Низький і високий рівень ФСГ відображає неблагополуччя репродуктивної системи. Коли значення виходить за межі норми, ймовірні різні порушення. Найчастіше зміни ФСГ призводять до безпліддя.
Підвищення фолікулостимулюючого гормону зустрічається при:
- передчасному виснаженні яєчників (ранній клімакс),
- недорозвитку статевих залоз,
- ендометріоїдних кістах,
- маткових кровотечах,
- пухлини гіпофіза (аденомі),
- хірургічному видаленні яєчників або яєчок (кастрації),
- запаленні яєчок,
- синдромі тестикулярной фемінізації,
- зловживанні алкоголем.
Низький ФСГ буває у пацієнтів з:
- вторинним гіпогонадизмом,
- синдромом Шихана,
- пролактиномою,
- синдромом полікістозних яєчників,
- ожирінням.
Крім того, на концентрацію ФСГ в крові впливають гормональні засоби контрацепції, деякі інші лікарські засоби, черепно-мозкові травми та інші чинники.
Коли лікар обстежує пацієнта з порушеним рівнем ФСГ, він оцінює всі можливі причини цього дисбалансу.
Норма фоллікулотропіна
Точні межі нормальних значень ФСГ в різних лабораторіях можуть дещо відрізнятися. Вони залежать від конкретних технологій, методик і реактивів в лікувальному закладі.
Зазвичай фолікулостимулюючий гормон вимірюється в міжнародних одиницях мед / мл.
Норма для дітей залежить від віку і статі. У дівчаток до року ФСГ повинен бути від 1,8 до 20,3 мед / мл. Далі до п'яти років концентрація гормону укладається в рамки 0,6-6,2 мед / мл. До шкільного віку цей показник зменшується до 4,5 мед / мл і залишається стабільним до початку пубертату.
У немовлят чоловічої статі ФСГ повинен бути нижче 3,5 мед / мл, у хлопчиків дошкільного віку — менше 1,5 мед / мл, у молодших школярів — до 3 мед / мл.
У дівчат і жінок дітородного віку норма фоллікулотропіна змінюється за фазами менструального циклу.
Якщо аналіз здавати в фолікулярний період, то ФСГ укладається в межі від 1,37-9,9 мед / мл. У дні овуляції цей показник дорівнює 6,2-17,2 мед / мл. Якщо в лютеїнову фазу циклу, то його концентрація повинна бути від 1 до 9 мед / мл.
Для жінок репродуктивного віку надзвичайно важливо рівновагу між гонадотропінами ФСГ і ЛГ. Рівень першого з них в нормі завжди вище в 1,5-2 рази. Коли фолікулостимулюючого гормону стає відносно багато, то це співвідношення зростає.
У разі коли ФСГ перевищує ЛГ в 2,5 рази і більше, то вірогідні:
- виснаження яєчників (наближення менопаузи) ,
- синдром полікістозних яєчників,
- ФСГ-секретирующая .
у жінок після клімаксу ФСГ в нормі підвищується . Його рівень досягає 19-100 мед / л.
У юнаків до 20 років концентрація гормону в крові дорівнює 0,4-10 мед / мл. У дорослих чоловіків після 21 років цей показник вкладається в межі 1-12 мед / мл.
Коли рекомендують здавати аналіз на гормон
ФСГ зазвичай рекомендує здавати лікуючий лікар: гінеколог, андролог, ендокринолог, репродуктолог і т.д.
Цей гормон визначають разом з цілим рядом інших параметрів (ЛГ, пролактин, статеві стероїди і т.д.) Це дозволяє лікарю скласти цілісне уявлення про здоров'я пацієнта.
Гормон досліджують:
- при безплідді,
- при нерегулярних місячних,
- при маткових кровотечах,
- при відсутності овуляції,
- при мимовільному аборті,
- при ендометріозі,
- при поликистозе яєчників,
- при зниженні статевого потягу,
- при імпотенції,
- при хронічних запаленнях статевої системи,
- при затримці росту і розвитку дітей,
- при передчасному статевому дозріванні.
Як здавати гормон
Жінкам рекомендують здавати аналізи на гонадотропіни в конкретні дні менструального циклу. Зазвичай лікарі призначають дослідження на 3-5 або 6-7 день.
У чоловіків, у дітей, у жінок після клімаксу або з аменореєю іншої причини, у вагітних ФСГ визначають в будь-який день місяця.
Щоб отримати точні результати, необхідно обмежити фізичні і емоційні навантаження за 2-3 дня до забору крові. У день дослідження рекомендується не палити (хоча б 60 хвилин до аналізу). Напередодні ввечері варто обмежити в меню жирну їжу. Також необхідно утриматися від спиртного. Кров на ФСГ здають строго натщесерце. Будь-яку їжу, солодкі напої, кава і чай потрібно виключити на 8-12 годин. На аналіз найкраще приходити в ранкові години (з 7 до 11).
