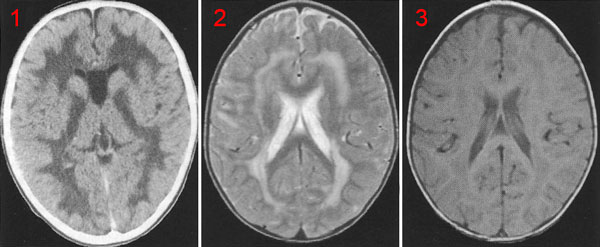
Гнійні менінгіти — група захворювань з переважним ураженням оболонок мозку бактеріальної природи, що об'єднує ряд окремих нозологічних форм, що характеризуються загальними клінічними і морфологічними ознаками. Збудниками гнійного менінгіту можуть бути менингококки, стафілококи, пневмококи і інші бактеріальні агенти.
В останні роки в зв'язку з широким застосуванням ефективних антибактеріальних засобів збільшується число захворювань, викликаних синьогнійної паличкою ,, вульгарним протеєм та іншими мікроорганізмами, стійкими до антибіотиків і сульфаніламідів. Гнійні менінгіти можуть бути первинними і вторинними.
Менінгококовий менінгіт
Етіологія менінгококового менінгіту
Типовим представником первинних гнійних менінгітів є менінгіт, викликаний менингококком Neisseria meningitidis. Менінгокок представляє грамотріцательньщ диплококк Вейксельбаума, який легко виявляється при мікроскопічному дослідженні і лейкоцитах або внеклеточно. Виділяють чотири групи менінгококу, що відрізняються за своїми біологічними властивостями. Частіше за інших зустрічаються менінгококи групи А, більш чутливі до дії сульфаніламідів. Коки групи В, С і D менш чутливі до впливу цих препаратів. Останнім часом виявлено ще декілька груп диплококков Вейксельбаума.
Епідеміологія менінгококового менінгіту
Менінгококова інфекція передається крапельним шляхом. Джерелом інфекції є хвора людина або здоровий носій. Менінгококи дуже нестійкі до впливу зовнішніх факторів — температурних коливань, недостатній вологості повітря, впливу сонячного світла і швидко гинуть поза людським організмом.
Мабуть, цим почасти пояснюється відносно низька контагіозність захворювання. Безсумнівно, велику роль відіграє також ступінь сприйнятливості макроорганізму до менінгококової інфекції.
Як правило, захворювання має спорадичний характер, але іноді відзначаються невеликі епідемії. Їх вираженість має певну періодичність. У країнах Європи і Америки останній підйом менінгококової інфекції відзначався в період другої світової війни і в перші повоєнні роки. Захворювання характеризується також досить чітко вираженою сезонністю — найбільше число спалахів реєструється в зимово-весняний період. Захворювання відзначається в осіб різного віку, але хворіють переважно діти, особливо ясельного та дошкільного віку.
Менінгококова інфекція може проявлятися різними формами — безсимптомним бактерионосительством, назофарингіт, артритом, пневмонією, менінгококцемія, гнійним менінгітом і менінгоенцефалітом. Тому стара назва «епідемічний цереброспінальної менінгіт» замінено більш правильним — «менінгококовий менінгіт», як частковий вияв менінгококової інфекції [Покровський В. І., 1976].
Патогенез менінгококового менінгіту
Після потрапляння в організм менінгокок спочатку вегетирует в верхніх дихальних шляхах, викликаючи первинний назофарингіт, що протікає зазвичай латентно. У осіб, менш резистентних до інфекції, менінгокок потім проникає в кров і розноситься по всьому організму. Найбільш переконливим доказом такого шляху поширення інфекції служить менінгококцемія, нерідко супроводжується висипанням характерною геморагічної висипки.
Клініка менінгококового менінгіту
В результаті проникнення менінгококів в оболонки мозку в них розвивається запальний процес, зовні виявляється клінічною картиною гнійного менінгіту. Захворювання зазвичай розвивається раптово. Початок настільки гостре, що хворий або навколишні можуть вказати не тільки його день, а й годину. Температура підвищується до 38-39 ° С, виникає резчайшая головний біль, яка іноді іррадіює в шию, спину і навіть в ноги. Головний біль супроводжується блювотою, що не приносить полегшення.
З'являються загальна гіперестезія, менінгеальні симптоми — Керніга, Брудзинського, — ригідність м'язів потилиці, проте їх вираженість може бути різною і не завжди відповідає тяжкості процесу. Нерідко на початку захворювання відзначається брадикардія — 50-60 ударів в секунду. Протягом захворювання частота пульсу збільшується, в деяких випадках виникає аритмія.
Свідомість спочатку збережено, але в разі несвоєчасного початку лікування затемнюється, хворий впадає в сопорозное стан. Може спостерігатися різке рухове збудження, іноді делириозное стан. У міру прогресування захворювання збудження змінюється сонливістю і ступором, перехідним в кому. Очне дно залишається нормальним, іноді відзначається деяке розширення венозних судин. У дітей грудного віку початок хвороби проявляється загальним занепокоєнням, різким плачем, нерідко виникають судоми клоніко-тонічного характеру, що переходять іноді в епілептичний статус. Дуже важливий для діагностики менінгіту у немовлят симптом вибухне і напруження великого джерельця.
Нерідко на 3-4-й день хвороби відзначаються герпетичні висипання на шкірі і слизових оболонках порожнини рота, губ.
З локальних неврологічних симптомів частіше відзначається ураження окорухових нервів: диплопія, птоз, анізокорія, косоокість. Рідше спостерігається ураження інших черепних нервів. До застосування пеніциліну часто страждали слухові нерви, і глухота була одним з найбільш частих ускладнень менінгіту. В даний час необоротна поразка VIII пари відзначається рідко.
При аналізі крові виявляються лейкоцитоз і збільшена ШОЕ. Однак можливі випадки захворювання з нормальною картиною крові.
Морфологія менінгококового менінгіту
Субарахноидальное простір заповнений гнійним ексудатом. Поверхневі вени розширені. Скупчення гною відзначається переважно на конвекситальной поверхні кори, по підставі мозку, на оболонках спинного мозку. З оболонок мозку запальний процес по периваскулярні просторів переходить на речовину мозку. В результаті виникають набряк, невеликі гнійні вогнища в речовині мозку, дрібні крововиливи і тромби в судинах. Мікроскопічно в оболонках мозку визначається картина запально-клітинної інфільтрації. На різних стадіях захворювання вона носить переважно поліморфнонуклеарних характер, а потім з'являються лімфоцити і плазматичні клітини. У шлуночках, часто значно розширених, міститься каламутна рідина.
Спинномозкова рідина (в перші години захворювання) може бути не змінена, але вже на 1-2-й день тиск її різко підвищується, прозорість втрачається, вона стає каламутною , іноді сіруватого або жовтувато-сірого кольору. Кількість клітин різко підвищено і досягає сотень і тисяч в 1 мм 3. Це переважно нейтрофіли і незначне число лімфоцитів. При мляво розвивається процесі можливо переважання лімфоцитів. У клітинах можуть бути виявлені менингококки. Кількість білка в лікворі підвищений, іноді до 10-15% — Різко знижений вміст глюкози. Зниження рівня хлоридів має вторинний характер, будучи обумовлено частою блювотою, і не має діагностичного значення. Підвищується рівень імуноглобуліну IgM, а також активність багатьох ферментів, особливо в тих випадках, коли перебіг захворювання приймає хронічний характер. Реакція Ланге має западання в правій частині кривої.
Тривалість захворювання при адекватному лікуванні в середньому становить 2-6 тижні, однак можливі гіпертоксичні форми, що протікають блискавично і призводять до летального результату протягом першої доби.
Менінгококцемія
Характерною клінічною особливістю цієї форми менінгококової інфекції є виникнення на шкірі геморагічної висипки — зазвичай грубої, що має вигляд зірочок різної форми і величини, щільних на дотик, які виступають під рівнем шкіри. Найчастіше висип з'являється в області сідниць, стегон, на гомілках. Іноді уражаються суглоби. Підвищується температура, розвивається, тахікардія, знижується артеріальний тиск, виникають задишка та інші симптоми загальної інтоксикації. Менінгококцемія може супроводжуватися ураженням оболонок мозку, але може протікати і без явищ менінгіту.
Найбільш важке проявлення менінгококової інфекції — бактеріальний шок. У цьому випадку захворювання розвивається гостро. Раптово підвищується температура, виникає озноб. Незабаром з'являється рясна геморагічна висипка, спочатку дрібна, а потім більша, з некротичними ділянками. Пульс частішає, артеріальний тиск знижується, тони серця стають приглушеними, дихання нерівномірним. Іноді виникають судоми. Хворий впадає в коматозний стан. Розвивається картина судинного колапсу. Дуже часто, не приходячи до тями, хворий вмирає. Тривалий час такий результат пов'язували з руйнуванням коркового шару падпочечнкков (синдром Уотерхауса — Фрідерікеена). В даний час припускають, що причиною такого важкого перебігу в основному є ендотоксичний шок, що приводить до порушення гемодинаміки в результаті ураження дрібних судин і підвищення згортання крові, що супроводжуються утворенням великої кількості микротромбов (синдром диссеминированной внутріеосудістой згортання). Поразка наднирників в частині випадків не виявляється.
Вторинні гнійні менінгіти
Етіологія. Вторинні гнійні менінгіти виникають при наявності гнійного вогнища в організмі. Вони можуть розвиватися або в результаті безпосереднього переходу інфекції з гнійних вогнищ на оболонки мозку, наприклад, при гнійному отиті або гаймориті, тромбозі синусів твердої мозкової оболонки, абсцес мозку, або шляхом метастазування з гнійних вогнищ, розташованих на віддалі, наприклад, при абсцесах або бронхоектазах легких, виразковий ендокардит та ін. Гнійний менінгіт іноді ускладнює проникаючі поранення черепа.
Збудниками вторинного гнійного менінгіту можуть бути різні бактерії: — пневмококи, стафілококи, гемофільна паличка Афанасьєва — Пфейффера, сальмонели, синьогнійна паличка, лістерелли.
Клініка вторинних гнійних менінгітів
Захворювання починається з різкого погіршення загального стану, головний біль, підвищення температури, ознобу. Рано виникають менінгеальні симптоми. Нерідко, особливо в дитячому віці, з'являються судоми. Швидко настає порушення свідомості, що супроводжується у багатьох випадках психомоторнимзбудженням, галюцинаціями. Досить часто відзначається ураження черепних нервів: птоз, косоокість, диплопія, парез лицьового нерва. Розвиваються тахікардія, що змінюється потім брадикардією, тахіпное. М'язовий тонус знижується. Глибокі рефлекси викликаються насилу, рано зникають черевні рефлекси. Підошовні рефлекси спочатку не змінюються, але в більш пізніх стадіях захворювання можуть з'явитися патологічні знаки. Загальний важкий стан хворих нерідко супроводжується порушенням функції тазових органів. Спинномозкова рідина каламутна, витікає під великим 'Тиском. Різко підвищений нейтрофільний цитоз, що досягає декількох тисяч клітин, підвищений вміст білка, іноді до 8-10%. У крові виявляється високий лейкоцитоз, із зсувом формули вліво, що досягає 15-20- 10в9 / л, збільшена ШОЕ.
Перебіг менінгіту гостре. Але можливо як блискавичне, так і хронічний перебіг захворювання. У деяких випадках типова клінічна картина менінгіту маскується вираженими явищами загального септичного стану. При пізньому початку або недостатньо активному лікуванні антибіотиками захворювання може закінчитися гідроцефалією, а також розвитком стійких паралічів, атаксії, порушень зору і слуху, епілепсії, деменції.
При будь-яких формах гнійного менінгіту можуть виникати важкі ускладнення, що вимагають невідкладної допомоги — гостре набухання і набряк мозку, а також субдуральний випіт. Набряк і набухання мозку спостерігаються зазвичай при надгострий формах менінгіту і супроводжуються швидким наростанням загальномозкових симптомів. Обмеження стовбура мозку в тенториальном отворі мозочка і в великому потиличному отворі зміщаються миндалинами мозочка обумовлює важкі порушення серцево-судинної і дихальної систем.
Прогресуюче наростання осередкової симптоматики на тлі стихає оболонкових симптомів, що супроводжується появою застійних сосків, гектической температури, свідчить про формування субдурального випоту. Для диференціальної діагностики від енцефалітіческого синдрому слід вдатися до ехоенцефалографії, що дозволяє виявити зміщення серединних структур. У разі необхідності проводять ангіографію. Достовірні результати можуть бути отримані при комп'ютерній томографії.
Встановлення етіологічного фактора, що викликав конкретний випадок менінгіту, представляє значні труднощі і вимагає спеціальних бактеріологічних досліджень.
Співвідносна частота збудників, що викликають розвиток гнійного менінгіту по Gilroy (1969), наступна. У період новонароджене ™: кишкова паличка, сальмонели, стрептококи, золотистий стафілокок, стрептокок. У дитячому віці: менінгокок, паличка Афанасьєва — Пфейффера, пневмокок, кишкова паличка, стрептокок. У дорослих: менінгокок, пневмокок, стрептокок, золотистий стафілокок, паличка Афанасьєва — Пфейффера. Так, наприклад, пневмококові менінгітом хворіють переважно діти раннього віку та особи старше 40 років.
Джерелом інфекції є хронічні отити і синусити, мастоїдити і т. Д. Попаданню інфекції в оболонки мозку сприяють травми черепа (особливо при переломах в області передньої черепної ямки з пошкодженням lamina cribrosa), операції на придаткових пазухах носа і інші маніпуляції в цій області. Початку захворювання можуть передувати продромальний неспецифічні симптоми у вигляді загального нездужання і незначного підвищення температури. Шкірні висипання, часто зустрічаються при менінгококової менінгіті, для пневмококової менінгіту не характерні, за винятком herpes labialis. Клінічний перебіг характеризується винятковою тяжкістю, наявністю не тільки менінгеальних, але і енцефалітіческіе симптомів — судоми, ураження черепних нервів, порушення свідомості.
Спинномозкова рідина при пневмококової менінгіті каламутна, має зеленувате забарвлення. Бактериоскопия може виявити розташовані внеклеточно ланцетообразние диплококки. Навіть в умовах адекватного лікування смертність досягає 20-60%. Для пневмококової менінгіту характерно щодо нерідке розвиток субдурального випоту. Висловлюється думка, що при відсутності поліпшення протягом двох діб в умовах інтенсивної терапії антибіотиками (ампіцилін, левоміцетин) показано нейрохірургічне обстеження з метою виявлення показань до краніотомії.
Важко протікають також менінгіти, викликані стафілококової інфекцією. Виникненню менінгіту зазвичай передують хронічні пневмонії, абсцеси, остеомієліт, септичний стан. В останньому випадку картина менінгіту нерідко маскується важким загальним станом хворого. Менінгіти, викликані стафілококом, схильні до абсцедування і блокаді лікворних просторів.
Своєрідна клінічна картина менінгіту, що викликається гемофільної палички Афанасьєва — Пфейффера. Частіше хворіють ослаблені діти у віці до року, які страждають хронічними катарами верхніх дихальних шляхів, отити, пневмонією. Розвиток хвороби зазвичай повільне, рідше — гостре. Перебіг мляве, хвилеподібний, з періодами погіршення і поліпшення, хоча ~ возм5Жни_случаі ~ з важким і гострим перебігом і несприятливим результатом. Спинномозкова рідина зазвичай каламутна, молочно-білого і жовто-зеленого кольору. Кількість клітин може бути відносно невеликим (до 2000 в 1 мкл). При своєчасному початку лікування і правильному його веденні захворювання протікає відносно сприятливо і нерідко призводить до повного одужання.
Гнійні менінгіти, викликані синьогнійною паличкою, сальмонелами, кишковою паличкою, лістерелламі зустрічаються значно рідше. Етіологічний діагноз цих менінгітів, як правило, може бути встановлений тільки в результаті бактеріологічного дослідження спинномозкової рідини і крові.
Лікування гнійних менінгітів
Загальний принцип лікування полягає в тому, що як можна раніше, при першій підозрі на можливість менінгіту призначають найбільш універсальний за своєю дією антибіотик. Одночасно прагнуть виділити інфекційний агент і визначити його чутливість до різних антибіотиків. В подальшому переходять на лікування тими з них, до якого даний бактеріальний агент виявився найбільш чутливим. На практиці, однак, далеко не завжди вдається виділити збудника і визначити його чутливість до того чи іншого антибіотика.
Як показав! багаторічний досвід, максимальний ефект при менінгітах ,, викликаних кокової флорою, відзначається при внутрішньом'язовому введенні солей бензілпеніцілліновой кислоти з розрахунку 200 000-300 000 ОД на 1 кг маси у дорослих і 300 000-400 000 ОД у дітей у віці до 3 міс, що складає в залежності від маси хворого від 12 до 18 млн. ОД на добу. Повторні введення антибіотика через кожні 4 год у дорослих і через кожні 2 год у грудних дітей дозволяють підтримувати відносно постійний рівень його концентрації в спинномозковій рідині. Клінічний ефект терапії проявляється поліпшенням стану хворих, проясненням свідомості, зменшенням головного болю, зниженням температури, зникненням менінгеальних симптомів, санацією спинномозкової рідини.
Тривалість лікування визначається клінічним перебігом болезмі і зазвичай дорівнює 5-7 дням. Основним критерієм скасування пеніциліну є санація спинномозкової рідини:
зниження цитоза нижче 100 клітин в 1 мкл, при переважанні лімфоцитів (не менше 75%), що зазвичай досягається до цього терміну. При своєчасному початку лікування і достатній дозуванні антибіотиків у більшості хворих відзначається повне одужання [Покровський В. І., 1976].
Якщо хворий поступає в тяжкому коматозному стані або з явними симптомами менінгоенцефаліту в пізні терміни хвороби, на 4 5-й день від початку захворювання, показано внутрішньовенне ст! едення натрієвої солі пеніциліну від 4 до 12 млн. ОД в ссуткі при одночасному внутрішньом'язовому введенні 800 000-1 000 000 ОД пеніциліну на 1 кг маси на добу. У деяких випадках при неефективності лікування пеніциліном необхідно застосувати інші антибіотики. Широке поширення отримав левоміцетин, особливо його форма для парентерального введення — левоміцетину сукцинат натрію. Його призначають з розрахунку 50-100 мг / кг і вводять 3-4 рази на добу. Тривалість курсу лікування 7-10 діб. Левоміщетін краще за інших антибіотиків проникає через гематоенцефалічний бар'єр. У деяких випадках менінгококового менінгіту відзначається задовільний ефект від застосування тетрацикліну. Все більше застосування в лікуванні гнійних менінгітів знаходять напівсинтетичні пеніцілліши — ампіцилін, оксацилін, метицилін.
Вони особливо ефективні при пневмококової та стафілококової менингитах. Ампіцилін призначають з розрахунку 200-300 мг / кг на добу при шестикратному введенні, а оксацилін і метицилін до 300 мг / кг на добу. Метицилін вводять через 4 ч, а оксацилін через 3 ч. При гнійних менінгітах різної етіології високоефективним засобом є також антибіотик з широким спектром дії цефалоридин (цепорин), його вводять парентерально по 1 г кожні 6 ч. Цефалоридин і його аналоги значно стійкіше, ніж пеніцилін, до стафілококової пеніцилінази, що робить його призначення особливо показаним при менінгітах, викликаних стафілококами, стійкими до бензилпеніциліну.
Успішне лікування гнійних менінгітів проводиться також сульфаніламідними препаратами пролонгованої дії, зокрема сульфамонометоксін . При лікуванні сульфамонометоксін ефект настає раніше, ніж при лікуванні пеніциліном. Нормалізується температура, поліпшується картина крові. Кілька повільніше, проте, відбувається санація спинномозкової рідини і зникають менінгеальні симптоми. Сульфамонометоксин призначають всередину в таблетках за наступною схемою: в першу добу 2 г 2 рази на день, наступні — по 2 г 1 раз в день.
Тривалість курсу лікування 5-9 днів. Лікування сульфамонометоксін можна проводити в комбінації з пеніціллінотерапія. Лікування починають з ін'єкцій пеніциліну, потім після поліпшення загального стану, припинення блювоти і нормалізації свідомості призначають сульфамонометоксин. При проведенні пенициллинотерапии слід мати на увазі, що ін'єкції калієвої солі пеніциліну необхідно проводити повільно, щоб запобігти можливості виникнення тахіаритмії. Надмірне введення натрієвої солі пеніциліну може супроводжуватися затримкою рідини в організмі.
Якщо етіологію гнійного менінгіту встановити не вдається, показано проведення комбінованої терапії двома — трьома антибіотиками або поєднанням антибіотиків і сульфаніламідних препаратів. Ефективною при більшості гнійних менінгітів є комбінація пеніциліну і левоміцетину, що володіє широким спектром дії. Левоміцетин вводятьпарентерально у вигляді левоміцетину сукцинату натрію з розрахунку до 100 мг / кг 3-4 рази на добу. Парентеральне введення інших антибіотиків широкого спектра дії менш бажано, так як внутрішньом'язовіін'єкції антибіотиків групи тетрацикліну дуже болючі, а їх внутрішньовенне вливання часто ускладнюється Флебіти. Антибіотики — макроліди (еритроміцин, олеандоміцин) погано проникають через гематоенцефалічний бар'єр.
При лікуванні великими дозами антибіотиків можливі ускладнення. Застосування пеніциліну і напівсинтетичних антибіотиків може супроводжуватися головним болем, підвищенням температури, висипанням на шкірі, кропив'янка, болями в суглобах. Можливий розвиток лейкопенії при призначенні ампіциліну або гематурії при лікуванні метициліну. Застосування тетрацикліну іноді викликає шкірні висипання або симптоми подразнення шлунково-кишкового тракту. В особливо важких випадках, коли з'являються ознаки інфекційно-токсичного шоку (висока температура, геморагічний висип, блювання, падіння артеріального тиску, задишка, «трупні плями» на шкірі, судоми, вимикання свідомості), показаний весь комплекс реанімаційних заходів, в першу чергу парентеральневведення кортикостероїдних гормонів (гідрокортизон по 5-75 мг / кг на добу або преднізолон по 15-30 мг / кг на добу залежно від стану хворого), норадреналіну, розчинів поліглюкіну, реополіглюкіну, кисень.
Розвиток набряку мозку купіруют манітолом (10-15-20% розчини) в поєднанні з ін'єкціями кортикостероїдів, лазикса і етакриновою кислоти (Урегіту ®). Одночасно проводять корекцію електролітного балансу і введення рідини, щоб уникнути зневоднення організму. Не слід прагнути до зниження підвищеної температури тіла, суб'єктивно що полегшує самопочуття хворого, так як концентрація антибіотиків в крові при високій температурі виявляється більш значною. Корекція політично сумішами (в першу чергу фенотіазинові похідні) та жарознижувальними засобами (реопирин внутрішньом'язово) необхідна лише у випадках різкої гіпертермії, що досягає 41-42 ° С.
Для полегшення стану хворого призначають холод на голову, болезаспокійливі засоби. Необхідно стежити за станом сечового міхура і кишечника, охороняти хворого від утворення пролежнів. У випадках вторинних гнійних менінгітів показано хірургічне лікування гнійних процесів у вусі або придаткових порожнинах носа, що є причиною захворювання.