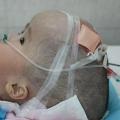
Гемолітична хвороба новонароджених — одне з найважчих захворювань періоду новорождепності. У колишні роки летальність при цьому захворюванні становила 60-80%. У період внутрішньоутробного розвитку воно часто призводило до мимовільних викиднів і мертвонароджень. Таким чином, гемолітична хвороба характеризувалася високою перинатальною смертністю.
Етіологія гемолітичної хвороби новонароджених
Етіологія гемолітичної хвороби новонароджених була невідомою до відкриття Landschteiner і Viner (1940) резус-фактора в крові людини. Вони довели, що причиною хвороби є біологічне невідповідність крові матері і дитини по резус-антигену (у матері резус-мінус, у дитини — резус-плюс). При цьому протягом вагітності резус-позитивний плід імунізують материнський організм (резус-антигени проникають через плацентарний бар'єр в потік крові матері). Як наслідок изоиммунизации в крові матері з'являються резус-аптітела, які, проникаючи до плоду, викликають руйнування його резус-позитивних еритроцитів, пошкоджують печінку, органи кровотворення і ін.
За даними Levine (1941), для імунізації жінки вагою 48 кг достатньо 0,13 мл крові плоду. Така кількість крові може легко проникнути в материнський кровотік, якщо врахувати, що загальна поверхня ворсинок — 6,5 м2, довжина — 18,35 км, а цілість ворсин, особливо при наявності захворювань у матері, може бути легко порушена.
Mischer, Vorlender відзначають можливість утворення в стінці матки інфаркту (внаслідок реакції антиген — антитіло), що полегшує передачу антитіл від матері до плоду.
За даними А. І. Струкова (1958), резус-фактор у крові плоду людини вперше визначається з 3-го місяця внутрішньоутробного розвитку. Отже, з цього часу резус-антигени можуть надходити в материнський організм.
Ступінь изоиммунизации материнського організму (висота титру резус-антитіл) наростає з кожною наступною вагітністю.
Гемолітична хвороба рідко буває у дитини після першої вагітності матері, виняток становлять лише ті випадки, коли матері в минулому переливали резус-позитивну кров (внутрішньом'язово або внутрішньовенно), часто задовго до вагітності, що сприяло изоиммунизации крові.
Ізоіммунізація після переливання крові завжди дуже небезпечна, вона супроводжується утворенням великої кількості антитіл, які зберігаються протягом усього життя (масивне надходження антигену при трансфузії крові). Тільки введена і перші місяці життя резус-позитивна кров не викликає изоиммунизации (Lubold, Kunc-Penze).
Гемолітична хвороба новонароджених на грунті изоиммунизации може бути викликана але тільки несумісністю крові матері і дитини по резус-фактору і його типам (Rh °, Rh ', Rh' і поєднання їх), по і по групових антигенів системи АВО, а також іншим додатковим антигенів крові (М, N, S, Fy, Hell, Р і ін.). Тому в кожному випадку гемолитического захворювання необхідно проводити ретельне серологічне обстеження крові матері і дитини для визначення причини изосенсибилизации.
Незважаючи на величезні успіхи імуногематології, проблема етіології і патогенезу гемолітичної хвороби і в даний час ще не вирішена. Неясна причина індивідуальної чутливості та стійкості до резус-імунізації резус-негативного організму. Так, на підставі множинних обстежень встановлено, що резус-позитивний населення становить 85%, резус-негативний 15%, резус-несумісність в шлюбі спостерігається в 9,5-13% всіх шлюбів. Частота гемолітичної хвороби значно менше і становить від 0,3 до 0,7%.
Імунізація і народження хворої дитини мають місце лише у 1 з 20-25 резус-негативних жінок, що мають резус-позитивного чоловіка, хоча резус -фактор має домінантний спадковий ознака. Очевидно, для изоиммунизации материнського організму та запобігання проявам хвороби у дитини необхідні ще додаткові умови. Мають значення характер реактивності організму матері, індивідуальні особливості її судинної системи, особливо ступінь проникності судин плаценти, наявність захворювань (токсикози, гіпертонічна хвороба, інфекційні хвороби).
Різна чутливість до резус-антигену може бути обумовлена активно набутою стійкістю ( резус-негативні женщіпи, рождепние резус-пололштельнимі матерями). на ступінь изоиммунизации материнського організму впливають також властивості резус-антигену батька: якщо резус-антиген крові батька гомозиготний, всі діти, на думку К. Штерна, будуть резус-позитивними.
Функціональний стан організму плода, особливо функція печінки, кровотворення, сприйнятливість до дії антитіл, здатність до їх нейтралізації, біохімічні та морфологічні особливості еритроцитів мають велике значення в генезі розвитку гемолітичної хвороби.
Патогенез гемолітичної хвороби новонароджених
Раніше в патогенезі гемолітичної хвороби провідне місце відводили посиленому гемолізу еритроцитів плоду в результаті реакції антиген — антитіло.
В даний час гемоліз вселедствіе передувала изоиммунизации, як основна ланка патогенезу, має значення в розвитку набряку і анемічній форм гемолітичної хвороби. У розвитку найбільш частою форми гемолітичної хвороби-жовтушною-головну роль відводить функціональному стану печінки плода, її зниженою здатності переводити токсичний непрямий білірубін в прямий (били рубай і ді глікуронід) — нетоксичний з'єднання, добре розчинний у воді і виведене з організму нирками.
Процес детоксикації непрямого білірубіну здійснюється в печінкових клітинах за допомогою ензимної системи, в якій головне значення має активність ферменту глюкуронтрансферази, що зв'язує непрямий білірубін з двома молекулами глюкуронової кислоти (непрямий білірубін + 2 молекули глюкуронової кислоти — білірубіндіглюкуронід). Відсутність повного паралелізму між ступенем изоиммунизации материнського організму і тяжкістю хвороби дитини, ступенем гемолізу (тобто анемизацией) і гіпербілірубінемією при важкої жовтушною гемолітичної хвороби і, нарешті, дані літератури останніх років про можливість розвитку важкої гіпербілірубіновой енцефалопатії поза зв'язком з попередньою ізоіммунізація (у незрілих дітей , які перенесли гіпоксію і так звану генуинную жовтяницю) дозволяють вважати таким, що очолює в розвитку жовтушною форми гемолітичної хвороби новонароджених дітей функціональний стан печінки новонародженого.
Більш того, доведено, що в основі фізіологічної жовтяниці новонароджених лежить також вроджена недостатність ферменту глюкуронтрансферази. Гипербилирубинемия властива всім новонародженим. Рівень білірубіпа в плазмі здорових новонароджених схильний до великих індивідуальних коливань — 2-12 мг% (в середньому близько 7 мг%).
Гемолітична жовтяниця характеризується досить швидким наростанням рівня непрямого білірубіну в крові, пізніше з'являється і прямий білірубін внаслідок застою пігменту в печінці і порушення екскреторної функції її.
Функціональний стан печінки при гемолітичній жовтяниці страждає в силу вищевказаної недостатності білірубінсвязивающего ферменту (глюкуронтрансферази). Крім цього, можливо, впливають осередки еритробластозу в печінці, пошкодження печінкових клітин токсичним непрямим білірубіном і застійні явища.
Існує, безсумнівно, зв'язок процесів зв'язування білірубіну з углеводпим обміном. Всі фактори, що негативно впливають на баланс глюкози в організмі, гальмують також і процес кон'югації непрямого білірубіну.
Рівень білірубіну в крові регулюється складними факторами. На концентрацію його в крові впливає кількість і склад плазми, позасудинний рідини (в сироватці крові практично весь білірубін знаходиться в зв'язаному стані з білками крові), діффундібельность і розчинність пігменту, спорідненість різних тканин до нього і місцеві відмінності проникності судин, рН крові, ступінь ацидозу , гіпоксії.
У походження гіпербілірубіпсміі недоношених має інічепіе велика пезролость печінки і проникність гематоенцефалічного бар'єру, а також незрілість гемоглобіну (фетальний гемоглобін). Деякі медикаменти, що вводяться вагітної перед пологами (аспірин, кофеїн, вітамін К), пригнічують еізімнио системи печінки плода і також сприяють розвитку гінербілірубіноміі.
Сульфаніламідні препарати, деякі антибіотики, саліцилати, хініп, кофеїн транспортуються в крові людини у вигляді альбумінового комплексу, зв'язуючись з білковою молекулою там же, де і білірубін. Вживання перерахованих медикаментів сприяє затримці білірубіну в тканинах, посилення його токсичного ефекту.
Важка гіпербілірубінемня у новонароджених може спостерігатися також при спадковому сфероцптозе, гемолітична анемія з пікноцітозом, існує також семейпая жовтяниця на грунті вродженого дефекту кон'югації і екскреції білірубіну.
Для визначення етіологічного фактора всякої важкої жовтяниці необхідно проводити ретельне обстеження матері і дитини (гематологічне, біохімічне, серологічне дослідження).
В патогепезе гемолитического захворювання недостатність печінки і процес гемолізу еритроцитів тісно переплітаються, і на перший план виступає то один з цих факторів, то інший, залежно від індивідуальних особливостей дитини, стану изоиммунизации.
В патогенезі набряку форми хвороби має значення гипериммунизации з гемолізом еритроцитів, а також недостатність печінки, нирок і порушення водно-сольового обміну.
Клініка і діагностика гемолітичної хвороби при резу з-н есовместімості крові матері і дитини
Загальновизнано підрозділ гемолітичної хвороби новонароджених на три клінічні форми:
1) загальний вроджений набряк плода (hydrops foetus universalis),
2) важка жовтяниця новонароджених (icterus gravis neonatorum),
3) вроджена анемія новоронеденних (anaemia neonatorum congenita).
Частота гемолітичної хвороби новонароджених на грунті резус-імунізації, за даними різних авторів, коливається в обмежених межах.
Крім трьох перерахованих клінічних форм гемолітичної хвороби, Г. П. Полякова (1972) виділяє ще перехідні форми — жовтяничній-осередкову і жовтяничній-анемічну.
Отечная форма гемолітичної хвороби — найбільш важке захворювання.
Важкість захворювання обумовлена тим, що зазвичай мати різко імунізована до резус-антигену (високий титр резус-антитіл в крові), і плід захворює задовго до народження.
Клінічна картина характерна: виражений загальний масивний набряк всіх покривів і порожнин (плевральної, перикардіальної і черевній) плода, різка блідість, гепатоспленомегалія. Плацента зазвичай набрякла, інфільтрована, вага її 1,5-2 кг, в ній можуть бути інфаркти.
У крові виявляють значну анемію (нь — 40-20 од., Еритроцитів 2 000 000-1 300 000 на 1 мм3 крові) з наявністю молодих форм червоної крові (нормобласти, еритробласти), часто з різко підвищеним лейкоцитозом і зрушенням лейкоцитарної формули до юних і мієлоцитів.
Як правило, дитина гине під час пологів або в перші години після народження. При патологоанатомічному дослідженні виявляють різке збільшення печінки, селезінки з гемосидерозом, мноі «ествепние осередки гемоноеза, набряк порожнин.
набряку гемолітичної хвороби слід диференціювати з природженим набряком на грунті токсоплазмозу, лістерелеза, сифілісу, а також при важкому пороці серця з різко вираженим порушенням кровообігу.
Важка жовтяниця новонароджених. Ця форма хвороби друга по тяжкості (після набряку форми) і є найбільш частим і типовим варіантом захворювання.
Жовтуха з'являється рано — в першу добу після, народження або дитина вже народжується желтушним. Желтушность інтенсивно наростає, і до 3-4-го дня життя шкіра дитини стає яскраво-жовтою (шафранного кольору з зеленуватим відтінком), сеча і кал також яскраво-жовтого кольору. На 3-5-й день при відсутності правильного лікування з'являються симптоми важкої билирубиновой інтоксикації центральної нервової системи, відомої клініцистам як синдром ядерної жовтяниці (kernicterus). Її вперше описав Schmorl (1904).
« Ядерна жовтяниця » — поняття анатомічне (фарбування в жовтий колір ядер підстави мозку). Без попередньої изоиммунизации вона розвивається іноді у недоношених при вродженої недостатності ензимних систем печінки.
Жовте забарвлення нуклеарні мас мозку — головний прояв гострої стадії захворювання. Частота ураження залежить головним чином від вмісту пігменту (непрямого білірубіну) в крові і тривалості його дії на мозок.
При розвитку ядерної жовтяниці діти стають млявими, часто виникають судоми, окорухові розлади, гіпертермія. Особливо характерна для цього захворювання поза хворого — опістотопус — витягнуті злегка ротирована кінцівки і стислі кулачки (поза боксера).
Печінка і селезінка збільшені, але не завжди. Анемія в перші дні життя часто відсутня. Якщо дитина переживає перший тиждень життя, у нього, як правило, розвивається швидко прогресуюча анемія.
Ж. Доссе (1956) виділяє три стадії в перебігу жовтяничного варіанту хвороби: при народженні і в перші кілька годин після нього — перша прихована фаза , коли клінічних ознак хвороби немає, і тільки при лабораторному обстеженні дитини (у випадках встановлення резус-конфлікту) можна виявити гипербилирубинемию (білірубіну в пуповинній крові більше 3-4 мг%), помірну анемію, іноді зі збільшенням числа ядерних форм еритроцитів, часто з високим ретикулоцитозом. Очспь важливо почати лікування саме в цій стадії хвороби.
Друга фаза захворювання характеризується появою клінічних симптомів хвороби — ранній жултухі (в першу добу), яка інтенсивно наростає. Нерідко одночасно помітно збільшуються в розмірі печінка і селезінка. Рівень білірубіну в крові швидко наростає, досягаючи 15-20 і навіть 30 мг%, причому ступінь гіпербілірубінемії у хлопчиків більше, ніж у дівчаток. І в цьому періоді захворювання (в перші 24-36 год після народження) зазвичай ще теж не пізно почати лікування.
В третій фазі хвороби стан дитини дуже важкий, виражені явища загальної інтоксикації і симптоми пошкодження центральної нервової системи. У цій фазі лікування, як правило, неефективно, діти гинуть, а у тих, що вижили залишаються важкі незворотні зміни з боку центральної нервової системи — глухота, відсталість у фізичному і психічному розвитку, синдром двостороннього або одностороннього атетоза. Крім того, у дітей, що вижили часто залишається жовто-зелене забарвлення молочних зубів і карієс в зв'язку з трофічних пошкодженням зубної емалі та дентину жовчними пігментами.
У дітей з жовтушною формою хвороби нерідко бувають геморагії на шкірі, мелена, гематурія в зв'язку з важким порушенням функції печінки (гіпопротромбінемія), системи згортання крові.
Нерідко жовтяниця виражена вже при народженні ребепка, тоді, як правило, навколоплідні води, первородна мастило і вартопов холодець пуповини також пофарбовані в жовтий колір.
Прогноз при таких ранніх клінічних проявах хвороби завжди серйозний зважаючи внутрішньоутробного початку хвороби. Під час пологів може бути розрив різко збільшених наренхіматозних органів дитини (печінки, селезінки).
Основною причиною смерті недоношених, померлих від гемолітичної хвороби в перші 24 години після народження, слід, по-видимому, вважати дегенеративні зміни в міокарді , а дітей, які загинули в більш пізні терміни (18-21-й день після народження), — цІРРОТІЧЕСКІЙ переродження печінкової паренхіми.
Діагноз жовтушною форми гемолітичної хвороби новонароджених часто буває нелегко встановити, особливо в ранні терміни розвитку хвороби, коли вона протікає приховано.
Захворювання діагностують на підставі точного обліку всіх даних: акушерського анамнезу, серологічного дослідження крові матері і дитини (резус і групова належність, титр резус-антитіл), клінічних проявів хвороби, даних обстеження дитини — гемограма, рівень білірубіну в динаміці.
Найбільшу діагностичну цінність має визначення рівня білірубіну в пуповіпной і периферичної крові. При утриманні білірубіну в пуповинній крові вище 3,5-4 мг ° / о, в венозної в першу добу життя дитини 9-10 мг ° / о і більше, на 2-й день — 14-15, а на 3-й — 18-20 мг% і вище слід діагностувати тяжку жовтяничну форму хвороби.
Важкість перебігу цієї форми знаходиться в прямій залежності від степопі гіпербілірубіномні. Чим вище уровепь білірубіну в крові, тому болипой небезпека розвитку ядерної жовтяниці. Ядерна жовтяниця — це основна причина смерті або інвалідності дітей з гемолітичною хворобою.
При важкій формі гемолітичної хвороби визначається білірубін і в сечі, проте уробплінурія спостерігається постійно, особливо в перші дні захворювання.
Температура тіла зазвичай нормальна, але іноді може короткочасно підвищуватися до 37,5-38 °.
жовтянична форма гемолітичної хвороби необхідно диференціювати насамперед з фізіологічної жовтяницею, так як дитина, народжена резус-негативної матір'ю, може бути здоровий навіть при наявності резус-конфлікту, і що спостерігається у нього жовтяниця в деяких випадках може бути фізіологічної.
Для останньої характерна поява жовтяничного забарвлення шкірних покривів лише на 2-3-й день життя і поступове його наростання. Але і не завжди жовтяницю, що з'явилася в перші 24 години після народження, слід вважати патологічної: ми спостерігали в першу добу життя поява желтушности у здорових доношених дітей, у яких в подальшому рівень білірубіну не перевищував 6-7 мг%, що відповідає показникам при фізіологічній жовтяниці.
У рідкісних випадках жовтяниця при гемолітичної хвороби вперше з'являється тільки на другу-третю добу.
при фізіологічній жовтяниці не буває збільшення печінки і селезінки, анемії, загальний стан дітей не порушено. Вона зазвичай проходить до 8-10-го дня, а жовтяниця при гемолітичної хвороби — набагато ноздпее, на 3-4-5-му тижні.
При вродженої атрезії жовчних ходів жовтяниця з'являється поздпо і впачале нічим не відрізняється від фізіологічної, різко посилюючись на 2-3-му тижні. Важливий симптом при атрезії жовчних шляхів — ахолічний кал, темна сеча. У цих випадках діти, як правило, гинуть через 4-5 міс після народження від вираженої печінкової недостатності і гіпотрофії.
Септическая жовтяниця зазвичай з'являється на 2-3-му тижні життя, до цього часу дитина вже встигає «закінчити» цикл фізіологічної жовтяниці. Жовтяниця при сепсисі різко виражена.
жовтяниця при інших інфекційних ураженнях новонароджених (цитомегалии, токсоплазмозі, природженому сифілісі) також обумовлена частково гемолизом еритроцитів, а також ураженням печінкової паренхіми. При цитомегалії жовтяниця нерідко з'являється рано, супроводжується анемією, еритробластозом, печінка і селезінка збільшені. Точній діагностиці допомагає наявність гігантських клітин з ядерними включеннями в осаді сечі, посмертно — в тканинах, а також відсутність серологічного конфлікту.
При природженому сифілісі жовтяниця виражена не різко, по часто відзначається гепатоспленомегалія. Для діагнозу важливо наявність ряду інших симптомів: сифілітичний нежить, тріщини губ, вроджена пухирчатка і інші зміни шкіри, сифілітичний остеохондрит.
Важка жовтяниця буває при гігантоклітинному гепатиті новонароджених, при галактоксеміі, іноді у новонароджених, народжених матерями, хворими на діабет .
Анемічна форма гемолітичної хвороби — найбільш легке захворювання серед інших форм цієї хвороби.
Захворювання починається на першому тижні життя дитини, іноді й пізніше. Звертає на себе увагу різка блідість шкіри і слизових, печінка і селезінка звичайно збільшені. Кількість еритроцитів різко знижений — до 2 000 000-2 500 000 в 1 мм 3 крові, гемоглобін нижче 40-50 од., Зазвичай має місце еритробластоз, ретикулоцитоз. Характер анемії — нормо-або гіпохромна, мікроцітарная. Зміни з боку лейкоцитарної форми зазвичай відсутні. Іноді анемія виникає поздпо — па 15-20-й день після народження (без попередньої жовтушною форми).
анемічного форму гемолітичної хвороби необхідно диференціювати з вродженою анемією внаслідок плодово-материнського кровотечі, діагностиці останньої допомагає відсутність серологічного конфлікту крові матері і дитини, виявлення значної кількості плодового гемоглобіну в материнській крові. Крім того, анемічну форму потрібно диференціювати з анемією внаслідок крововтрати при геморагічної хвороби новонароджених — мелене, а також з анемією, пов'язаної з перенесеним інфекційним захворюванням.
Лікування гемолітичної хвороби новонароджених
анемічного форму гемолітичної хвороби успішно лікують дробовими трансфузиями резус-негативної крові в поєднанні з вітамінами С, В], Вг, Be і препаратами заліза (після 1 міс життя) .
Абсолютно невиправданим виявилася пропозиція вводити всім новонародженим в пупкову вену ще в пологовому залі невелику кількість (30-50 мл) резус-негативної крові від резус-негативних донорів. Більшість дітей від матерів з резус-негативною приналежністю крові здорові і не потребують такого профілактичному заході. У разі важкого захворювання необхідно якомога раніше застосовувати більш активну терапію — заміну крові.
Дробові трансфузии резус-негативної крові або еритроцитарної маси не могли запобігти ураження мозку, печінки, нирок і тільки з введенням в практику замінних трансфузій крові (Wallerstein, 1946) летальність від жовтушною форми хвороби, за даними ряду авторів, значно знизилася — до 5-20%.
Але штучне переливання крові ефективно тільки при своєчасному застосуванні — не пізніш перших 36 годин після народження.
Основна мета заміни крові — видалення пошкоджених еритроцитів, які є джерелом токсичного білірубіну, а також видалення антитіл, непрямого білірубіну з крові і тканин. При гіпербілірубінемії, яка не супроводжується посиленим гемолізом, єдиною метою заміни крові є видалення непрямого білірубіну.
На підставі власного досвіду ми при заміні переливанні крові рекомендуємо вводити немовляті резус-негативну кров в кількості 150-180 мл / кг ваги дитини . Обсяг витягнутої крові повинен на 50-60 мл бути меншим загальної кількості введеної крові.
Все автори рекомендують для переливання резус-негативну свіжу цитратную кров не більше 3-4-дневцой давності. Потрібно переливати одногрунпную кров. При АВ0-конфліктної жовтяниці переливають еритромасу 0 (I) групи навпіл з плазмою АВ (IV) групи АБО одногруппной.
Показання до замепной трансфузии крові визначають в даний нремя, виходячи з рівня концентрації білірубіну в плазмі крові і швидкості його наростання. «Небезпечний» рівень білірубіну, при якому може розвинутися ядерна жовтяниця, становить 18-20 мг%.
Однак зміст білірубіну в першу добу рідко досягає 15-20 мг%, зазвичай така концентрація буває в крові на 2-3 -й і навіть 4-й день після рол {Депп, в той час як штучне переливання найбільш ефективно в перші 24 год життя. Рівень білірубіну в 8-10 мг ° / о в першу добу життя вже є показанням для замепного переливання крові.
За нашими даними, при швидкості наростання рівня білірубіну в сироватці крові більш ніж на 0,4-0,35 мг% в 1 ч слід діагностувати тяжку жовтяничну форму.
При високій концентрації білірубіну в пуповинної крові (більше 3,5-4 мг%) і наявності жовтяниці у дитини, рождепного імунізованих материо, необхідно негайно ж приступити до заміни крові.
Таким чином, головний показник для операції заміни крові при жовтушною формі гемолітичної хвороби — рівень білірубіну (більше 3,5 мг% в пуповинної крові, 8-10 мг% — в першу добу, 14-15 мг% — в другі, 18-20 мг% — па третій день життя).
у сумнівних випадках визначають рівень білірубіну 2 рази в депь і навіть трикратно.
Після проведення першого замінного переливання крові спостерігається «феномен рикошету », або віддачі, тобто вторинне підвищення рівня білірубіну, ступінь і тривалість якого дуже варіабельні. Вони залежать, головним чином, від запасів білірубіну в тканинах хворої дитини, а також від освіти нового білірубіну, швидкості зв'язування і виведення його печінкою.
При контролі ефективності замінних трансфузій (в сенсі заміни еритроцитів) шляхом визначення фетального гемоглобіну до і після трансфузии виявлено, що незважаючи на майже повне видалення пошкоджених еритроцитів тільки частина білірубіну виводиться з організму і надходження його з тканин в кров може тривати.
Якщо повторне наростання білірубіну в крові не дуже перевершує той рівень, який був до замінити трансфузии, через кілька годин після первинного підвищення білірубін плазми починає знижуватися, тоді можна відмовитися від другої замінити трансфузии. Якщо ж рівень білірубіну продовжує наростати, штучне переливання повторюють.
Будь-яка гіпербілірубінемпя у новонародженого може бути небезпечною і вимагає заміни крові в зв'язку з можливістю розвитку ядерної жовтяниці, показаннями для неї служать вищенаведені дані про критичний рівень білірубіну і його прирості.
У недоношених в зв'язку з більшою проникністю гематоепцефаліческого бар'єру і меншою способноечио крові утримувати білірубін (гіпопротеінемпя), ядерна жолтуха може виникати і при більш низькій концентрації білірубіну в плазмі. Небезпечним рівнем білірубіну в цих випадках вважають 14 мг% і вище. На думку деяких авторів, при щоденному добовому прирості білірубіну у недоношених дітей на 5 мг% слід думати про значне гемолизе і про можливість досягнення «небезпечного» рівня.
Замініть переливання найзручніше проводити через пупкову вену, катетерізіруя її, шляхом обнажеппя пупкової вени (метод Пінкус). За нашими даними, пупкова вена прохідна для катетера іноді і до 7-8-х діб. Можна робити заміну крові шляхом екссангвінаціі через променеву артерію або внутрішню підшкірну вену стегна, зовнішню яремну вену, а кров вводити через підшкірні вени голови.
Ускладнення при операції заміни крові нечасті. Може виникнути калієва інтоксикація (при використанні «старої» крові) з явищами сонливості, гіпотонії м'язів, змінами серцевої діяльності, судомами.
Ускладнення з боку серця бувають обумовлені перевантаженням правого серця (при швидкому проведенні операції). Можливо також охолодження дитини протягом операції внаслідок використання холодної крові, відсутність додаткового обігріву тіла дитини. Часті ускладнення — напади ціанозу, блювота.
І. Р. Зак (1960) досліджував насиченість крові киснем і не виявив суттєвої різниці в ній до і після заміни крові. Таким чином, ціаноз, мабуть, пов'язаний з циркуляторними розладами.
Профілактикою перевантаження правого серця є повільне введення крові малими порціями (по 10-12 мл). Як рідкісні ускладнення при цій операції описують емболію, тромбоз, аритмію, ацидоз, тромбоцитопенія, бактериемию, сироватковий гепатит.
Багаторазові заменпие трансфузии крові застосовують і для лікування набряку ферми гемолітичної хвороби в поєднанні з пункцією черевної порожнини для вилучення асцитичної рідини (до операції заміни крові).
При важкої жовтушною і набряку формах необхідно також боротися з інфекцією, метеоризмом. При ядерної жовтяниці, в зв'язку зі значними порушеннями лікворообігу, доцільні люмбальна пункція з лікувальною метою.
В даний час рекомендують поряд із заміною крові застосовувати плазмозамінники — неокомпенсан або гемодез, які, «фіксуючи» на себе білірубін, знижують його концентрацію в тканинах (А. Ф. Тур, Л. С. Персианинов, 1970) , пли низькомолекулярний полівінілпіролідон (по 8-15 мл / кг ваги в вену 1-2 рази на добу).
Доцільно також вводити 10% альбумін по 10-15 мл через день або одногруппную плазму в первия 3-4 дня захворювання, так як альбумін пов'язує непрямий білірубін і транспортує його в печінку.
Велике значення має глюкозотерапія: в перші 4-5 днів щодня вводять 20 мл глюкови (з 1 од. Інсуліну) або 30-40 мл 10% розчину внутрішньовенно,
В. Л. Таболин (1907) при синдромі згущення жовчі рекомендує застосувати грілку на область печінки або диатермию, 25% розчин машин сульфату всередину по 1 чайній лоіше 3 рази в день, лінокаін. Останній активізує жировий обмін, перешкоджає жировій дегенерації печепі. Призначають також калію оротат але 20-30 мг / кг ваги на добу протягом 10-14 днів.
При легкій жовтушною формі можна використовувати також фототерапию, білий або синє світло (1000 або 5000 лк) протягом 24-36 год. За даними І. Ірсовой (1971), експозиція протягом 8-12 год знижує білірубін на 3-4 мг%.
Від вигодовування материнським молоком в перші 9-11 днів слід відмовитися, так як присутність в жіночому молоці антитіл при изоиммунизации не підлягає сумніву. Дитину прикладають до грудей після негативного аналізу молока на антитіла під контролем біопроб: і точіння 3 дпей, прикладаючи дитину до грудей послідовно 1-2, 3-4 і все 6-7 годувань, щодня досліджують у нього содержапіе гемоглобіну та еритроцитів. При стабільності зазначених показників продовжують годування материнським молоком, при зниженні їх — знову переводять на годування донорським молоком.
При наявності в крові і молоці матері гемолизинов (АВО-конфлікт) від грудного годування доводиться зовсім відмовитися, так як цей вид антитіл довго зберігається в молоці і не руйнується при кип'ятінні.
Техніка операції заміни крові
Допорскую кров перед вве дением зігрівають в водяній бані протягом 20-30 хв (температура води не вище 36-37 °). Дитину перед операцією не годують щоб уникнути блювоти і зригування, сповивають його таким чином, щоб під час операції руки і поги були витягнуті і без листя. Живіт залишають відкритим. Шкіру живота і куксу пуповини дворазово обробляють спиртом і 2% розчином йоду. Операційне поле обкладають стерильними пелюшками. До паска дитини і з боків грудної клітки прикладають теплі грілки, загорнуті у фланелеві пелюшки.
Лікар і операційна сестра готуються до операції зі строгим дотриманням усіх правил асептики і антисептики. Операцію проводять в операційній або маніпуляційної кімнаті.
Дитину укладають горизонтально. Пуповину відсікають ножицями так, щоб її залишок мав довжину не більше 1,5, а краще 1 см від шкірного кільця. Отвір пупкової вени легко виявляють після розтягування і розправлення кукси двома пінцетами, зазвичай видно два маленьких білуватих кружечка (зрізи пупкових артерій) і одне велике отвір спавшейся пупкової вени з фестончастими краями, іноді з краплею крові.
До введення спеціального капронової катетера в пупкову вену вводять пуговчатий зонд на глибину 3-4 см для того, щоб намацати хід вени і випустити трохи крові зі згустками, які можуть закупорити катетер.
Негайно ж після вилучення пуговчатого зонда в пупкову вену вводять катетер, попередньо промитий 6% розчином цитрату натрію і фізіологічним розчином, на глибину 8. 10 см від шкірного кільця строго паралельно черевній стінці. Поблизу пупкового кільця його фіксує пінцетом асистент.
Введення крові через катетер поперемінно чергують з кровеізвлеченіем за допомогою 10-грамового шприца (у недоношених користуються 5-грама шприцом).
До введення донорської крові необхідно визначити групу крові в ампулі і зробити пробу на сумісність, для чого беруть сироватку крові дитини з першої витягнутої порції і краплю донорської крові з ампули.
Спочатку витягують 30-40 мл крові, а дале заміну виробляють так: вводять 12 мл крові за 2 хв, закінчивши введення, що не спимо шприц, роблять паузу (5-6 с) і потім витягають 10 мл крові за 1 хв. Знову вводять 12 мл і через 5-6 с витягають 10 мл і так далі протягом 1,5-2 ч. Після виливання кожної порції витягнутої крові шприц промивають 6% розчином цитрату натрію і фізіологічним розчином.
Введення і витяг крові виробляють дуже повільно, так як тільки при такому виконанні замінити траісфузіі видаляється велика кількість білірубіну, сенсибілізованих еритроцитів дитини і антитіл. Кількість введеної і виведеної крові враховують, записуючи на окремому аркуші, який додають до історії хвороби.
Після кожних 100 мл введеної крові в пупкову вену вводять 20 мл 20% розчину глюкози і 1,5-2 мл 10% розчину кальцію глюконату. При гіпокснческіх станах, особливо у недоношених, вводять 1-2 мл 5% розчину соди на початку операції і після кожних 100 мл крові. В кінці замінити трансфузии в пупкову вену вводять 100 000 ОД пеніциліну.
Першу і останню порції витягується крові направляють в лабораторію для визначення рівня білірубіну, що необхідно для контролю ефективності замінного переливання крові.
З другої половини операції дитині безперервно дають зволожений кисень, так як вводиться кров не оксігенізірована.
При інфузії і ексфузіі крові не повинно відчуватися ніяких перешкод і труднощів. В іншому випадку слід витягти катетер, промити його розчином цитрату натрію і фізіологічним розчином і прочистити мандреном від згустків.
У більшості випадків вводити кров легше, ніж витягувати. 15 тих випадках, коли на початку зксфузія і ііфузіі відбуваються добре, а в подальшому зксфузія але вдається, можна, переконавшись, що в вені немає згустків, ввести в пупкову вену 10-20 мл 20% розчину глюкози, це нерідко допомагає усунути тимчасовий спазм або спадання ієни.
Якщо під час заміни крові у дитини з'являються позиви на блювоту, неспокій, вичікують 2-3 хв перед введенням чергової порції крові. Після вилучення катетера накладають пов'язку, що давить.
Перші 3-4 дні після операції дитині з профілактичною метою вводять антибіотики (пеніцилін, оксацилін та ін.).
Відомо, що у дітей, які перенесли в періоді новонародженості важку гемолітичну жовтяницю, нерідко є важкі залишкові явища ураження центральної нервової системи, найчастіше полягають в різному ступені розумової і фізичної відсталості і симптомах ураження підкіркових гангліїв — атетоз, хореоатетоз, екстрапірамідна ригідність, церебральні паралічі.
Ми спостерігали в динаміці 128 дітей, які перенесли гемолітичну хворобу новонароджених (повторні огляди протягом 1-4 лот), для вивчення стану їх здоров'я і оцінки ефективності лікування. З них 102 дітей виробляли заменное трансфузии крові, а 26 осіб лікували дробовими трансфузиями крові з додаванням комплексу симптоматичних засобів. При цьому тільки у 9 (тобто в 8,8%) з 102 дітей, які лікувалися замінити трансфузиями крові, були остаточпие явища гіпербілірубіновой енцефалопатії. У той же час у 17 з 26 дітей, що страждали гемолітичною хворобою і ядерної я «елтухой і лікувалися дробовими трансфузиями крові, відзначалися виражені залишкові явища.
Клінічні прояви з боку нервової системи були поліморфними (атетоз, торзионная дістопія, епілептиформні синдром, дебільність), причому найбільш часто відзначалися торзионная дистонія і атетоз, що свідчать про ураження підкоркових гангліїв головного мозку.
Після виписки з акушерського стаціопара діти, які перенесли гемолітичну хворобу, перші 2-4 міс потребують особливо ретельного нагляду педіатра. Необхідно систематично проводити контроль стану червоної крові.
Пізня анемія розвивається майже у 2/3 дітей, які перенесли гемолітичну хворобу і лікувалися заміною крові, і є, можливо, пізнім проявом хвороби. Можна було б припустити, що має аченіе велика кількість перелитої крові, яка пригнічує на деякий час еритропоез. Але таке припущення не підтверджується, бо, як сказано вище, апемія розвивається не у всіх дітей, які перенесли операції »зпмепи крові, а лише у 2/3. Мабуть, пізня аіомія обумовлена триваючої циркуляцією антіерітроцітарпмх антитіл.
Крім анемії, у дітей, які перенесли гемолітичну хворобу, на першому році життя спостерігаються часті ааболоіапія, особливо респіраторні, майже у 25% відзначається ексудативний діатез. Тому на першому році життя профілактичні щеплення таким дітям треба проводити осторояшо, враховуючи індивідуальні особливості організму, наявність або відсутність симптомів ураження нервової системи, проявів ексудативного діатезу.
При виписці з акушерського стаціонару необхідно передати в дитячу консультацію повну виписку з історії хвороби дитини з детальними рекомендаціями щодо білоруського режиму годування, аеротерапії, терміни проведення аналізу крові і т. Д.
Профілактика гемолітичної хвороби новонароджених
В ранні терміни вагітності жінок слід обстежити на резус і групову приналежність крові. Якщо кров вагітної резус-негативна або О (I) групи, слід визначати в динаміці титр антирезус-антитіл (повних і неповних), а такя {е титр анти-А і анти-В антитіл. Всі вагітні з резус-негативною і 0 (1) групою крові повинні бути на обліку в жіночій консультації.
Особливої уваги потребують ті вагітні, у яких акушерський анамнез обтяжений (повторні викидні, мертвонародження, смерть попередніх дітей від жовтяниці) , а також вагітні, які одержували в минулому гемотерапію (внутрішньовенні або внутрішньом'язові влівапія крові).
Сенсибілізація до резус-аптнгену особливо висока при імунізації кров'ю, при цьому антитіла можуть зберігатися протягом усього життя у високому титрі. Рекомендується визначати титр антитіл в крові вагітної еялемесячно в перші 6 міс вагітності і кожні 2 тижні — в наступному. Можна проводити і непряму реакцію Кумбса з сироваткою крові матері (якісна реакція на наявність антитіл).
У деяких клініках досліджують навколоплідні води, отримані трансабдомпнальним шляхом, на білірубін і антитіла задовго до пологів (Л. С. Персианинов, 1974 ).
В останні роки з'явилися повідомлення про можливість сенсибілізації організму вагітної до Rh-антигену і антигенів системи АВО (Шауер і Куліх) при штучному перериванні вагітності в 8-9 тижнів, так як при цьому елементи плодового яйця, що містять антігепи, можуть проникати в кровоносне русло матері і імунізувати її.
При відсутності резус-антитіл рекомендується проводити неспецифічну десенсибилизацию під час вагітності.
При наявності в крові, крім неспецифічної десенсибілізації, антирезус-аптітел в титрі вище 1: 16 можна виробляти часткові заменное трансфузии резус-негативної одногруппной, спеціально підібраною донорської крові в кількості 250-300 мл, попередньо випустивши крові на 50 мл менше, останню збирають і передають на станцію переливання крові для виготовлення стандартних сироваток-антирезус.
При повторному наростанні титру антитіл часткові заменное трансфузии вагітним з резус-негативною кров'ю можна виробляти кілька разів (В. Є. Дашкевич). Вони сприяють деякому зниженню сенсибілізації вагітної до резус-антигену, так як нопіжается титр резус-антитіл в крові.
Є вказівки на возмоншость десенсибілізації вагітних шляхом трансплантації шкірного клаптя від чоловіка.
Для профілактики резус імунізації після перших пологів в останні роки застосовують імунний антирезус — у-глобулін в дозі 3-5 мл внутрімишечпо в перші 48-72 годин після пологів, який руйнує резус-позитивні еритроцити плоду, що проникли в материнський кровотік під час пологів.
Вагітних з резус-негативною кров'ю необхідно госпіталізувати за 2-3 тижнів до передбачуваного терміну пологів і проводити їм глюкозо-кисневу терапію, а також призначати полівітаміни. При наростанні титру антитіл слід викликати пологи за 2-4 тижні до терміну. Показанням для цього є стан плода.