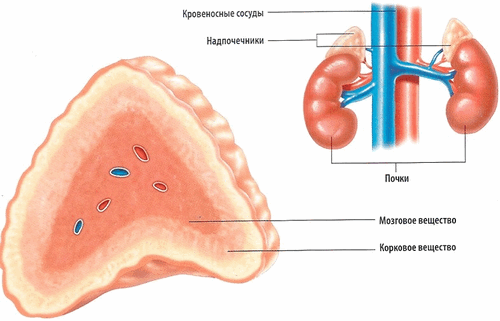
Маса обох наднирників у дорослої людини — близько 14 г. Кожна з залоз має 2 чітко розмежовані частини — внутрішній мозковий і зовнішній корковий шар. Кора наднирників є джерелом стероїдних гормонів декількох видів. Ці біологічні речовини регулюють багато метаболічні процеси в організмі і впливають на активність нервової, імунної, серцево-судинної систем. Функціональна недостатність кори надниркових залоз ставить під загрозу життя пацієнта.
Гормони кори надниркових залоз
У корі виділяють 3 шари. Вони відрізняються по мікроскопічній будові і виконуваної функції.
Самий верхній шар називається клубочковий. Його утворюють щільні округлі структури із залозистої тканини. У клубочковом шарі переважно синтезуються мінералокортикоїди. Основний гормон цієї групи — альдостерон. Мінералокортикоїди є життєво необхідними для організму.
Наступний шар — пучковий. Під мікроскопом ця зона виглядає тканиною з безлічі радіально спрямованих тяжів. Цей шар досить масивний. У ньому синтезуються життєво важливі речовини — глюкокортикоїди. Основний гормон цієї групи — кортизол.
Найбільш внутрішній шар кори — сітчастий. У ньому тяжі з ендокринних клітин розташовуються хаотично, переплітаються між собою. Цей шар досить тонкий. Продукт сітчастого відділу кори надниркових залоз — статеві стероїди (слабкі андрогени).
Все стероїдні гормони виробляються з їх попередника — холестерину. У клітинах надниркових залоз безперервно йдуть послідовні реакції перетворення одних проміжних речовин в інші і синтез кінцевих продуктів (гормонів).
Регуляція роботи наднирників
Робота кори надниркових залоз частково регулюється гіпофізом і гіпоталамусом. У центральних відділах ендокринної системи виробляються кортикотропин-рилізинг-фактор і адренокортикотропіну (АКТГ).
гормонів тропів впливає переважно на пучкову зону кори надниркових залоз. Також доведено вплив цього біологічно активної речовини на сітчастий шар. В результаті АКТГ підвищує синтез кортизолу і андрогенів.
Клубочковая зона кори надниркових залоз функціонально не залежить від гіпофіза і гіпоталамуса. Залізисті клітини цього шару реагують на концентрацію електролітів у плазмі крові. Активність вироблення мінералокортикоїдів визначається ренінангіотензинової системою. Чим більше концентрація реніну, тим більше гормонів виробляє клубочковая зона кори.
Функція надниркових залоз в організмі
Функція кори надниркових залоз складається з діяльності її шарів.
Мінералокортикоїди клубочкового шару підтримують водно-сольовий баланс. Альдостерон і його аналоги впливають на нирки. Гормони цього типу викликають підвищення затримки натрію в організмі і посилюють виділення калію з сечею. Альдостерон також затримує хлориди і рідина. Все це призводить до підвищення об'єму циркулюючої крові. Мінералокортикоїди підтримують нормальний артеріальний тиск і перешкоджають зневоднення.
Глюкокортикоїди виконують істотно більший набір функцій. Ці гормони беруть участь у всіх видах обміну речовин в організмі людини.
Дія кортизолу і його аналогів:
- підсилюють катаболізм (розпад) білків,
- пригнічують утворення нових білків,
- підсилюють перетворення тригліцеридів ,
- підвищують рівень цукру в крові,
- стимулюють секрецію інсуліну,
- знижують чутливість клітин до інсуліну,
- підвищують жироотложение (переважно по абдоминальному типу),
- підвищують чутливість тканин до катехоламінів (адреналіну і норадреналіну),
- підвищують збудливість нервової системи,
- покращують чутливість сенсорних органів,
- підвищують системний артеріальний тиск,
- затримують воду в організмі,
- збільшують концентрацію натрію в плазмі,
- зменшують число лімфоцитів, базофілів і еозинофілів в крові,
- пригнічують запалення,
- пригнічують проникність судин,
- пригнічують імунітет.
Глюкокортикоїди — гормони стресу. Вони допомагають організму адаптуватися до різких змін у навколишньому середовищі. Підвищення концентрації цих біологічно активних речовин сприяє стійкості до надмірних подразників. Глюкокортикоїди пригнічують алергію. Також саме ці гормони регулюють циркадний рівень температури тіла. Пік викиду стероїдів в кров сприяє передранкового зниження продукції тепла.
Андрогени сітчастої зони кори надниркових залоз не є життєво важливими. Однак ці гормони грають важливу роль в дитячому віці у чоловіків і протягом усього життя у жінок.
Ефекти андрогенів надниркових залоз:
- стимулюють окостеніння епіфізарних хрящів,
- підвищують синтез білка в кістковій, м'язовій тканині та шкірі,
- формують у жінок лібідо,
- підсилюють ріст волосся в андроген- областях.
Недолік гормонів наднирників
Недостатність кори надниркових залоз формується через припинення роботи ендокринних клітин.
Виділяють первинну і вторинну .
Первинна форма розвивається через ураження самих периферичних залоз. Кора може бути зруйнована в результаті різних факторів. Найбільш часто захворювання провокує аутоімунне запалення і інфекційний процес (наприклад, туберкульоз). Також залозиста тканина може загинути через тромбозу, крововиливи, зростання пухлини і т. Д. Крім того, первинна гостра надниркова недостатність формується в результаті радикального лікування (операція з видалення залоз).
Вторинна недостатність виникає через припинення синтезу АКТГ в гіпофізі. Це може бути наслідком ішемії, тромбоемболії, травми і т. П. Також і лікування аденом гіпофіза часто призводить до зниження рівня гормонів тропів крові.
За швидкістю появи симптомів виділяють:
- гостру форму,
- хронічну недостатність.
Гостра надниркова недостатність характеризується дуже швидким розвитком. Всі ознаки захворювання з'являються протягом кількох годин або днів. Симптоми вкладаються в картину аддісоніческій криз. Причиною гострої форми є різке припинення роботи кори надниркових залоз.
Хронічна недостатність розвивається поступово. Часто це захворювання протікає приховано.
За тяжкості проявів патологію ділять на:
- компенсовану,
- субкомпенсовану,
- декомпенсированную.
Сильний стрес може різко погіршити стан хворого. У разі травми, інфекції, хірургічного втручання іноді відбувається виражене посилення всіх симптомів. В результаті розвивається загострення — аддісоніческій криз.
Прояви гострої форми недостатності
Практично у всіх хворих з аддісоніческій криз спостерігаються нудота, блювота, діарея і біль в області живота. У критичних випадках ураження шлунково-кишкового тракту приймає форму геморагічного гастриту і ентериту. Ця патологія імітує картину сильного шлункової кровотечі.
Також пацієнти скаржаться на сильну м'язову слабкість. Стомлюваність так сильна, що хворому складно стояти і ходити.
Крім того, гостра надниркова недостатність супроводжується порушеннями роботи серця і психічними відхиленнями.
Криз часто проявляється сильним зниженням артеріального тиску. Тонус судин різко падає. Спостерігається зниження об'єму циркулюючої крові. Тиск дуже складно стабілізувати навіть за допомогою стандартної протишокової терапії. Аддісоніческій криз не можна купірувати адреналіном.
Психічні відхилення дуже різноманітні. Іноді лікарі помилково діагностують психоз, церебральну кому, токсичний синдром.
Симптомом гострої недостатності кори може бути:
- загальмованість,
- оглушення,
- кома,
- галюцинації ,
- маячня і т. д.
залежно від того, які симптоми переважають, аддісоніческій криз ділять на кілька форм: серцево-судинний, абдомінальний, нервово-м'язовий , психічний.
Ознаки хронічної надниркової недостатності
Симптоми з'являються у тих пацієнтів, чия кора наднирників зруйнована на 80-90%. Також ознаки хвороби є у пацієнтів з різким пригніченням синтезу АКТГ (більш 70-90% від норми).
Симптоми пов'язані з дефіцитом глюкокортикоїдів і мінералокортикоїдів. Причому при вторинній формі недостатності спостерігаються тільки ознаки зниження вироблення глюкокортикоїдів.
Недостатність надниркових залоз хронічної форми проявляється:
- слабкістю,
- стомлюваністю,
- зниженням витривалості,
- зниженням м'язової сили,
- апатією,
- зниженням системного артеріального тиску,
- зниженням рівня цукру крові,
- зменшенням маси тіла,
- порушеннями травлення.
При первинній недостатності спостерігається ще й:
- гіперпігментація шкіри і слизових,
- зміна смакових пристрастей (тяга до солоного),
- сильна гіпотонія,
- зменшення росту волосся на лобку і під пахвами.
Ці прояви виникають через атрофії клубочкового і сітчастого шару.
Діагностика

Гостра надниркова недостатність діагностується за даними огляду пацієнта, бесіди з ним або його близькими. Також для точного встановлення захворювання потрібні аналізи крові. В першу чергу інформативно визначення концентрації кортизолу. Якщо картина аддісоніческій криз супроводжується пригніченим рівнем гормону (менше 20 мкг / 100 мл), то ймовірність гострої форми недостатності кори практично 100% -а. Крім того, роблять проби на АКТГ, калій, натрій, кислотно-лужну рівновагу. Зазвичай діагностику цього захворювання проводять лікарі швидкої допомоги або реанімаційного відділення.
частіше виявляється лікарями в поліклініках. Пацієнти звертаються з характерними скаргами до терапевтів, гастроентерологів, ендокринологів, кардіологів, гінекологів та ін.
Недостатність кори надниркових залоз в хронічній формі вимагає комплексної діагностики.
Проводять:
- УЗД або томографію наднирників,
- томографію гіпофіза,
- клінічний аналіз крові,
- дослідження кортизолу і АКТГ крові,
- оцінку добового ритму кортизолу і АКТГ,
- дослідження сечі за добу на кортизол і 17-ОКС,
- визначення електролітів крові (калій, натрій, хлориди),
- визначення pH.
Також про причини первинної надниркової недостатності можна судити по тесту на антитіла до антигену 21-гідроксилази.
Крім того, іноді потрібні спеціальні стимуляційні проби (з інсуліном або АКТГ). Ці діагностичні тести дозволяють визначити рівень ураження (гіпофіз або самі наднирники).
Лікування гострої форми захворювання
Лікування аддісоніческій криз вимагає максимальної оперативності. Чим раніше буде надана допомога, тим краще прогноз для життя і здоров'я.
Терапія включає введення:
- фізіологічного розчину,
- 5-40% -го розчину глюкози,
- гідрокортизону або преднізолону (внутрішньовенно ),
- антибіотиків або й інших симптоматичних засобів.
Гостру недостатність кори надниркових залоз лікують за особливою схемою. Спочатку використовують максимальну дозу гормонів. Потім поступово знижують обсяг введеного розчину. Через кілька днів пацієнта переводять на таблетки.
Лікування хронічної недостатності
Якщо у пацієнта виявлена хронічна недостатність кори надниркових залоз, то лікування включає корекцію гормонального дефіциту і ліквідацію причини захворювання.
Для придушення хворобливого процесу, який спровокував гіпокортіцізм, може знадобитися антибактеріальне лікування туберкульозу, сифілісу, протигрибкові засоби. Також іноді потрібні операції (видалення пухлин або аневризм) і променева терапія (онкологічний процес).
Навіть якщо причина недостатності кори усунена, дефіцит гормонів може зберегтися. Хронічна форма захворювання зазвичай вимагає довічної замісної терапії.
Лікування первинної недостатності включає мінералокортикоїди і глюкокортикоїди. Терапію контролюють за клінічними проявами. Враховують показники артеріального тиску, загальне самопочуття, м'язову силу, динаміку маси тіла, наявність гіперпігментації і шлунково-кишкових розладів.
Вторинна надниркова недостатність коректується тільки препаратами глюкокортикоїдів. Лікування мінералокортикоїдами не потрібно.
Якщо у пацієнта планується хірургічне лікування або виникає запалення, терміново потрібно підвищити дози гормональних препаратів (в 2-5 разів). Цей захід знімає ризик загострення (маніфестації аддісоніческій криз).
Пацієнтам з низьким рівнем рекомендовано особливе харчування. Раціон повинен бути багатий білками, жирами і вуглеводами, натрієм, вітамінами. Обмежують споживання продуктів з високим вмістом калію.
Гіпокортицизм (надниркових залоз)
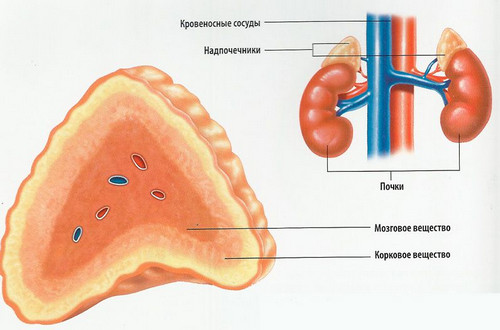
 Кора наднирників складається з 3 шарів, що відрізняються за будовою і функціями. У зовнішньому (клубочковом) шарі виділяються мінералокортикоїди. Ці гормони відповідають за водно-сольовий баланс, підтримують об'єм циркулюючої крові та артеріальний тиск. Найсильніший минералокортикоид — альдостерон.
Кора наднирників складається з 3 шарів, що відрізняються за будовою і функціями. У зовнішньому (клубочковом) шарі виділяються мінералокортикоїди. Ці гормони відповідають за водно-сольовий баланс, підтримують об'єм циркулюючої крові та артеріальний тиск. Найсильніший минералокортикоид — альдостерон.
В середньому (Пучкова) шарі виробляються глюкокортикоїди. Ці біологічно активні речовини відносяться до життєвоважливі для організму.
Глюкокортикоїди впливають на:
- рівень системного артеріального тиску,
- концентрацію цукру крові,
- обмін ліпідів і білків,
- запальні реакції при,
- активність центральної нервової системи.
Основний природний гормон цієї групи - кортизол. Саме дефіцит глюкокортикоїдів призводить до розвитку важкої патології - гострої або хронічної .
У самому внутрішньому шарі кори (сітчастому) синтезуються статеві стероїди. Тут утворюються слабкі андрогени, що впливають на обмін речовин, сексуальний потяг, зовнішність. Статеві грають велику роль в дитячому віці у хлопчиків і на протязі всього життя у жінок. Їх недолік позначається на самопочутті та метаболізмі, але не загрожує життю.
Роботу кори надниркових залоз регулює цілий ряд механізмів. Синтез минералокортикоидов підпорядковується сигналам ренінангіотензинової системи. На пучкову і сітчасту зони великий вплив мають гормони тропів гіпофіза. В першу чергу має значення концентрація адренокортикотропіну (АКТГ). Це біологічно активна речовина виділяється в кров під контролем кортиколиберина гіпоталамуса.
У роботі надниркових залоз простежується чіткий добовий ритм. В передранкові години різко зростає виділення в кров кортизолу та інших глюкокортикоїдів. У вечірні години концентрація цих гормонів мінімальна. Циркадний ритм дозволяє кортизолу готувати організм до настання нового дня. Завдяки передранкового піку людина прокидається з відносно високим рівнем глікемії. Крім того, кортизол пригнічує реакції запалення і алергії. Під час голоду або хвороби ці ефекти гормону допомагають організму вижити.
Класифікація гипокортицизма
Дефіцит глюкокортикоїдів та інших гормонів наднирників може сформуватися через ураження залозистої тканини кори, гіпофіза або гіпоталамуса.
Відповідно виділяють:
- первинний гіпокортицизм (патологія надниркових залоз, немає синтезу кортизолу),
- вторинний гіпокортицизм (патологія гіпофіза, немає синтезу АКТГ),
- третинний гіпокортіцізм (патологія гіпоталамуса, немає синтезу кортиколиберина).
Для діагностики рівня ураження застосовують лабораторні аналізи і спеціальні проби. На практиці лікарям досить складно диференціювати третинний і вторинний. Обидва ці стани протікають без порушення водно-електролітного балансу. В обох випадках низький АКТГ поєднується з мінімальною концентрацією кортизолу (і його аналогів).
За швидкістю розвитку клінічної картини гіпокортіцізм буває гострим і хронічним.
Гострий розвивається стрімко і завжди супроводжується важкою симптоматикою. У хворих можуть бути ознаки порушень роботи нервової системи, шлунково-кишкового тракту, мускулатури. У всіх випадках гострого гипокортицизма у пацієнтів виявляють загрожує життю падіння артеріального тиску.
Хронічний гіпокортіцізм розвивається повільно. Тривалий час цей стан залишається в стадії компенсації. Симптоми захворювання турбують хворого, але не загрожують його життю. При несприятливому розвитку подій хронічна патологія може проявлятися кризом. В такий момент відбувається декомпенсація захворювання. Організм не справляється з дефіцитом гормонів. Зазвичай кризового погіршення самопочуття буває пов'язано з супутніми захворюваннями і травмами.
Причини появи недостатності кори надниркових залоз
Первинний гіпокортицизм виникає в більшості випадків через аутоімунного запалення. Клітини кори піддаються агресії з боку захисних сил організму. Поступово більша частина тканини руйнується і перестає виконувати свою функцію. Причини аутоімунного ураження наднирників вивчені недостатньо.
Інші причини первинного гипокортицизма:
- туберкульоз (при ураженні 90-100% обсягу залозистої тканини),
- обмінні порушення (гемахроматоз, амілоїдоз, саркоїдоз),
- крововилив або ішемія,
- онкологічна пухлина,
- метастази раку іншої локалізації в обидва наднирника,
- наслідки опромінення радіацією,
- наслідки хірургічного втручання на надниркових залозах.
Третинна і вторинна недостатність надниркових залоз може розвиватися идиопатически. В цьому випадку причини патології невідомі.
З діагностованих причин частіше знаходять:
- післяпологовий некроз гіпофіза (синдром Шихана),
- черепно-мозкові травми,
- доброякісні або злоякісні пухлини,
- ішемію або крововилив,
- обмінні порушення.
Однією з найбільш частих причин гипокортицизма є раптова відміна гормональних препаратів. Ятрогенна недостатність кори з'являється у відповідь на припинення лікування глюкокортикоїдами. В основі такої реакції - пригнічення синтезу АКТГ в гіпофізі. Секреція адренокортикотропіну пригнічується за принципом зворотного зв'язку. Якщо лікування препаратами тривалий і масивне, то з часом може розвиватися атрофія кори надниркових залоз.
Прояви первинної форми захворювання
Первинна форма поєднує симптоматику нестачі глюкокортикоїдів і мінералокортикоїдів.
Ранніми ознаками патології вважають:
- сильну слабкість (особливо у вечірні години),
- зниження ваги,
- погіршення апетиту на тлі порушень травлення,
- зниження цифр артеріального тиску.
Через деякий час до перерахованих ранніх ознак приєднуються зміни смакових пристрастей, епізоди гіпоглікемії і психічні порушення.
Симптоми розгорнутої форми хвороби:
- пігментація шкіри (швидше за все темніють природні складки і місця тертя),
- головні болі,
- непритомність при різкому вставанні,
- депресія,
- пристрасть до солоної їжі,
- порушення в статевій сфері.
Ознаки вторинного гипокортицизма
Якщо порушення в роботі кори пов'язані з дефіцитом адренокортикотропіну, то в клінічній картині немає симптомів дефіциту альдостерону. Ось тому ознаки вторинного і третинного гипокортицизма включають тільки слабкість, гіпотензія, зниження маси тіла. Ця форма захворювання менш важка, ніж первинна. Пацієнти відзначають погіршення самопочуття, але в цілому їх стан залишається стабільним.
Вторинний гіпокортицизм ніколи не супроводжується гіперпігментацією шкіри і слизових.
Лікування надниркової недостатності
Для того щоб поліпшити самопочуття пацієнта, нормалізувати метаболізм і артеріальний тиск, потрібно замісна гормональна терапія.
При первинній формі захворювання хворому призначають препарати, що містять аналоги минералокортикоидов і глюкокортикоїдів.
Доза підбирається на підставі:
- цифр артеріального тиску,
- динаміки маси тіла,
- роботи шлунково-кишкового тракту,
- загального самопочуття.
При вторинному і третинному Гіпокортицизм досить замісної терапії аналогами кортизолу. Препарат титрують, враховуючи клінічні прояви.
Для того щоб уникнути кризового погіршення стану, всім хворим з хронічною недостатністю кори рекомендують профілактичне збільшення дози (на 50-100%) під час стресів, хірургічних втручань і захворювань.
Лікування гипокортицизма в гострій формі проводиться лікарями реанімації. Гормональні засоби в перші кілька днів вводять ін'єкціями. Тільки потім пацієнта переводять на таблетовані форми.
Усі хворі з гіпокортицизмом повинні перебувати на диспансерному обліку і регулярно проходити обстеження в ендокринолога.
Гостра надниркова недостатність (гострий гіпокортіцізм)
Гострий дефіцит може стати причиною загибелі пацієнта. Це стан відносять до вкрай важким. Під час кризу організм відчуває виражений дефіцит глюкокортикоїдів. Недолік цих життєво важливих біологічних речовин провокує судинний колапс, порушення свідомості, різку слабкість і адинамию.
Етіологія
Гостра найчастіше буває наслідком погіршення хронічної форми хвороби. В цьому випадку патологія кори існує тривалий час, але компенсується за рахунок резервних можливостей організму і лікування. Потім після впливу емоційного стресу, інфекційного запалення, хірургічного втручання або інших факторів відбувається зрив адаптаційних можливостей. В результаті самопочуття пацієнта різко погіршується, посилюються всі симптоми гипокортицизма, приєднуються ознаки ураження серцево-судинної, травної, нервової систем. Також надниркованедостатність може з'явитися первинно в гострій формі. Так відбувається при різкому руйнуванні залозистої тканини кори.
Причини гострого гипокортицизма:
- крововилив в тканину надниркових залоз,
- ішемія надниркових залоз,
- травма,
- адреналектомія,
- декомпенсація при хронічній формі,
- скасування препаратів глюкокортикоїдів (при неендокріннимі патології).
Наднирковозалозна недостатність у дітей може маніфестувати ще в період новонародженості. Причиною патології буває апоплексія через родову травму і інфекційних процесів. Крім того, вроджена дисфункція кори може виявитися гострим дефіцитом глюкокортикоїдів.
Ятрогенний гострий гіпокортіцізм — серйозна проблема у всіх медичних спеціальностях. Глюкокортикостероїди активно використовуються для придушення запальних реакцій. Синтетичні аналоги кортизолу призначають при алергіях і аутоімунних процесах. Зазвичай дози глюкокортикоїдів в таких ситуаціях набагато вище фізіологічних. Курс лікування може бути досить тривалим і інтенсивним. Якщо препарати синтетичних гормонів будуть скасовані різко, то у пацієнта вірогідний розвиток гипокортицизма. Це відбувається через придушення штучними аналогами секреції природних гормонів. Блок на вироблення власного кортизолу не може бути знятий моментально. Щоб відновити синтез природних гормонів, потрібно скасовувати таблетки поступово. Щоб повністю прибрати середню терапевтичну дозу без ризику для здоров'я, потрібно до 4-8 тижнів.
Ще один вид ятрогенного гипокортицизма — гостра після двосторонньої адреналектомія. Також дефіцит гормонів може бути після видалення єдиного надниркової залози (наприклад, якщо другий атрофовані).
Класифікація гострого гипокортицизма
У клінічній картині у різних пацієнтів переважають симптоми ураження серця, центральної нервової системи, травного тракту .
Відповідно виділяють 3 основні форми:
- серцево-судинна,
- шлунково-кишкова,
- нервово-психічна.
У всіх хворих спостерігають головний біль, зниження апетиту, нудоту, падіння рівня тиску.
Далі приєднуються більш важкі симптоми:
- різка слабкість,
- адинамія,
- озноб,
- біль в області живота,
- підвищення температури тіла,
- багаторазова блювота,
- зневоднення,
- прискорений пульс,
- прогресуюче зниження тиску.
Якщо гостра надниркова недостатність розвивається через крововилив у наднирники, то всі симптоми з'являються швидко і яскраво. У багатьох пацієнтів з'являється петехіальний висип на шкірі.
Діагностика гострого гипокортицизма
Життя хворого багато в чому залежить від того, як швидко буде встановлений правильний діагноз.
Хвороба може бути запідозрений:
- якщо у пацієнта в анамнезі є дані на хронічний первинний або вторинний гіпокортицизм,
- якщо відомо про травми черевної порожнини,
- якщо гострий стан з'явилося після операції на наднирниках.
Медикам доводиться проводити диференційну діагностику гипокортицизма з цілим рядом інших захворювань.
Гостра надниркова недостатність іноді протікає під маскою:
- гострих хірургічних патологій,
- інфаркту або інсульту,
- міопатії,
- целіакії,
- порфірії,
- синдрому Пархона,
- синдрому Фанконі,
- інтоксикації свинцем,
- гиперпаратиреоза,
- депресії,
- шизофренії,
- психозу,
- анорексії.
Діагностичні тести не проводяться. Якщо це можливо, то у хворого беруть кров на експрес-аналіз кортизолу, альдостерону, адренокортикотропіну. Також виконують дослідження електролітів плазми (калій, натрій та ін.).
Діагностика надниркової недостатності також підкріплюється вимірюваннями сечовини і залишкового азоту крові, глікемії, кислотно-лужної рівноваги. Крім того, всім пацієнтам виконують електрокардіографію.
Лікування гострої форми гипокортицизма

Перша доба — вирішальні для прогнозу по життю і здоров'ю пацієнта. У ці 24 години лікарі виконують протишокові заходи і вводять гормональні препарати (мінералокортикоїди, глюкокортикоїди).
У схемі терапії на 1 місці знаходяться великі дози стероїдних препаратів. Медикаменти вводять ін'єкційно. Зазвичай поєднують внутрішньовенну інфузію і внутрішньом'язові уколи. Це дозволяє швидко отримати лікувальний ефект і створити депо гормонів в організмі.
Також застосовують:
- розчини глюкози (для підвищення цукру крові),
- розчини натрію хлориду (для подолання зневоднення),
- адреналін, мезатон (для підвищення тиску),
- аскорбінову кислоту (для підтримки центральної нервової системи),
- антибіотики (якщо є інфекційне запалення),
- симптоматичне лікування (в залежності від причини гипокортицизма).
За першу добу може бути введено 300-500 мг (і навіть більше) гідрокортизону. Надалі пацієнта переводять на внутрішньом'язовіін'єкції і зменшують дозу в 3-5 разів. У міру стабілізації стану ін'єкційні форми замінюються на таблетки. Первинна гостра недостатність надниркових залоз протікає особливо важко. Пацієнтам потрібні великі дози стероїдів, що поєднують глюкокортикоидную і мінералокортикоїдної активності.
Лікування гострої надниркової недостатності передбачає обов'язкову профілактику повторних кризів. Якщо це необхідно, то пацієнтів навчають правилам зміни доз замісної гормональної терапії.
Прогноз при гострій недостатності кори надниркових залоз зазвичай сприятливий. Якщо лікування розпочато відразу ж, то стан стабілізується в найближчі кілька днів. Якщо діагноз не встановлений і терапія не проводиться, то ризик загибелі хворого — до 50%. Найчастіше причиною смерті стає серцева недостатність.
Гипопитуитаризм або як «болить» гіпофіз
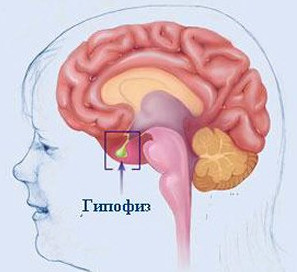
Гипопитуитаризм — це захворювання головною ендокринної залози — гіпофіза, точніше, її передньої долі (аденогіпофіза), пов'язане зі зниженням функції.
Механізм розвитку патології
Безперервна робота ендокринних залоз по синтезу специфічних гормонів відбувається «під керівництвом» і наглядом центральної залози — гіпофіза. Вона продукує «тропів» гормони завдяки яким активізується робота інших «периферичних» залоз. Крім того, через гіпофіз здійснюється зв'язок з командами з центральної нервової системи. Для цього є подкорковая зона, яка називається гіпоталамус. У ній нервові клітини згруповані в ядра за принципом контролю за різною діяльністю організму.
Ці клітини реагують на концентрацію хімічних і біологічних речовин в крові, що притікає: якщо вони визначають недолік або надлишок чогось, то дають команду гіпофізу про необхідної корекції, а гіпофіз передає уточнений «наказ» конкретним ендокринних залоз-виконавцям. Гипопитуитаризм викликає зрив налагодженої системи, тому що при цій патології виникає недостатність або зовсім відсутнє виробництво «керівних» . Оскільки це порушення не протікає без відома гіпоталамуса гіпоталамо-гіпофізарна недостатність вважається основним патологічним механізмом гіпопітуїтаризму.
З метою уточнення провідної причини в діагностиці прийнято виділяти:
- первинний гіпопітуїтаризм — коли є точні докази порушень в гіпофізі, знижується концентрація всіх шести або одного з продукуються гормонів,
- вторинний гіпопітуїтаризм — якщо головним фактором служить патологія центральної нервової системи, що передається через гіпоталамо-гіпофізарну недостатність.
Основні причини
Причинами поразки передньої долі гіпофіза можуть бути:
- доброякісні або злоякісні пухлини,
- розвиток специфічного процесу при хронічних інфекційних захворюваннях (туберкульоз, сифіліс),
- черепно-мозкові травми,
- запальні хвороби мозку,
- прояви судинних порушень при атеросклерозі артерій головного мозку з ішемією в гіпоталамо-гіпофізарної зоні,
- саркоїдоз, розростання рубцевої тканини,
- хвороби крові,
- виражені аутоімунні захворювання,
- хвороби ,пов'язані з порушенням обміну речовин в організмі (тривале голодування, цукровий діабет, наслідки хронічної ниркової і печінкової недостатності),
- вроджені відхилення в розвитку гіпофіза.
Одна з причин раніше була добре знайома акушерам: в результаті важких патологічних пологів наступав некроз передньої долі гіпофіза. Згодом формувалася хвороба Симмондса (при повному некрозі) або хвороба Шиена (при неповному).
Клінічні прояви
Симптоми гіпопітуїтаризму проявляються, якщо в робочому стані залишається 1/10-я частина клітин гіпофіза. Хвороба може розвиватися довго, поки не досягне критичного рівня. Гіпоталамо-гіпофізарна недостатність починається з проявів дефіциту гонадотропного гормону, який відповідає за розвиток статевих залоз. Якщо хвороба починається в дитячі роки, то в підлітковому віці формується евнухоподобний тип фігури, сповільнюється кістковий зростання, затримується статевий розвиток.
У дорослої людини відсутня статевий потяг, м'язова тканина замінюється жировою, у чоловіків випадає волосся на обличчі, в пахви, атрофуються яєчка. У жінок зменшуються молочні залози, зникають менструації, атрофуються статеві органи.
Недостатність соматотропного гормону проявляється у дітей в зупинці росту, у дорослих в наростаючій м'язової слабкості, болях в серці, підвищеної стомлюваності від невеликої фізичного навантаження.
Дефіцит тиреотропного гормону в дитячому організмі є частою причиною уповільненої фізичного і розумового розвитку, а у дорослих викликає (зниження функції щитовидної залози), що проявляється в слабкості, низький артеріальний тиск, рідкісному пульсі, захворюваннях шлунка і кишечника.
Пухлини гіпофіза при гіпопітуїтаризмі викликають головні болі, порушення зору, втрату нюху.
Дуже рідко хвороба виникає раптово. Клінічно це проявляється в різких інтенсивних головних болях, втрати свідомості, погіршення зору, зниження артеріального тиску.
Хвороба Симмондса (гіпофізарна кахексія) в даний час зустрічається дуже рідко. Чітка система спостереження за вагітними жінками веде до своєчасного виявлення та лікування будь-яких відхилень. 100 років тому характерні симптоми хвороби Симмондс пов'язав з некротичними змінами в передній долі гіпофіза.
Суть хвороби можна висловити, як різке схуднення і старіння в післяпологовому періоді. Жінка значно втрачає вагу, шкіра стає старою і зморшкуватою, випадають і кришаться зуби, волосся. Психічні зміни включають повну байдужість, втома, сонливість, втрату пам'яті, галюцинації. З боку інших органів виявляються розлади шлунка і кишечника, падіння артеріального тиску, атрофія статевих ознак. В даний час хвороба може виявлятися не настільки запущеній, але окремі симптоми знайомі гінекологів.
Діагностика
 Гипопитуитаризм можна виявити за допомогою лабораторних аналізів. Вивчається концентрація в крові тропних гормонів гіпофіза і їх відповідність гормонального синтезу периферичних залоз. Якщо буде виявлено знижений рівень і тих і інших — це вірна ознака, таким чином проявляється гіпоталамо-гіпофізарна недостатність.
Гипопитуитаризм можна виявити за допомогою лабораторних аналізів. Вивчається концентрація в крові тропних гормонів гіпофіза і їх відповідність гормонального синтезу периферичних залоз. Якщо буде виявлено знижений рівень і тих і інших — це вірна ознака, таким чином проявляється гіпоталамо-гіпофізарна недостатність.
Особливий вид діагностики — перевірка реакції на введення тестових препаратів, здатних викликати активацію синтезу гормонів.
зниження соматотропного гормону побічно позначається на кістковому скелеті. Є спеціальні таблиці відповідності показників окостеніння віком. Враховуються параметри тіла, статеві ознаки.
Недостатність адренокортикотропного гормону може бути тимчасовим явищем, вона пов'язана із застосуванням в терапії різних захворювань великих доз глюкокортикоїдів.
Пухлиноподібні освіти гіпофізу виявляються на рентгенограмі черепа зі спеціальною укладанням пацієнта або при магніторезонансної томографії.
лікування
терапія гіпопітуїтаризму в першу чергу потребує усунення причини хвороби і відшкодування відсутніх гормонів тропів.
При пухлинах проводиться курсова променева терапія, можливо оперативне лікування. При запальному або судинному процесі потрібна масивна терапія антибіотиками, специфічними засобами при туберкульозі і сифілісі, судинні препарати для відновлення кровопостачання в гіпоталамо-гіпофізарної зоні.
Лікування гормональними препаратами призначається після виявлення рівня зниження своїх гормонів.
Одночасно проводиться симптоматична терапія для корекції викликаних змін.
Сучасна діагностика і лікування дозволяють уникнути важкого ступеня гіпопітуїтаризму. Особливе значення надається обстеження дітей, щорічної диспансеризації школярів.
Гіпофізарний нанізм (гіпофізарна карликовість)
гіпофізарний нанізм — захворювання, викликане недостатнім виробленням соматотропного гормону в передній долі гіпофіза, порушенням його якісного складу або несприйнятністю тканин до гормону. Терміни синоніми — «гипофизарная карликовість» і «мікросомія».
Статистика показує різну поширеність хвороби в світі: в Америці, Азії та Африці один випадок на 4000 населення, в Росії в 5 разів рідше. Однак, будь-яких расових або національних причин не виявлено. Відомо, що особи чоловічої статі хворіють в два рази частіше, ніж жінки.
Патологічний механізм хвороби
Вивчення зв'язків продукції соматотропного показало, що індукувати патологію може гіпоталамус.
Нормальний процес виглядає так: гіпоталамус виділяє стимулюючий гормон, у відповідь передня частка гіпофіза синтезує і викидає в кров соматотропний гормон (СТГ), він надходить в печінку і тканини і викликає активну продукцію інсуліноподібний фактор росту № 1 (ІПФР-1), в результаті збільшується кількість пластичних (будівельних матеріалів) і відбувається зростання кісткового скелета, формуються м'язи.
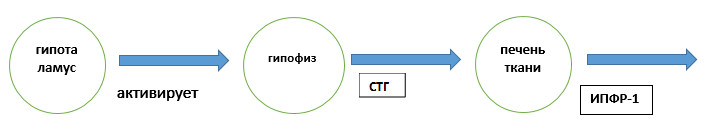
Зрив цього ланцюжка на будь-якому етапі призводить до гіпофізарний нанізм.
Причини
Основною причиною гіпофізарний нанізм вважається спадковість. Це доводиться народженням в одній сім'ї дітей, які згодом стали карликами. Однак існують і інші причини:
- пухлини гіпофіза або гіпоталамуса з виборчим порушенням продукування соматотропного гормону або декількох гормонів,
- родові травми головного мозку новонародженого,
- лейкоз в дитячому віці,
- наслідки променевої терапії.
Критерії зростання
Встановлено, що при нормальному розвитку дитина повинна рости на 7-8 см на рік, при гипофизарном нанізмі відзначається зростання тільки на 3-4 см. Відповідно відставання від однолітків буде проявлятися вже в дошкільному віці. Критеріями карликовості вважається верхня межа зростання для чоловіків 130 см, для жінок 120 см.
Симптоми і клінічні прояви
Ендокринологи налічують близько 60 різновидів карликовості.
- гіпофізарний нанізм у дітей виявляється в дошкільному віці, коли батьки і лікарі помічають затримку росту малюка в порівнянні з однолітками приблизно на 2 роки. П'ятирічна дитина виглядає як трилітка.
- При вродженої карликовості тіло дитини розвивається і виглядає пропорційним, але руки, ноги, голова значно менше, ніж повинні бути за віком.
- Характерні дрібні «лялькові» риси обличчя з довгими віями, виступаючим лобом, невеликим провалом перенісся.
- Все органи також відстають у рості, у юнаків недорозвинення яєчок, у дівчат затримка або відсутність місячних.
- Через нерозвинену гортані голос високий, пронизливий.
- можливо зайве відкладення жиру на тулубі.
- Турбує загальна слабкість, при розвитку пухлини гіпофіза головні болі з нудотою, блювотою і порушенням зору (двоїння в очах).
- Характерно поведінка хворих на гіпофізарний нанізм: вони уразливі, примхливі, замкнуті, вимагають захисту, через наявність одночасного дефіциту тиреотропного гормону вчаться погано. Існують форми захворювання, для яких характерний розвиток повного ідіотизму.
- Хворі бездітні, хоча створюють сім'ї.
- У дорослому віці шкіра швидко старіє, що проявляється безліччю зморшок на обличчі.
Зовнішні ознаки хвороби іноді плутають з геміфаціальной мікросомії. Це інше спадкове захворювання, яке проявляється ізольованим порушенням росту кісток лицьового скелета, вушних раковин, неба, скул і щелеп. Воно проявляється вже в грудному періоді. Особа асиметрично за рахунок сглаженности кута вилиці з одного боку, різко порушений прикус. Дитині важко ковтати і жувати. Геміфаціальний мікросомія виявляється при огляді ортодонта (лікарі приймають в дитячій стоматологічній поліклініці).
Це захворювання не пов'язано з . Воно виникає у плода в перші місяці вагітності в результаті неправильного закладання кісткового паростка. Лікування проводиться до 16-18 років, поки не зупиниться зростання кісткової тканини. Дитині з геміфаціальной мікросомії потрібне тривале носіння встановлених на щелепи скоб, пластичні операції особи. Для батьків визначається ризик повторного народження дітей з подібною патологією в 2%.
Діагностика
При диспансерному огляді педіатри проводять вимірювання параметрів зростання. Відзначають темп зростання в порівнянні з попереднім періодом. При виявленні відставання дитина прямує до ендокринолога.
Один із способів діагностики — рентгенограма кисті. За характером розвитку кісткової тканини можна встановити відхилення від необхідних вікових змін.
Визначення гормонів тропів в крові біохімічними методиками дає характерну картину їх зниження. Крім того, проводять тести на введення провокуючих чинників з метою з'ясування можливостей гіпофіза по синтезу гормонів тропів.
Рентгенограма «турецького сідла» (кісткове утворення, на якому лежить гіпофіз) і магнітно-резонансна томографія допомагають виявити збільшення передньої долі гіпофіза.
Лікування гіпофізарний нанізм
Харчування хворих повинно містити досить білка і вітамінів, бути енергетично повноцінним.
Лікувальна тактика вимагає повного обстеження хворих. При наявності пухлини проводиться променева терапія, хіміотерапія, оперативне втручання за вказівкою лікаря.
З метою відшкодування відсутніх гормонів дитині починають введення штучних чинників зростання. Американські лікарі вважають, що в такий терапії потребують? від усіх народжених немовлят і широко застосовують тривалий метод компенсації.
Введення препаратів з соматотропного гормону проводиться щодня до закінчення формування кісткового скелета. Ця ознака виявляється на рентгенограмі. Якщо процес уже завершений, ефекту від лікування гормоном росту не буде.
Додатково призначаються анаболічні засоби, вітаміни. Якщо діагностується загальна недостатність гіпофіза (гипопитуитаризм) в лікування додаються всі необхідні фактори.
Ефективна терапія призводить до збільшення зростання в перший рік на 10-15 см, в подальшому темп зростання знижується до 2 см в рік.
Прогноз
Прогноз сприятливий за відсутності пухлини і ранньому початку лікування. Хоча досягти достатнього зростання рідко вдається. Оточуючим слід ставитися до дитини не як до малюка, а в відповідно до його фактичного віком. Потрібно пам'ятати, що найчастіше інтелектуальні можливості не знижені. Маленька людина з гіпофізарний нанізм в змозі опанувати посильної професією.
Адіпозогенітальная дистрофія, ожиріння при дистрофії
Адіпозогенітальная дистрофія відноситься до групи не просто ендокринної патології, а нейроендокринної. Хлопчики частіше страждають на це захворювання.

У механізмі розвитку захворювання точно встановлена початкова роль гіпоталамуса, підкіркового центру регуляції ендокринної системи. У зоні гіпоталамуса зібрані групи нервових клітин, об'єднаних в ядра. Кожне ядро «керує» і контролює певні види діяльності організму, посилаючи сигнали в гіпофіз про виробництво гормонів тропів.
відповідно до «наказом» гіпофіз синтезує 6 тропних гормонів в передній долі і 2 в задній. Гормони тропів направляються кожен до своїх цільовим ендокринних залоз і регулюють таким чином вироблення остаточних гормонів, що сприяють життєзабезпечення організму людини.
Синдром захворювання адипозогенітальною дистрофії викликаний головним больовою точкою в гіпоталамусі. Результатом порушень є ураження ядер, що відповідають за статевий розвиток і обмін речовин, зниження вироблення гормонів лютропина і фоллитропина.
Причини
Причини адипозогенітальною дистрофії проявляються в дитячому або в юнацькому віці, але утворитися вони можуть внутрішньоутробно і залежать від стану здоров'я майбутньої матері.
- Будь-які перенесені вагітною жінкою інфекційні захворювання ведуть до одночасного важкого ураження плода (токсоплазмоз, грип, бактеріальні інфекції).
- Інтоксикацію плода з руйнуванням ядер гіпоталамуса здатні викликати прийом алкоголю, куріння, вплив промислових отруйних речовин.
- Важкі ускладнення дитячих інфекційних захворювань з поширенням на головний мозок і оболонки викликають менінгіти, енцефаліти, арахноїдити .
- Родові травми головного мозку із залученням зони гіпоталамуса.
- Доброякісні і злоякісні пухлини мозку.
Адіпозогенітальная дистрофія є придбаним захворюванням, спадковість тут не має значення.
Клінічні прояви
Адіпозогенітальная дистрофія виявляється при диспансерному огляді дітей з значного перевищення ваги.
- Зайве відкладення жирової тканини спостерігається на животі, грудях, стегнах, особі.
- Підвищений апетит, цей синдром отримав назву «булімії» або «вовчого голоду».
- У хлопчиків в підлітковому віці при захворюванні виявляється гінекомастія (набухання молочних залоз), крипторхізм (затримка опускання яєчка в мошонку), недорозвинення статевого члена.
- Дівчата, які страждають адипозогенітальною дистрофією, відстають від ровесниць у формуванні молочних залоз, у них не з'являються менструації.
- Підлітки не мають вторинних статевих ознак (оволосіння на лобку, в пахвових западинах).
- Юнаки з адипозогенітальною дистрофією тривалий час зберігають дитячий голос, не відбувається мутації.
- Підлітки мають високий зріст, подовжені непропорційно руки, великі стопи.
- Порушено формування суглобів: через слабкі зв'язок формується зайва рухливість в розгинанні, підлітки часто отримують вивихи, підвертають стопу.
- Одна з ознак адипозогенітальною дистрофії — плоскостопість.
- Ближче до дорослого періоду у юнаків виявляють відсутність зростання бороди і вусів, у дівчат атрофію зовнішніх і внутрішніх статевих органів.
- Відзначається сухість шкіри, схильність до інфікування.
- З боку органів травлення синдром адипозогенітальною дистрофії виражається в порушенні вироблення шлункового соку і жовчі, у дітей схильність до закрепів.
- реакція серцево-судинної системи на зайву вагу і порушення харчування міокарда — рання миокардиодистрофия, м'язові клітини замінюються на слабкі сполучнотканинні, серце не здатне досить повноцінно працювати, що проявляється патологічними явищами (підвищення артеріального тиску, аритмія).
- При адипозогенітальною дистрофії не страждає інтелект, розумовий розвиток дітей відповідає віку.
Діагностика адипозогенітальною дистрофії
Батьки не повинні радіти зайвої повноті малюка. Це не показник здоров'я, скоріше навпаки. Зайва вага — один з початкових симптомів в загальному синдромі такого захворювання, як адипозогенитальная дистрофія. Якщо педіатр направляє дитини до ендокринолога на обстеження, батьки повинні обов'язково його раду.
Лікар-ендокринолог після огляду порекомендує провести аналізи крові на специфічні гормони, цукор крові.
Для виключення хвороб центральної нервової системи необхідний огляд невролога.
Доктора обов'язково будуть розпитувати матір дитини про період вагітності, вона повинна чесно розповісти про всі порушення. Перед лікарями стоїть завдання виключення спадкових форм ожиріння.
Лікування захворювання
 З метою зниження ваги при адипозогенітальною дистрофії призначається дієта, що обмежує вміст жирів і вуглеводів. Дитині заборонені солодощі, тістечка, мед, білий хліб, жирне молоко, вершки, сметана, насичені бульйони і супи, макаронні вироби, фастфуд, чіпси, газована вода. Рекомендується дробове харчування до шести разів на день, м'ясо переважно нежирних сортів, курка, овочеві тушковані блюда, молочні вироби зі зниженою жирністю, овочі і несолодкі фрукти.
З метою зниження ваги при адипозогенітальною дистрофії призначається дієта, що обмежує вміст жирів і вуглеводів. Дитині заборонені солодощі, тістечка, мед, білий хліб, жирне молоко, вершки, сметана, насичені бульйони і супи, макаронні вироби, фастфуд, чіпси, газована вода. Рекомендується дробове харчування до шести разів на день, м'ясо переважно нежирних сортів, курка, овочеві тушковані блюда, молочні вироби зі зниженою жирністю, овочі і несолодкі фрукти.
При необхідності захворювання вимагає препаратів, що пригнічують апетит.
Заняття фізичним навантаженням потрібно починати з ранкової зарядки, рекомендується плавання.
При виявленні залишкових явищ перенесеного інфекційного захворювання дитині проводиться курс антибіотиків, противірусного лікування.
У разі зв'язку Адіпозогенітальная синдрому з пухлиною мозку призначається відповідне лікування: променева терапія, хіміотерапія, оперативне втручання.
Обов'язково рекомендуються лікарські препарати, що покращують роботу мозкових центрів гіпоталамуса.
Питання про доцільність замісної гормональної терапії при адипозогенітальною дистрофії вирішується не раніше 12 -річного віку підлітка:
- хлопчикам спочатку призначається гонадотропін, а до 16 років вводяться статеві гормони,
- дівчаткам проводиться курсове лікування естрогенами в поєднанні з прогестероном для формування менструального циклу.
Прогноз захворювання сприятливий, в гіршому випадку з дитини сформується євнух, який не має потомства. При своєчасному лікуванні хворі живуть повноцінним життям, можуть бути встановлені обмеження щодо виконання важкої фізичної роботи.
нецукровий діабет
Терміном «нецукровий діабет» називається ендокринне захворювання, що характеризується появою у людини спраги і діурезу більше 2 літрів сечі на добу, що не супроводжується підвищенням в крові концентрації глюкози. Стан може розвиватися як внаслідок порушення центральної регуляції сечоутворення , так і в результаті патології приймають сигнали ниркових структур. Симптоми хвороби мають деякі відмінності у жінок, дітей і чоловіків. Лікування патології обов'язкове, так як збільшені обсяги добової сечі сильно змінюють водно-сольовий баланс, що позначається на всіх органах.
Анатомія і фізіологія коротко
 Нирки — дуже важливий парний орган. Вони виводять з організму токсини, продукти білкового, жирового і вуглеводного обмінів, вони виробляють гормони і речовини, що стимулюють утворення клітин крові в кістковому мозку. Але найголовніша функція — підтримання водно-сольового і кислотно-основного балансів, при зміні основних параметрів яких страждає стан всіх внутрішніх органів і можуть статися летальні зміни.
Нирки — дуже важливий парний орган. Вони виводять з організму токсини, продукти білкового, жирового і вуглеводного обмінів, вони виробляють гормони і речовини, що стимулюють утворення клітин крові в кістковому мозку. Але найголовніша функція — підтримання водно-сольового і кислотно-основного балансів, при зміні основних параметрів яких страждає стан всіх внутрішніх органів і можуть статися летальні зміни.
Основна структурна одиниця нирки — нефрон. Він складається з клубочка і канальців. Всі ці структури тісно пов'язані з кровоносною системою. Щоб зрозуміти, як запускається нецукровий діабет, розглянемо етапи утворення сечі:
- У клубочке нирки відбувається відфільтровування крові: великі білки (вони потрібні для підтримки в крові онкотичного тиску, утримуючи на собі рідину в посудині) і клітини крові йдуть назад в русло, рідина крові з розчиненими в ній більш дрібними речовинами проходить в клубочки.
- Біля канальців нирки знаходяться кровоносні судини. Канальці, «звіряючи» зміст різних речовин в надійшла до них рідини і в крові, «вирішують» що віддавати назад (ці речовини всмоктуються в судини), а що виводити. Деякі речовини, які для організму некорисні, виводяться незважаючи на їх концентрацію. Канальці ж повертають і більшу частину потрапила до них рідини в кров: так, її надходить близько 150 літрів на добу, виділяється же всього близько 1,5 літрів.
- Коли все, що потрібно, повернулося в судини, що залишилася рідина (її трохи) з речовинами надходить у систему мочевиведенія. Це називається секрецією.
Діяльність нирки регулюється не стільки змістом в крові різних речовин, скільки рівнем таких гормонів, як:
- Ренин, який виробляється самою ниркою. Він посилює зворотне всмоктування натрію і води з канальців в судини, підвищуючи тим самим артеріальний тиск,
- Вазопрессин (АДГ, антидіуретичного гормону), синтезованого в гіпоталамусі — маленької залозі в порожнині черепа, яка є головним «диригентом» всіх гормональних процесів в організмі. Рівень АДГ в нормі регулюється концентрацією в крові натрію: чим його більше, тим більше і гормону. Також рівень вазопресину знижується при зменшенні концентрації реніну. Суть дії цього гормону — зменшення кількості виділеної на добу сечі.
- Є й інші гормони, що регулюють роботу нирок, але в контексті даної теми їх розглядати не будемо.
Види захворювання
Залежно від рівня ураження нецукровий діабет буває:
- Центрального генезу. Захворювання зазвичай розвивається внаслідок зниженого синтезу вазопресину в гіпоталамусі. Також центральний нецукровий діабет може розвинутися, якщо АДГ виробляється в нормальній кількості, але гіпофіз — друга головна ендокринна залоза, розташована біля гіпоталамуса і отримує команди безпосередньо від нього — не виділяє весь гормон в кров.
- Нирковий: вазопресину синтезується нормальна кількість, але нирки на нього не реагують належним чином.
- Функціональний нецукровий діабет: розвивається у деяких дітей до року в результаті недостатньої зрілості нирок і підвищеної активності того ферменту, який руйнує вазопресин.
- У вагітних жінок — в результаті підвищеного вироблення плацентою одного з ферментів, що руйнує антидіуретичний гормон.
- Первинна полидипсия: внаслідок спраги, що розвивається внаслідок психічного захворювання або патології головного мозку у жінок або чоловіків ( дуже рідко — дітей) пригнічується синтез . Якщо така людина втратить багато рідини і не встигне її заповнити, синтез гормону відновиться.
- Ятрогенний: такий нецукровий діабет розвивається внаслідок неправильного прийому сечогінних препаратів (зазвичай для самолікування).
Причини захворювання
Причини нецукрового діабету відрізняються в залежності від виду захворювання:
1. Нефрогенна форма діабету розвивається:
- у дітей — внаслідок вродженого порушення будови ниркових рецепторів до вазопресину,
- у дорослих — через таких причин:
виділення через нирки багатою глюкозою сечі (при цукровому діабеті),
обмінних порушень,
хронічній нирковій недостатності,
стану, яке виникає після тривалої закупорки сечоводу каменем,
безконтрольного прийому деяких препаратів.
2. Центральний нецукровий діабет також може бути вродженим і набутим:
- вроджена форма захворювання проявляється у дітей внаслідок:
дефекту гена, що відповідає за вироблення вазопресину,
синдрому, що передається у спадок, який включає в себе не тільки ураження нирок, а й атрофію диска зорового нерва, і розвиток цукрового діабету II типу,
порушень розвитку мозку у внутрішньоутробному періоді,
- причини набутого нецукрового діабету наступні:
наслідки перенесеного грипу або інших гострих респіраторних вірусних,
операції на головному мозку,
пухлини гіпофіза або гіпоталамуса,
енцефаліт,
черепно-мозкова травма,
нейросифилис,
метастази в гіпофіз,
саркоїдоз,
ІПМ,
туберкульоз,
гистиоцитоз,
ураження мозку цитомегаловірусом або токсоплазмой (це зазвичай захворювання, що з'являються у внутрішньоутробному періоді, проявляються у дітей),
порушення будови судин, що живлять гіпоталамо-гіпофізарну зону.
пролактинома
Доброякісна пухлина з локалізацією в області передньої частини гіпофіза, що характеризується підвищеною здатністю виробляти пролактин, позначається терміном пролактінома. Серед всіх різновидів пухлинних утворень гіпофіза дана різновид зустрічається досить часто. Пролактинома набагато частіше утворюється у жінок фертильного віку, проте в деяких випадках виявляється в організмі чоловіків. Жіноча пролактінома часто досягає в розмірах всього кілька міліметрів, чоловіча ж пролактінома може бути понад 1 см діаметром.
Пролактин — активна речовина (, стимулюючий продукцію грудного молока. У нормі він виробляється не тільки у жінок, але і у представників чоловічої статі, проте в малій кількості. Пролактин, фолікулостимулюючий і лютеїнізуючий регулюють статеву і дітородну функції. В організмі у жінок дані гормони гіпофіза впливають на вироблення естрогену. У чоловічому організмі — забезпечують оптимальну рухливість сперматозоїдів і синтез тестостерону.
Гиперпролактинемия (надлишкова продукція пролактину) призводить у жінок до безпліддя і ановуляції (частіше при мікроаденоме). В організмі чоловіка пролактінома може викликати розвиток гінекомастії, порушення еректильної функції або порушення сексуального потягу.
Причини виникнення пролактиноми у жінок (мікроаденома) або у чоловіків не встановлені.
Незважаючи на це, у деяких хворих даним захворюванням виявлені генетичні порушення у вигляді неоплазии (ендокринного походження). Такі патології можуть супроводжуватися гиперсекреторной активністю підшлункової або паращитовидной залоз, можливо, гіпофіза або пептичнимивиразками. Не виключається також спадковий тип розвитку (пролактиноми).
Класифікація
- Мікропролактінома (інтраселярна) - мікроаденома (менше 1 см діаметром), що не перевищують розміри турецького сідла,
- макропролактиномами (екстраселлярная) - макроаденома (понад 1 см діаметром), перевищують розміри турецького сідла.
Відповідно до розмірів пролактиноми (макро- або мікроаденома) відрізняється клінічна симптоматика, лікування.
Симптоматика даної патології
Симптоми даної патології обумовлюються зайвої виробленням пролактину, компресійним дією (здавленням прилеглих тканин) пухлинного освіти.
Часто макропролактіноми викликають симптоми порушення зорової функції очних нервів. Це можуть бути такі симптоми пролактиноми як: утруднене диференціювання бічних об'єктів, звужені поля зору, двоїння предметів в очах. У разі компресії пухлинних освітою перехрещення зорових нервів може виникати сліпота.
Пролактинома великих розмірів може викликати симптоми, обумовлені здавленням тканини головного мозку. Симптоми порушення роботи центральної нервової системи можуть бути представлені головними болями, тривогою, депресією, дратівливістю.
Пролактинома великих розмірів також порушує вироблення інших гормонів гіпофіза, так як здавлює тканину аденогипофиза.
Ознаки пролактиноми у жінок
На початкових стадіях розвитку пролактиноми перші ознаки у жінок - це порушення менструального циклу у вигляді опсо-, оліго- або аменореї. На тлі цієї патології вироблення лютеїнізуючого і веде до неможливості овуляції і зачаття.
Також характерні симптоми пролактиноми - це підвищення рівня пролактину - галакторея (вироблення молока) незалежно від вагітності (при її відсутності ). Галакторея часто може викликати виникнення мастопатії.
Гиперпролактинемия може також викликати остеопороз внаслідок вимивання з кістки мінеральних компонентів. Внаслідок цього у жінок зустрічається підвищена крихкість кісток. Дефіцит естрогенів призводить до затримки води в організмі. Розвиток пролактиноми може супроводжуватися Гиперандрогения синдромом, як наслідки цього виникають вугрі, можливий гірсутизм. У жінок в більшості випадків зустрічається мікроаденома.
Ознаки даної патології у чоловіків
У чоловіків пролактінома викликає зниження вироблення тестостерону, патологію сперматогенезу. Як наслідок цієї патології проявляються безпліддя, зниження потенції, порушення статевого потягу. Часто спостерігається гінекомастія у представників сильної статі, можливо, з галактореей. До всього іншого спостерігаються на тлі розвитку пролактиноми атрофічні зміни яєчок, остеопороз, зниження росту волосся на шкірі обличчя, а також слабкість в м'язах.
У чоловіків в більшості випадків зустрічаються пролактиноми макротип.
Діагностика
Найбільш достовірним діагностичним методом дослідження, що дозволяє виявити і підтвердити діагноз пролактінома (макро- або мікроаденома), є МРТ з контрастуванням, націлені на обстеження гіпофіза. Характерно, що МРТ дозволяє виявити як макроаденом, так і Мікроаденому будь-якої локалізації.
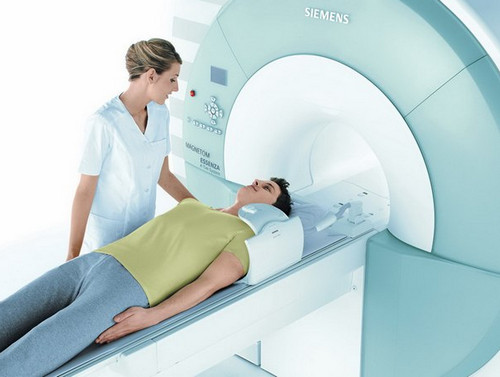
У разі великої пролактиноми частіше призначають КТ області головного мозку, що пояснюється хорошою візуалізацією підстави турецького сідла, в якому зазвичай розташовується гіпофіз.
Серед лабораторних досліджень відіграють роль для постановки діагнозу аналіз рівня пролактину в крові. Діагноз пролактиноми підтверджується при рівні даного гормону вище 9,1 нмоль / л (або вище 200 нг / мл). Нормальні значення пролактину у чоловіків - до 15 нг / мл, у жінок - до 20 нг / мл.
При отриманні за результатами дослідження рівня пролактину в межах 40-100 нг / мл (або 1,8-4,5 нмоль / л) необхідно виключити: вагітність, травматичне ушкодження грудної клітини, гіпотиреоз, печінкову і ниркову недостатність , патологічну функціональність гіпоталамо-гіпофізарної системи, а також можливе застосування медикаментів, що викликають вироблення пролактину.
Показовий також спеціальний тест із застосуванням тиролиберина. У разі наявності скарг на зорову систему рекомендується огляд офтальмологом. Виняток остеопорозу проводиться денситометрії.
Лікувальна тактика
Лікування пролактиноми має бути спрямоване на нормалізацію рівня вироблення гормону. Лікувальна тактика та вибір схеми терапії пролактиноми визначається ендокринологом. Лікування пролактиноми включає такі медикаменти як: бромкриптин, перитол, лізурид, леводопа, достинекс, ципрогептадин. Лікування даними препаратами дає позитивний ефект досить часто, мікроаденома малих розмірів на тлі лікування можуть зникнути. Доцільне лікування веде до наступних ефектів: відновлюється фертильність, менструації у жінок, вироблення тестостерону, відновлення тестостерону у чоловіків.
Лікування контролюється томографією пухлинного освіти в динаміці. При неефективності лікування або великих розмірах пухлини показано оперативне лікування.
У деяких випадках можливе лікування із застосуванням променевої терапії. Ефект від цього методу в терапію, формується після закінчення декількох років. У молодих жінок, які планують вагітність, таке лікування не використовують. Пролактинома і вагітність несумісні, однак фертильність відновлюється.
Пацієнта, з перенесеною пролактиномою, навіть якщо проведене лікування було ефективним, ставлять на диспансерний облік. Щорічно ця група людей повинна підлягати КТ, консультації офтальмолога, і 2 рази в рік - визначення рівня вмісту пролактину. При виявленні рецидиву показано вторинне лікування.
Синдром гіперпролактинемії у чоловіків
 Гормон, який виробляє гіпофіз, називається — пролактин. Він відповідає за репродуктивну функцію організму. За рахунок нього відбувається утворення яйцеклітин і сперматозоїдів. Найчастіше захворювання вражає жінок, але і чоловіків стикаються з цією проблемою. Пік захворюваності приходить на 25-40 років. Гиперпролактинемия у чоловіків призводить до порушень функцій статевої системи і безпліддя.
Гормон, який виробляє гіпофіз, називається — пролактин. Він відповідає за репродуктивну функцію організму. За рахунок нього відбувається утворення яйцеклітин і сперматозоїдів. Найчастіше захворювання вражає жінок, але і чоловіків стикаються з цією проблемою. Пік захворюваності приходить на 25-40 років. Гиперпролактинемия у чоловіків призводить до порушень функцій статевої системи і безпліддя.
Причини гіперпролактинемії
в крові може бути короткочасним, наприклад рівень гормону збільшується уві сні, після занять фізичною культурою або після прийому білкової їжі. Але це підвищення є фізіологічним і не приносить шкоди організму.
Більш тривалий за часом підвищення гормону в крові можна визначити за допомогою аналізу крові. До причин відносять:
- прийом деяких лікарських препаратів (нейролептики, антидепресанти, оральні контрацептиви, кокаїн, нудоти кошти та інші),
- захворювання ендокринної системи — полікістоз яєчників, гіпотиреоз, хронічний гепатит, оперізуючий лишай, хронічна ниркова недостатність,
- інфекційні захворювання — менінгіт, туберкульоз та інші,
- пухлини гіпоталамуса,
- хвороби гіпофіза.
Ознаки гіперпролактинемії
Перші ознаки, які можуть вказувати на захворювання — це слабкість, різка зміна настрою, різкий набір ваги, випадання волосся. Ознаки хвороби наростають поступово, дуже часто чоловіки не звертають належної уваги на зниження потенції, так як думають, що причиною всьому втому. Іноді навіть лікарі можуть помилково ставити невірний діагноз. Для того щоб поставити правильний діагноз необхідно здати аналіз крові на гормони. Чим довше захворювання протікає без лікування, тим більше симптомів з'являється у людини:
- відсутність статевого потягу,
- збільшення молочних залоз,
- виділення молока або молозива з грудей,
- головний біль,
- зниження зору,
- безпліддя,
- депресія,
- збільшення яєчок,
- остеопороз.
До якого лікаря звернутися при появі симптомів захворювання?
гІПЕРПРОЛАКТИНЕМІЄЮ або гінеколог-ендокринолог. Тільки лікар зможе дати об'єктивну оцінку стану пацієнта, призначити йому необхідні аналізи, а потім правильне лікування.
Лікування
Для того щоб вилікувати гіперпролактинемію необхідно для початку встановити її причину. Тільки після цього лікар приступає до комплексної терапії захворювання. Щоб в крові лікарі призначають антагоністи дофаміну. Ці лікарські препарати знижують пролактин в крові і тим самим відновлюють репродуктивні функції. Антагоністи дофаміну добре переносяться хворими і в 95% випадках не викликають побічних ефектів. До таких препаратів відносять:
- Парлодел,
- Каберголін,
- Норпролак.
Призначення цих лікарських засобів повинен проводити тільки лікар. Не варто займатися самолікуванням.
Прогноз і профілактика
Захворювання можна повністю вилікувати — головне вчасно почати лікування. Більш того, вже під час лікування нормалізується репродуктивна функція і з'являється можливість завагітніти. Також не варто забувати про хвороби, яка спровокувала підйом пролактину. Це захворювання також потребує контролю і лікуванні.
При появі перших ознак захворювання — головний біль, збільшення маси тіла, погіршення зору і зниження статевого потягу — варто звернутися до лікаря. Ці ознаки говорять про те, що у вашому організмі стався гормональний збій. Не затягуйте з походом в поліклініку і не займайтеся самолікуванням — це може погіршити перебіг захворювання.
гігантизм
Терміном «гігантизм» називають стан, що виникає внаслідок підвищеного вироблення в організмі гормону росту — соматотропіну, що характеризується надмірним зростанням людини (зазвичай вище 2 метрів). При цьому захворюванні тулуб, кінцівки і голова збільшуються практично пропорційно, є також порушення функцій репродуктивних органів і центральної нервової системи.

гігантизм — хвороба , яка розвивається у дітей і підлітків, коли зони росту на кістках, чутливі до гормону росту, ще відкриті. Якщо ж з якоїсь причини надмірне вироблення соматотропіну сталася вже після закінчення росту людини, то рости починають тільки окремі ділянки його кісток. Такий стан називається акромегалію.

гігантизм має різні причини, при цьому симптоми захворювання досить одноманітні. Лікування гігантизму може бути і консервативним, і оперативним.
Види захворювання
гігантизм і гіпофізарний гігантизм — синоніми. Захворювання розвивається внаслідок підвищеного вироблення соматотропіну в гіпофізі — одному з головних ендокринних органів, розташованому в порожнині черепа і пов'язаному з головним мозком.
По виду порушень, до яких призводить гіперсекреція соматотропіну, виділяють такі види гігантизму:
- Істинний: всі розміри тіла збільшуються пропорційно, порушення функцій нервової системи і внутрішніх органів немає.
- акромегаліческое гігантизм: ростуть тулуб, обличчя і кінцівки, при цьому деякі ділянки кісток (зазвичай це надбрівні дуги, лобові горби, кисті і стопи) збільшуються в розмірах більших інших.

- євнухоїдний гігантизм розвивається в разі порушень синтезу статевих гормонів, яке проявляється у людей зниженням або припиненням нормальної роботи статевих органів. Якщо на цьому тлі ще й підвищується вироблення соматотропіну, то у людини:
- зникають вторинні статеві ознаки (немає специфічного для якогось статі розширення і звуження кісток, оволосіння, відкладення жиру, тембру голосу),
- зони росту в суглобах залишаються відкритими,
- кінцівки непропорційно подовжуються.
- Церебральний гігантизм проявляється не тільки високим ростом, але і порушенням інтелекту. Розвивається захворювання внаслідок ураження головного мозку, яке зачіпає і структури гіпофіза.
- Парціальний гігантизм: збільшуються тільки окремі частини тіла.
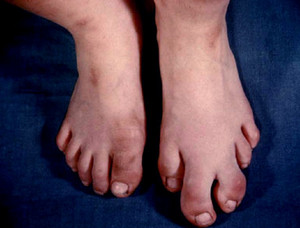
- Спланхномегалія — в розмірах збільшуються внутрішні органи.
- Половинний гігантизм: в розмірах збільшується тільки одна половина тулуба.
Який розвинеться гігантизм у людини, залежить не стільки від причини захворювання, скільки від індивідуальних особливостей рецепторів до соматотропного гормону.
Чому розвивається захворювання
Можна перерахувати наступні причини гігантизму:
- Запальний процес в гіпофізі, викликаний вірусами (найчастіше вірусом грипу), бактеріями або грибами, що стало ускладненням менінгіту або менінгоенцефаліту.
- Отруєння токсичними для гіпофіза речовинами.
- Пухлини гіпофіза.
- Черепно-мозкові травми.
- Зниження ( найчастіше внаслідок генетичних причин) чутливості рецепторів, розташованих в епіфізах довгих трубчастих кісток, до статевих гормонів. В результаті після закінчення періоду статевого дозрівання людини, зони росту кісток не зачиняються, а продовжують сприймати соматотропин і рости.
Як виявляється захворювання
Таку хворобу, як гігантизм, важко не помітити, адже при ній сильно змінюється зовнішній вигляд людини. Зазвичай сильне збільшення зростання відбувається у віці 8-15 років, коли можуть також потроху змінюватися і обриси особи або спостерігатися більш швидке зростання стоп і кистей. Також гігантизм у дітей має і інші симптоми:
Діагностика патології
Діагноз «гігантизм» встановлюється на підставі характерного зовнішнього вигляду людини.

Для встановлення причини хвороби проводяться такі дослідження:
- рентгенографію черепа, по якій може бути виявлено збільшення ширини турецького сідла - поглиблення в черепі, в якому знаходиться гіпофіз,
- рентгенографію кистей рук: спостерігається невідповідність між віком кісток і дійсним віком людини,
- МРТ головного мозку: точно видно, що відбувається з гіпофізом,
- огляд очного дна.
Терапія захворювання
Лікування гігантизму залежить від його виду, причин, супутнього порушення функцій внутрішніх органів. Гігантизм може бути лечен консервативно, оперативно і за допомогою променевої терапії.
Медикаментозне лікування
Дане захворювання вимагає призначення:
- препаратів аналогів гормону росту,
- статеві гормони за розробленими схемами,
- якщо гігантизм був лечен оперативним способом, після цього призначаються препарати агоністи дофаміну,
- призначаються медикаменти, спрямовані на усунення тих станів, з якими гігантизм виявився пов'язаний: цукрового і нецукрового діабету, гіпогонадизму, порушень роботи щитовидної залози.
Променева терапія
Добре зарекомендувало себе лікування такого захворювання, як гігантизм, викликаного пухлинами гіпофіза, за допомогою рентгенівського опромінення. Може застосовуватися також опромінення гіпофіза гамма-променями.
Оперативне лікування
При гігантизмі, викликаному пухлинами гіпофіза, проводиться їх хірургічне видалення. Також для корекції зовнішніх порушень, пов'язаних з підвищеним рівнем в крові гормону росту, можуть проводитися пластичні операції.
Таким чином, гігантизм - це ендокринна патологія, що спостерігається у дітей, при якій відзначається надлишковий ріст людини, а також порушення з боку внутрішніх органів. Лікується захворювання консервативним або оперативним способом. Прогноз хвороби відносно сприятливий.
