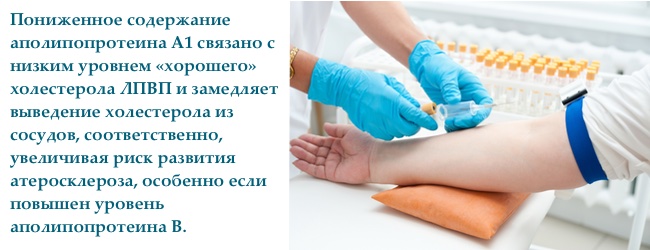
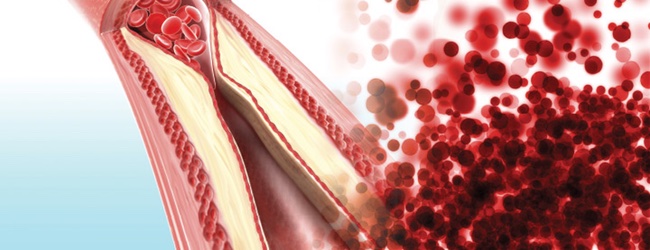
Аполіпопротеїн А — основний білок «хорошого холестерину», оберігає судини від .
Синоніми: Apo AI, Apo-AI, ApoA-I
Згідно сучасної біохімічної номенклатурі слід використовувати терміни:
- ««, а не «холестерин»
- «липопротеин» замість «ліпопротеїд»
- «тригліцерола» або «триацилгліцеролів» замість « тригліцеринів »
У даній статті будуть використані як старі, так і нові визначення.
Аполіпопротеїн А — це
білковий компонент ліпопротеїнів — комплексів, що транспортують жири в кров'яному руслі.
покривають нерозчинні в воді холестерин і . Вченим відомі більше 5 видів аполіпропротеінов — А, B, C, D, Е, кожен з яких транспортує свою групу ліпопротеїнів.
Термін " аполіпопротеїн А " — збірна назва групи аполипопротеинов А: АI і AII. Римськими цифрами позначають поліпептидний ланцюг, арабськими — полиморфную форму. Найпоширеніша в спеціалізованій літературі та лабораторних тестах назву "аполіпопротеїн А1" не вірно.
— речовини насичені холестерином або тріацілгріцерідамі, транспортують жири.
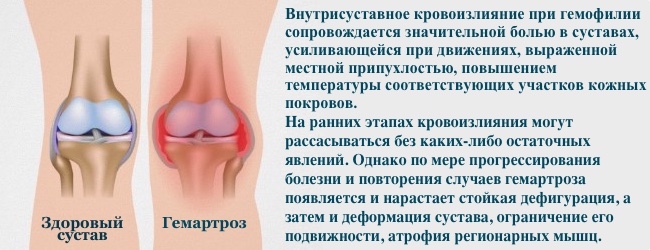
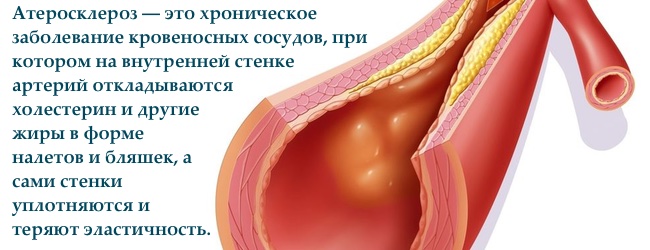
Ліпопротєїни високої щільності або ЛПВЩ або «хороший холестерин" збирає зайвий холестерин з тканин і доставляє його в печінку. У печінці холестерин застосовується для синтезу жирних кислот або виділяється з жовчю. Клітини здатні віддати холестерин тільки за допомогою ліпопротеїнів високої щільності. Таким чином, вони (ЛПВЩ) охороняють судини від атеросклерозу, а також здатні зменшити вже існуючі атеросклеротичні (читай жирові) маси в судинній стінці, захищаючи нас від ішемічної хвороби серця, інфаркту та інсульту.
Аполіпопротеїн А необхідний для запуску ферменту ЛХАТ (лецитин холестерол ацілтрансферази, LCAT), що вивільняє холестерол з тканини всередину ліпопротеїнів високої щільності і завершення перенесення вивантаженням холестерину в печінці. Синтезується в печінці і стінці кишечника.
Існують два типи аполипопротеинов А — Апо-АI (Apo-AI) і Апо-II (Apo-II) . Кількість Апо А-I в 3 рази більше ніж Апо А-II. Концентрацію АпоА-I можемо оцінювати прямо окремим лабораторним тестом або опосередковано за рівнем . Деякі дослідники вважають, що Апо-АI кращий показник , ніж холестерол ліпопротеїнів високої щільності.
Співвідношення АпоА до АпоВ має бути менше 1,5, чим нижче показник, тим вище ризик серцево-судинних ускладнень атеросклерозу.
Аналіз на аполіпопротеїн А призначається
- відхилення від норми результатів , особливо ЛПВЩ
- наявність факторів ризику (наприклад, якщо серед прямих родичів були випадки раптової серцевої смерті або у віці до 45 років)
- 1 і 2 типів — регулярно 1 раз в рік, в тому числі і при порушеній толерантності до
- (обвід талії більше 80 см у жінок і 94 см у чоловіків),
- симптоми порушеного обміну жирів
- через 4-6 тижнів після початку лікування препаратами, які знижують рівень холестерину в — зметою контролю успішності лікування
Норма аполипопротеина А в крові, г / л
- чоловіки 1,0-1,5
- жінки 1,1-1,6
Ризик серцево-судинних захворювань значно зростає при показнику нижче 0,9 г / л .
Норма аполипопротеина B в крові не визначена міжнародними стандартами, тому залежить від методики і реактивів, що застосовуються в лабораторії. У бланку лабораторного дослідження норма написана в графі — референсні значення.
Аналіз на аполіпопротеїн А проводять разом з наступними дослідженнями
- — (, , , , ), (, , )
- ліпіди крові (ліпідограмма) — загальний холестерол, ліпопротеїни високої щільності ЛПВЩ, , , триацилгліцеролів, , ,
- ,
4 факти про аполіпопротеїн А в тілі людини
- дефіцит АпоА-I набагато краще корелює з ризиком ішемічної хвороби серця і атеросклерозу периферичних судин
- у жінок аполіпопротеїн Апропорційний ЛПВЩ, в той же час ЛПВЩ у них вище
- основний девіз щодо аполипопротеина А — "чим вище — тим краще!"
- рівень аполіпопротеїну А на 95% залежить від отриманого генетичного спадщини від батьків, в той же час на неї впливає стать, а дієта і — немає
Фактори, що впливають на результат аналізу
- знижують — куріння, андрогени, сечогінні, бета-блокатори, прогестини (синтетичний )
- підвищують — ,, зниження ваги, карбамазепін, естрогени, етанол, ловастатин, ніацин, гормональні протизаплідні препарати, фенобарбітал, правастатин, симвастатин
Причини підвищеного рівня аполіпопротеїну в крові
Підвищення рівня аполіпопротеїну А окремо від інших показників ліпідограмми не має клінічного значення.
Сімейна гіперальфаліпопротеінемія — рідкісне спадкове стан, підвищені ліпопротеїни високої щільності, а ризик атеросклерозу знижений.
Причини зниження рівня аполіпопротеїну А в крові
Знижений АпоА-I — свідчення недостатнього виведення холестеролу з тканин. Зниження AпoA-I з підвищенням ApoB-100 — лабораторний показник високого ризику .
- вроджене порушення обміну жирів зі зниженням AпoA-I — вроджений дефіцит АпоА,
- сімейна гіпоальфаліпопротеінемія
- декомпенсований цукровий діабет
- ішемічна хвороба серця
Аполіпопротеїн А-I в лікворі
Аполіпопротеїн А-I — найважливіший аполіпопротеїн в . Норма Апо А-I в лікворі 1,5-3 мг / л. При прямому руйнуванні мозкової тканини його концентрація значно підвищується.
імуноглобулін А
Сироватковий імуноглобулін A (IgA) складає 10 15% від загальної кількості імуноглобулінів, синтезується зрілими В-лімфоцитами.
До цього класу імуноглобулінів відносяться антитіла, що забезпечують місцевий імунітет: захист дихальних, сечостатевих шляхів і шлунково-кишкового тракту від інфекцій.
Основне кількість імуноглобуліну а (IgA) знаходиться не в сироватці, а на поверхні слизових оболонок в відесекреторного імуноглобуліну А. Активує комплемент по альтернативному шляху. Час напіввиведення 6-7 доби.
Імуноглобулін А (IgA) є тімуснезавісімих і самостійним, його синтез в самому ранньому віці недостатній. Надходження імуноглобуліну А з молозивом і грудним молоком матері попереджає раннє заселення кишечника немовляти бактеріями.
Дефіцит імуноглобуліну А (IgA) призводить до виникнення повторних інфекцій, аутоімунних порушень , алергії.
Визначення змісту імуноглобуліну А має клінічне і діагностичне значення при:
- синдромі
- рецидивуючих бактеріальних респіраторних інфекціях
- отитах
- анафилактическихпосттрансфузійних реакціях
- дифузних захворюваннях сполучної тканини (, , )
- пухлинних захворюваннях лімфоїдної системи (, , лімфоми, ретікулосаркоми)
Метод визначення імуноглобуліну А (IgA)
Імунохемілюмінесцентні.
Нормальні межі рівня імуноглобуліну А (IgA)
Дорослі 0,7-4, 0
10-16 років 0,53-2,04
5-10 років 0,27-1,95
2-5 років 0,2-1 , 0
Матеріал для аналізу рівня імуноглобуліну А (IgA)
Сироватка крові — 1 мл.
Умови зберігання:
& lt, 5 днів при температурі 2-8 ° С,
& lt, 6 місяців при температурі -20 ° С.
Забір крові здійснюється в вакуумну систему без антикоагулянту або з активатором згортання. Цілісна кров повинна бути доставлена в лабораторію протягом 2 годин при температурі 2-8 ° С.
Підготовка пацієнта до аналізу на імуноглобуліни А (IgA)
Забор здійснюють в ранкові години натщесерце. Напередодні дослідження і в день забору крові виключити жирну їжу.
Фактори, що впливають на рівень імуноглобуліну А (IgA)
Підвищують : .
Знижують : імунодепресанти, цитостатики, препарати золота, декстран, естрогени, карбамазепін, вальпроєва кислота, іонізуюча радіація, спленектомія, втрата білка при ентеро і нефропатиях, опіках.
Розшифровка аналізів
Підвищення рівня імуноглобуліну А:
- множинна мієлома імуноглобулін А (lgA) -типу
- бессимптомная моноклональна імуноглобулін А (IgA) гаммапатія
- синдром Віскотта-Олдріча
- ревматоїдний артрит
- аутоімунний гепатит
- захворювання печінки (цироз, гепатит)
Зниження рівня імуноглобуліну А:
- агаммаглобулинемия (синдром Брутона)
- селективний IgA дефіцит
- атаксія-телеангіектазії ( синдром Луї-Бара)
- атопічний дерматит
- транзиторнадитяча гипогаммаглобулинемия
- новоутворення лімфатичної системи
- лімфопроліферативні захворювання
- злоякісні анемії
- — структура аномальна
Визначення антитіл за системою АВО
І ммунние антитіла за системою АВ0 з'являються внаслідок изоиммунизации при парентеральному — через кров, надходження в організм несумісного в груповому відношенні антигену , при іногрупной вагітності, при переливанні крові, несумісної за системою АВ0, а також при проведенні деяких щеплень та імунізації.
Такі стани можуть супроводжуватися підвищенням рівня природних антитіл в крові пацієнтів.
Метод визначення імунних антитіл
Агглютинация в гелі.
Нормальні межі змісту імунних антитіл
Природні антитіла а 1: 256, р 1: 128
Повні імунні антитіла — не виявлені
Неповні імунні антитіла — не виявлені
Матеріал для дослідження
Сироватка крові -1 мл.
Умови зберігання:
& lt, 12 годин при температурі 2-8 ° С.
Забір крові здійснюється в вакуумну систему без антикоагулянту або з активатором згортання. Цілісна кров повинна бути доставлена в лабораторію протягом 2 годин при температурі 2-8 ° С.
Підготовка пацієнта до аналізу неповних анатітел
Спеціальної підготовки не потрібно.
Фактори, що впливають на рівень неповних антитіл
Чи не виявлені.
Розшифровка аналізів
Виявлено імунні антитіла повної та неповної форми — мало місце надходження в організм людини антигену, несумісного за системою АВ0.
Виявлено високий титр природних антитіл (навіть при відсутності імунних антитіл) — стан підвищеної сенсибілізації організму: можливо, мало місце надходження в організм людини антигену, несумісного за системою АВ0.
Не виявлено імунних антитіл при титрі природних антитіл не вище, ніж? 1: 256,? 1: 128 — відсутність у людини изоиммунизации груповими факторами системи АВ0 до моменту дослідження.
ЛДГ лактатдегидрогеназа, характеристика фракцій
ЛДГ або лактатдегидрогеназа каталізує оборотне перетворення молочної кислоти () в пировиноградную. У цього ферменту виділено 5 фракцій з однаковим коферментом у всіх. А для білкової частини фракцій доведено існування 4 поліпептидних субодиниць однакового розміру, але двох різних типів, які умовно позначені:
- Н тип (від heart — серце)
- М-тип (від muscle — м'язи).
Спосіб поєднання між собою білкових субодиниць в молекулі визначає тип изофермента і його фізико-хімічні властивості:
- ЛДГ 1 — НННН
- ЛДГ 2 — НННМ
- ЛДГ 3 — ННММ
- ЛДГ 4 — НМММ
- ЛДГ 5 — ММММ
У серцевому м'язі переважає ЛДГ 1 та підвищення її активності в крові завжди співвідносять з деструктивними процесами в міокарді — ЛДГ 1 дуже показовий в діагностиціінфаркту міокарда. ЛДГ 2 і, особливо, ЛДГ 3 переважають в нирках, легенях. ЛДГ 4 та ЛДГ 5 — це ізоферменти печінки і скелетної мускулатури.
Визначають ізоферменти ЛДГ методом електрофорезу в поліакриламідному гелі, або пробирочную методом, використовуючи виборче пригнічення окремих фракцій (теплове, хімічне).
Збільшується активність лактатдегідрогенази (ЛДГ) при , некротичних ураженнях нирок, гепатиті, , злоякісних новоутвореннях, лейкозах, гемолітичної та серповидноклітинній , , прогресуючої .
У хворих на інфаркт міокарда підвищення активності ЛДГ відзначається через 12-24 години від початку нападу. Максимальне збільшення активності ферменту настає через 48-72 години. Знижуватися активність починає на 5-6 добу. Нормалізується активність ЛДГ на 7-8 добу.
Ступінь підвищення активності ЛДГ пропорційна тяжкості ураження міокарда:
- при мелкоочаговом інфаркті активність ЛДГ збільшується на третину,
- при крупноочаговом інфаркті — в 1,5-2 рази,
- при трансмуральном інфаркті — в 2,5-3 рази.
Підвищення загальної активності ЛДГ при інфаркті міокарда обумовлено збільшенням активності її ізоферменту ЛДГ 1. Разом з тим, відомі випадки, коли загальна активність ЛДГ при інфаркті міокарда залишається в межах норми або незначно збільшується за рахунок компенсаторного перерозподілу активностей інших її ізоферментів у відповідь на збільшення активності ЛДГ 1. Тому найбільш показовими в діагностиці інфаркту міокарда та іншої патології, є методи , що дозволяють визначати активність окремих ізоферментів ЛДГ, до того ж володіють органоспецефічностью.
Недостатність кровообігу по малому колу, тромбоз легеневої артерії викликає збільшення активності легеневої фракції ЛДГ 3. При патології печінки збільшується активність ЛДГ 4 і ЛДГ 5.

Нормальні межі рівня ЛДГ в крові
0-450 Од / л
Зміни рівня ЛДГ у крові — може відбуватися як у бік підвищення однієї з фракцій так і зниження.
Підвищення ЛДГ
- інфаркт міокарда
- ураження печінки
- лейкози
- інфекційний мононуклеоз
- тромбоцитопенії (зниження числа )
- пухлини
- прогресуюча м'язова дистрофія
Лактатдегидрогеназа фракція 1 — ЛДГ-1
Норма ЛДГ -1: 19-29%
Підвищення ЛДГ-1
- інфаркт міокарда
Лактатдегидрогеназа фракція 2 — ЛДГ-2
Норма ЛДГ-2: 23-37%
Підвищення ЛДГ-2
Лактатдегидрогеназа фракція 3 — ЛДГ-3
Норма ЛДГ-3: 17-25%
Підвищення ЛДГ-3
- гострі лейкози
Лактатдегидрогеназа фракція 4 — ЛДГ-4
Норма ЛДГ-4: 8-17%
Підвищення ЛДГ-4
- ураження м'язів
Лактатдегидрогеназа фракція 5 — ЛДГ-5
Норма ЛДГ-5: 8-18%
Підвищення ЛДГ -5
- гострий гепатит
- цироз печінки
- ураження м'язів
Фактор фон Віллебранда
Фактор фон Віллебранда — великий білок плазми , зниження активності або кількості якого діагностичний маркер хвороби фон Віллебранда.
Синоніми: vWF
Фактор фон Віллебранда — це
глікопротеїн, приймає участь в зупинці кровотечі — активує і стабілізує . Одночасно і , підвищується при будь-якому запальному процесі.
Фактор фон Віллебранда синтезують:
- клітини внутрішньої поверхні всіх судин — ендотелій, в них же фактор депонується у вигляді тілець Вейбеля-Паладі
- мегакаріоцити — гігантські материнські клітини тромбоцитів, знаходяться в червоному кістковому мозку
- альфа-гранули тромбоцитів
- субендотеліальними сполучна тканина
Первинна молекула фактора фон Віллебранда (мономер) складається з 2050 амінокислот, в ній розрізнять кілька специфічних ділянок (доменів), кожен зяких виконує свою специфічну функцію:
- А1 домен — контакт з мембраною тромбоцитів і гепарином
- А3 домен — зв'язок з колагену
- С1 домен — для активації тромбоцитів
- « цістеінового вузол »прискорює утворення димерів
- на D '/ D3 домені розташоване« посадочне місце »для фактора згортаннякрові VIII
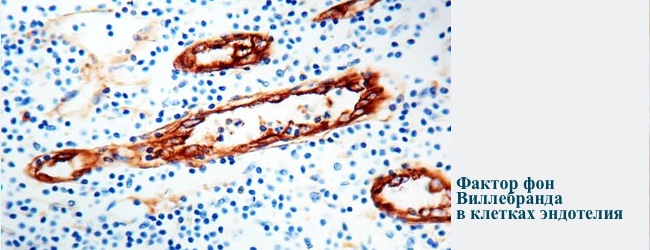
Мономери фактора фон Віллебранда складаються в більш складні одиниці — димери , а потім і в мультімери — величезні комплекси з більш ніж 80 субодиниць, молекулярна вага 15 000 кДа.
Фермент крові ADAMTS13 руйнує зв'язку між амінокислотами в структурі фактора фон Віллебранда, що веде до розпаду мультімеров, дрібні залишки видаляються іншими пептадазамі.
Фактор фон Віллебранда один з небагатьох білків крові, який має на своїй поверхні аглютиноген групи крові AB0. Саме група крові відповідальна за рівень фактора фон Віллебранда — мінімум у осіб з першою групою крові, максимум — у четверний групи.
Функція фактора фон Віллебранда
- забезпечує первинний гемостаз — склеювання тромбоцитів між собою (агрегація) і до стінки пошкодженогосудини (адгезія),
- стабілізує фактор VIII (антигемофільних глобулін), охороняючи його від деактивації протеазами (протеїн С або фактор Xa)
- локалізує фактор VIII в місці кровотечі і формування тромбу
При дослідженні фактора фон Віллебранда необхідно оцінити його кількість (антиген) і функціональну активність (рістоцетін кофактор).
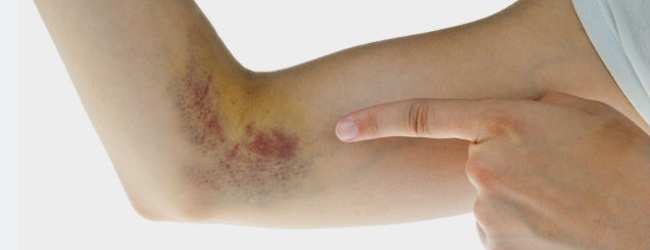
Хвороба фон Віллебранда
проявляється частими кровотечами в результаті недостатності фактора фон Віллебранда. Найбільш часте вроджене захворювання з геморагічним синдромом, хворіють близько 1% населення, як чоловіки, так і жінки, але переважно в легкій формі. Тільки у 125/1 000 000 з'являться симптоми, а лише 1 з 10 хворих будуть мати потребу в лікуванні.
Виділяють дві форми хвороби — вроджену та придбану .
Відомо більше 300 мутацій на 12-й хромосомі (де закодована моллекула фактора фон Віллебранда), які призводять до розвитку вродженої хвороби фон Віллебранда . Залежно від характеру генетичних змін виділені кілька типів:
- тип 1 — кількість vWF знижено, функція збережена, 75% випадків, симптоми: швидка поява синців, легкі або середньотяжкі кровотечі з носа, сильні , після , стоматологічних маніпуляцій і хірургічних операцій, вид і тяжкість кровотечі значно варіюють
- тип 2 — нормальна кількість vWF , але функція знижена, підтипи: 2A, 2B, 2M a 2N
- тип 3 — зустрічається рідко, vWF в дуже малих кількостях або не визначається лабораторними методами, екстремально низький рівень фактора VIII, кровотечі середньотяжкі і важкі, часто діагностують у дітей з -за вираженої симптоматики та ускладнень
Придбана форма хвороби фон Віллебранда може бути при таких захворюваннях:
- синдром Гейден — руйнування vWF при аортальному стенозі, що призводить до , число великихмономерів знижується, що призводить до зниження загальної ефективності фактора
- — споживання фактора
- легенева гіпертензія або пороки серця — vWF швидко розпадається
- , , , , — абсорбується на поверхні пухлинних клітин
- (наприклад, ) і — утворюються антитіла до vWF
- -знижена функція веде до недостатнього синтезу фактора в ендотелії
- — рідкісна форма пухлин нирок у дітей, яка поглинає фактор з крові
- лікарські препарати — вальпроєва кислота, ципрофлоксацин, Гекодез

Діагноз хвороби фон Віллебранда вважається підтвердженим на підставі наступних критеріїв: позитивний сімейний анамнез (серед родичів були випадки хвороби), схильність до більш частих кровотеч протягом усього життя, лабораторно доведенийдефект активності або кількості фактора фон Віллебранда в 2-х дослідженнях з інтервалом 2-3 місяці.
Дослідження фактора фон Віллебранда проводиться
- після оцінки первинних параметрів згортання крові (АЧТЧ) і тромбоцитів
- часті і / або тривалі кровотечі, особливо у дітей
- зниження фактора VIII
- виявлення хвороби фон Віллебранда у кровного родича
Норми фактора фон Віллебранда в крові
3 факти про фактор фон Віллебранда
- хвороба фон Віллебранда — це не «a20> коагулопатия , оскільки фактор фон Віллербанда безпосередньо не бере участь в процесі згортаннякрові
- у осіб з I групою крові на 25% менше фактора ніж у представників з іншими групами
- дослідження vWF лежить в основі діагностики типу і підтипу вродженої хвороби фон Віллебранда
Дослідження фактора фон Віллебранда проводиться разом з наступними аналізами
- ,
- — (, , , ,), (, , )
- в
- — , , , , , , , , , , активований час рекальцифікації плазми, час кровотечі, час згортання, розчинні фібрин-мономерні комплекси
- фактор згортання крові VIII
- зв'язує здатність vWF з фактором VIII
- зв'язує здатність vWF з колегеном
- молекулярно-генетичне дослідження — виявленням мутації (типи 2N і 3) — в пренатальної діагностики
дослідження мультімеров фактора фон Віллебранда — оцінка різних категорій мультімеров фактора щоб відрізнити підтипи типу 2
Фактори, що впливають на результат дослідження
- підвищують — фізичне навантаження, емоційний стрес, , пологи, гормональні контрацептиви, адреналін,
Патологія фактора фон Віллебранда
- хвороба фон Віллебранда — читай вище
- тромботическая пурпура — знижена активність ферменту ADAMTS (в нормі розщеплює мультімери фактора фон Віллебранда) або він заблокований антитілами, що призводить до і некрозу капілярів головного мозку
- уремічний-гемолітичний синдром — потрійна комбінація мікроангіопатичною (неиммунной) гемолітичної , зниження числа тромбоцитів і на тлі інфекції (або без неї), аномальне збільшення молекули фактора фон Віллебранда
Причини підвищення фактора фон-Віллебранда в крові
- гостре або загострення хронічного запалення
- пошкодження судин — , цукровий діабет
- злоякісні пухлини
Розшифровка результатів аналізів на фактор фон Віллебранда
Розшифровка результатів аналізу факторафон Віллебранда не однозначна. Простого порівняння отриманого результату з нормою мало, необхідна консультація фахівця-гематолога (особливо у випадках визначення типу і підтипу хвороби).
- якщо результат одного з аналізів виходить за межі норми або залишається нормальним, але не відповідає симптоматиці — є підозра на хворобу фон Віллебранда , то дослідження проводяться двічі (іноді і тричі)
- легка форма хвороби супроводжується нормальними показниками активності і кількості фактора і, навпаки, у здорової людини показники можуть бути помірно змінені
- нормальні або гранично підвищені результати коагуляційних тестів із значно зниженою антигеном і активністю фактора вказують накількісний дефіцит фактора фон Віллебранда при 1 типі , рідше при придбаної формі
- кількість антигену фактора фон Віллебранда нормально або злегка знижений, активність (ристоцетин кофактор) знижена — тип 2 хвороби фон Віллебранда , для визначення підтипу потрібні подальші тести
- якщо кількість фактора фон Віллебранда і антигемофильного глобуліну знижено або ж вони не визначаються в крові — 3 тип хвороби фон Віллебранда (проявляється кровотечами в дитячомувіці і «схожий» на гемофілію А).
- при сумнівних результатах дослідження vWF можна порівняти з іншими білками гострої фази — С-реактивний білок, фібриноген, ШОЕ
Залишковий азот крові
Залишковий азот крові — це сума всіх азотовмісних речовин в крові, після видалення з неї білків. Білки крові є найбільшими азотовмісними речовинами. До речовин входять до складу залишкового азоту входять , амінокислоти, , креатин, , , индикан, а також деякі інші.
Норма залишкового азоту в крові:
14,3-28,6 ммоль / л
Причини підвищення залишкового азоту в крові
- порушення функції нирок — при , , стресі, опіках
- хронічні захворювання нирок(, )
- обтурація сечових шляхів
- кровотеча з верхніх відділів травного тракту
- важкі бактеріальні інфекції
- знижена функція надниркових залоз (хвороба Аддісона)
Причини зниження залишкового азоту в крові
- важкі хвороби печінки (вірусні, токсичні та аутоімунні гепатити) з нирковою недостатністю
- дієта з низьким вмістом білка і високим — вуглеводів
- після регідратації безазотними інфузійнимирозчинами
Фактор згортання крові VIII
Фактор VIII або антигемофільних глобулін — лабораторний діагностичний маркер гемофілії А і ризику тромбозів.
Синоніми: FVIII, F8, антигемофільних й фактор A, антигемофільний глобулін, тромбоцитарний кофактор I, FVIII: C (коагуляционная активність фактора VIII)
Антигемофільний фактор згортання крові — це
— плазмовий глікопротеїн і фактор згортання крові з молекуллярной масою 330 кДа.
Синтезується переважно в печінці, менше в селезінці, підшлунковій залозі, нирках і м'язової тканини. Складається з 2-х ланцюгів (легкої та важкої), іони і міді стабілізують його структуру.
відносить до ферментативним коагуляційний факторів (як і фактор ). Одночасно , тобто його концентрація зростає при будь-якому запальному процесі (разом з , ).
Антигемофільний глобулін легко руйнується під впливом ферментів плазми, тому в кров'яному руслі циркулює в зв'язаній формі з в співвідношенні 1 : 1. При контакті з негативно зарядженою поверхнею фосфоліпідів (у разі порушення цілісності ендотелію) фактор VIII вивільняється від переносника. Під впливом тромбіну (фактор IIa) або фактора Xa вільний фактор VIII переходить в активну форму — VIIIа і формує комплекс (внутрішня теназа) з фактором IXa, мембранними фосфоліпідами і іонами кальцію Ca 2 + . Фактор VIII в даній коаліції виконує функції кофактора і в 10 000 разів прискорює активацію фактора X (X> Xa).
Группа крови на 30% визначає активність фактора VIII: у I (??) групи — найменший, поступово підвищується у II (А?) і III (В?), досягаючи максимуму у IV (АВ) групи.

Ген антигемофильного фактора розташований на статевий X-хромосомі (Xq28). У жінок дві статеві X-хромосоми і якщо ген фактора VIII на одній з них не «працює», то інша повністю компенсує розвинувся дефіцит. В такому випадку сама жінка буде без будь-яких симптомів або підвищеної кровоточивості, але може передати «хвору» хромосому своїм дітям.
У чоловіків статевих хромосом також дві, одна Y і одна X. Якщо Х-хромосома буде нести пошкоджений ген антигемофильного глобуліну, то в такому випадку говорять про захворювання на гемофілію.
Гемофілія А
А — спадкове захворювання системи згортання крові, в результаті вродженого нестачі фактора VIII. Ген гемофілії А розташований на Х-хромосомі. Хворіють на гемофілію А чоловіки, захворювання у жінок зустрічається вкрай рідко (фатально при настанні статевої зрілості).
У 75% хворих на гемофілію є родичі з гемофілією, але у 25% — ні, що може бути пов'язано виникненням нової мутації або з «перескакиванием» захворювання через покоління, оскільки передають захворювання жінки, які самі залишаються здоровими.
Симптоми гемофілії А
- гемартрози — спонтанні крововиливи в суглоби — колінні, ліктьові, гомілковостопні, що веде до реактивного запалення їх внутрішньої вистелкі, руйнування хряща, а потім і кістки, хрящ «заростає» сполучною тканиною і стає нерухомим (анкілоз)
- суглоби постійно болючі, набряклі
- атрофія м'язів, м'язові контрактури, відхилення суглобової осі
- кровотеча може бути мимовільним , без будь-якогопровокуючого фактора в будь-який орган — шлунково-кишковий тракт, нирки, кровотечі з носа
- найбільш небезпечні крововиливи в головний і спинний мозок, в забрюшинное і заглотковий простір
- в результаті постійних кровепотерь
- при легкій формі гемофілії А кровотечі з'являються тільки після травм або операцій
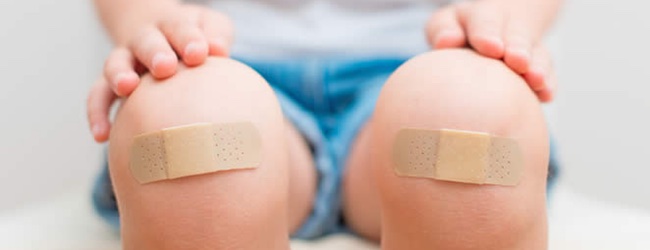
Жінки-носії гена гемофілії також можуть мати підвищену кровоточивість, якщо активність фактора VIII менш 40-50%. При гемофілії категорично заборонені внутрішньом'язовіін'єкції.
Рівень фактора VIII в крові — прямий діагностичний показник гемофілії. Інші параметри згортання крові можуть залишатися в межах норми. Симптоми гемофілії А і В повністю ідентичні, тому для постановки діагнозу одночасно проводять аналіз фактора VIII і IX.
Ступінь тяжкості гемофілії в залежності від активності фактора VIII
- важка — менше 1%
- середньо важка — 1-5%
- легка 5-40%
Для гемофілії проводиться у жінки носії (11-14 тиждень вагітності) або (15-18 тиждень ).
Аналіз на фактор згортання крові VIII проводиться
- крововилив в суглоб або будь-який інший орган без явної причини (наприклад, травми)
- швидке утворення великих синців у дитини
- виявлення гемофілії у кровного родича
- сильне післяопераційний кровотеча, яке не піддається стандартному лікуванню
- через 6місяців після епізоду тромбозу глибоких вен нижніх кінцівок або тромбоемболії легеневої артерії
- діагностоване ретроперитонеальний або ретрофарингеальний кровотеча
Норма антигемофильного глобуліну в крові
Існує два способи оцінки антигемофильного фактора в крові.
- фактор VIII в МО / л , норма 0,6-1,5 МО / л — оцінює кількість глобуліну
- фактор VIII в% — покаже саме активність білка, що більш важливо в діагностиці
— діти :
- 0-1 день — 60-140
- 1-28 день — 60-125
- 2-12 місяців — 55-100
- 1-6 років -75-150
— діти старше 6 років і дорослі — 50-150
аналіз на антигемофільний глобулін проводиться разом з наступними дослідженнями
- — , , , ,
- — , ,
- — підвищена ймовірність (крові в сечі)
- — , , , , , , , ,
- фактор фон Віллебранда
- антифосфоліпідні антитіла
- час напіврозпаду антигемофильного глобуліну — 8- 12 годин, активної форми — 1-2 години
- інгібітор антигемофильного глобуліну — антитіла, вироблені організмом у відповідь на лікування гемофілії преперата антигемофильного глобуліну, виявляються у 20-30% хворих на гемофілію через 20-40 днів після введення, виявляється безуспешностью лікування антигемофільних глобулін (його активність блокують антитіла)
- абсолютна більшість фактора VIIIвиробляє печінка, після у хворих на гемофілію розвивається ремісія
- для повноцінної коагуляционной активності досить 25% активності фактора VIII
- для зниження ризику крововтрати при операції активність антигемофильного глобуліну повинна бути не менше 80-100%
Фактори, що впливають на результат аналізу
- знижує активність фактора VIII — взяття меншого об'єму крові абонеправильний збір крові (активується процес коагуляції і фактор VIII споживається), підвищений , пізніше перемішування зразка, вилучання з канюлі, I група крові, дабігатран, ривароксабан
- підвищує рівень антигемофильного фактора — недотримання співвідношень між кров'ю а антикоагулянтом в пробірці, гемолізовані плазма, знижений гематокрит, вагітність, , фізичне навантаження перед взяттям проби, алкоголь, стрес, гормональні протизаплідні препарати, кортикостероїди, Десмопресин
Причини підвищення фактора VIII в крові
- гостре запалення — , , ,
- хронічні захворювання — , , ,
- — підвищення функції
- внутрішньосудинний гемоліз —
- захворювання нирок — , , ,
- дисфункція ендотелію і її причини / наслідки — , , інсульт, , цукровий діабет, дисліпідемія
- захворювання печінки — , аутоімунний гепатит,
- хірургічні втручання
- злоякісні новоутворення
При підвищенні активності фактора VIII більш ніж 150% — зростає ризик тромбозу . У такій ситуації необхідно зважити всі за і проти застосування антикоагулянтів, адже кожен шостий пацієнт з тромбозом вже мав підвищений антигемофільний глобулін.
Причини зниження фактора VIII в крові
- гемофілія А
- придбані коагулопатии
- дисемінованої внутрішньосудинне згортання — фактор VIII споживається з крові
- інгібітори фактора VIII
Глікірованний гемоглобін в крові
Глікозильований гемоглобін або «довгий цукор» — показник середнього рівня глюкози в за останні 3 місяці, найважливіший маркер тривалої компенсації цукрового діабету.
Синоніми : HbA1c, гемоглобін A1c, глікогемоглобін,? -1-N-деоксіфруктозіл гемоглобін, DOF
Глікозильований гемоглобін — це
продукт прямого приєднання глюкози до червоного пігменту — .
Якщо підвищення концентрації незначно і короткочасно, то реакція між цукром і оборотна і освічений, таким чином, глікірованний гемоглобін через деякий час розпадеться і повертається до нормі. Але, в разі тривало високого рівня цукру в крові (не тільки глюкози) зв'язок стає дуже міцною. Такий глікірованний гемоглобін буде видалений з кров'яного русла тільки при фізіологічній загибелі еритроцита — через 120 днів або 3 місяці.
Глікозильований гемоглобін з хімічної точки зору — сума Сахарідний з'єднань на N -кінців валина в гемоглобіні. HbA1c — сума всіх реакцій глікірованія гемоглобіну А, в тому числі і HbA 1 c , HbA 1 a 1 / a 2 , HbA 1 b 1 / b 2 / b 3 , HbA 1 d 1 / d 2 / d 3 a HbA 1 e . З Відповідність стабільному кетоаміну N -1-деоксіфруктозіл гемоглобін.
Швидкість освіти HbA1c залежить від концентрації глюкози в крові — чим вона вища, тим більше згенерує гликированного гемоглобіну.
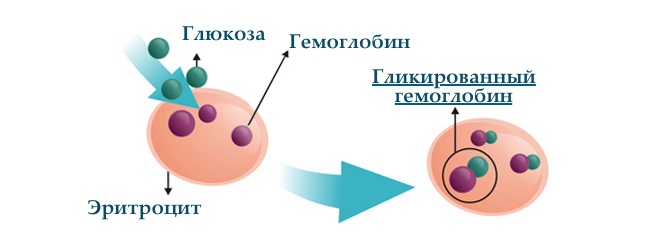
Глікозильований гемоглобіну не може точно «відповісти» які були рівні глюкози в минулий понеділок і п'ятницю. Він отображаент середній показник за останні 3 місяці . Така ось середня температура по лікарні, і має свої недоліки оскільки не покаже час гіпер- або гіпоглікемії (для цього необхідний глікемічний профіль).
трапляється (в меншій мірі) з і , що веде до запуску тромбозів при цукровому діабеті,
Середня концентрація глюкози в крові в залежності від рівня глікозильованого гемоглобіну
| HbA1c по IFCC,% | HbA1c, ммоль / моль | Середня гликемия, ммоль / л |
| 3, 1 | 31 | 4,2- 6,7 |
| 4,2 | 42 | 5,5-8,5 |
| 5,3 | 53 | 6,8-10,3 |
| 64 | 8,1-12,1 | |
| 7,5 | 75 | 9, 4-13,9 |
| 8,6 | 86 | 10,7-15,7 |
| 9,7 | 97 | 12,0-17,5 |
| 10,8 | 108 | 13,3-19,3 |
Глікозильований гемоглобін для діабетології і , як скляна куля для мага — в ньому видно минуле і майбутнє пацієнта з цукровим діабетом.
Аналіз на глікірованний гемоглобін HbA1c проводиться
- вперше діагностований цукровий діабет
- цукровий діабет 1-го типу
- цукровий діабет 2-го типу
- цукровий діабет у вагітних
- розвиток гострих ускладнень діабету — , гіперосмоляная кома
- погіршення симптоматики хронічних ускладнень діабету
- важкі і жізнеугрожающіе стану при супутньому цукровому діабеті — , інсульт
- метаболічний синдром, порушена глюкоза натще, порушена толерантність до глюкози
- вторинні форми цукрового діабету — хвороба Іценко-Кушинга, акромегалія, , альдостерома
Норми гликированного гемоглобіну в крові
Існує два міжнародні стандарти вимірювання рівнів гликированного гемоглобіну:
- IFCC (International Federation of Clinical Chemists, Міжнародна федерація клінічної хімії та лабораторної медицини) в ммоль / моль(Сучасний) і застарілий в%
28-40 ммоль / моль або 2,8-4,0%
- DCCT (Diabetes Control and Complications Trial, Клінічне дослідження контролю і ускладнень цукрового діабету) в%
4, 8-5,9%
у США застосовується система вимірювання DCCT а в Європі — IFCC. Перевести результати з однієї системи в іншу можна за формулами нижче або в онлайн калькуляторі.
HbA 1 з в ммоль / моль = (HbA 1 з в% DCCT — 2,152) / 0,09148
DCCT в % — HbA 1 з = (0.915 * IFCC) + 2.15

Норми гликированного гемоглобіну в крові визначено міжнародними стандартами, тому єдині для всіх лабораторій . У бланку лабораторного дослідження вони йдуть в графі — референсні значення або норма.
Аналіз крові на глікірованний гемоглобін проводять разом з наступними дослідженнями
- рівень глюкози в крові
- ,
- фруктозамін
- — (, , , , ), (, , ),
5 фактів про гемоглобіну глікірованного
- дослідження гликированного гемоглобіну не замінює домашній контроль глюкози в крові глюкометром
- в США доступні експрес-тести дослідження гликированного гемоглобіну в домашніх умовах, особливого сенсу їх використання пацієнтом немає (складно самостійно оцінити результат), але використання в амбулаторіях — раціонально
- для пацієнта з цукровим діабетом будь-якого типу (1-го, 2-го, цукрового діабету вагітних або при хворобі Іценко-Кушинга) за рівнем глікозильованого гемоглобіну визначають ступінь компенсації, тобто успішність лікування і ризик розвитку ускладнень
- не завжди варто домагатися ідеальної компенсації цукрового діабету , у старших пацієнтів нормальний HbA1c підвищує ризик розвитку гіпоглікемії і гипогликемической коми
- після тривало високих показників гликированного гемоглобіну не можна різко його знижувати — підвищений ризик ретинопатії і сліпоти

Фактори, що впливають на результат аналізу
- підвищують — різкі періодичні зміни рівня глюкози в крові, , підвищений рівень білірубіну, .
Причини підвищення рівня глікозильованого гемоглобіну
Підозра на діагноз цукрового діабету при гемоглобіну глікірованного 39-46 ммоль / моль має бути підтверджено або спростовано оральним глюкозотолерантних тестом.
Про цукровому діабеті свідчить показник гликированного гемоглобіну більше 47%.
У пацієнта з цукровим діабетом розрізняють три стадії компенсації (крім цукрового діабету вагітних)
| Стадія компенсації цукрового діабету | Рівень глікозильованого гемоглобіну, ммоль / моль |
| Ідеальна компенсація | v 43 |
| субкомпенсація(Мало) | 43-53 |
| Декомпенсація (незадовільний) | ^ 53 |
Частота контролю гликированного гемоглобіну
- при вперше діагностоване цукровому діабеті будь-якого типу — 1 раз
- у пацієнтів на НЕ фармакологічесом лікуванні (дієта і фіз.навантаження) або з преддиабетом — 1 раз на рік
- якщо пацієнт отримує таблетовані цукрознижуючі препарати
— при хорошій компенсації — 1 раз на рік
— при поганій компенсації — 2 рази на рік
- якщо пацієнт отримує інсуліну
— хороша компенсація — 2-4 рази на рік
— недостатня компенсація — 4 рази на рік
- у вагітних жінок з діабетом — 1 раз на місяць
Більше 4-х разів на рік аналіз проводитибезглуздо (економічно і клінічно). Завжди частота дослідження гликированного гемоглобіну визначається лікуючим лікарем, індивідуально з оцінкою всіх чинників.
Причини зниження рівня глікозильованого гемоглобіну
- захворювання, при яких порушений синтез гемоглобіну — або
- — вроджена чи набута
- важка — зниження загального рівня гемоглобіну в крові
- гостра крововтрата
Антитіла до внутрішнього фактору
Антитіла до внутрішнього фактору — високоспецифічного маркер пернициозной анемії та дефіциту вітаміну В12.
Синоніми: IF Antibody, IF Antibody Type 1 or Type 2, Intrinsic Factor Binding, AIFA
Антитіла до внутрішнього фактору — це
білковий продукт імунної системи, мета якого — зробити недієздатним внутрішній фактор.
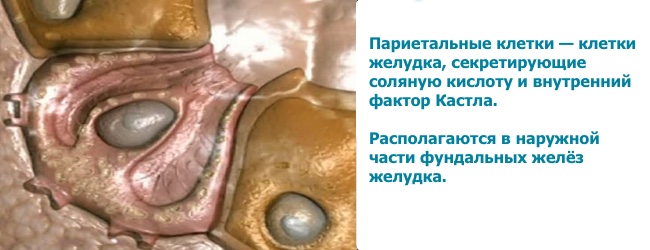
Внутрішній фактор — це глікопротеїн, його виробляють парієтальних клітинах шлунка, необхідний для всмоктування вітаміну В12 (кобаламін). Знаходиться в шлунковому соку і на поверхні слизової шлунка. Оптимум дії рН 7 (лужна). Активність і рівень внутрішнього фактора не залежать від хлорного кислоти, пепсину та желудочнока соку, тобто навіть при атрофічному гастриті при хелікобактерної інфекції внутрішній фактор буде виконувати свою функцію. Тільки завдяки внутрішньому чиннику регулюється засвоювання організмом вітаміну В12.
Для розуміння ролі внутрішнього чинника подивимося на початкові етапи обміну вітаміну В12.
Слинні залози синтезують білок гаптокорріном (або HC або R протеїн або трансобаламін I, TCN1) до якого приєднується вітамін В12 в ротовій порожнині. Зв'язок транскобаламіна з вітаміном В12 (чутливого до лізису в кислому середовищі) захищає останнього від руйнування. У такому тандемі вони благополучно потрапляють в 12-палої кишки, де транспортер перетравлюється ферментами підшлункової залози, а вітамін В12 отримує можливість приєднатися до внутрішнього фактору "прийшов" з шлунка. Новостворений комплекс всмоктується в кров уже в порожній кишці. Без внутрішнього чинника вітамін В12 не може приєднатися до рецепторів ентероцитів. Усередині клітин слизової оболонки тонкого кишечника В12 "прощається" з внутрішнім фактором і приєднується до іншого білка — транскобаламіном II (TCN2) і в парі з ним переноситься в печінку.
Види антитіл до внутрішнього фактору
- тип 1 — блокуючі антитіла — займають посадочне місце вітаміну В12 на внутрішньому чиннику, не здатні повністю заблокувати внутрішній фактор, але при ахлоргідрії (і защелачивании середовища шлунка) починають діяти, більш характерні для
- тип 2 — зв'язують антитіла — перешкоджають приєднаннюкомплексу [вітамін В12 + внутрішній фактор] до рецептора на слизовій кишечника
Обидва види антитіл призводять до того ж результату — кобаламін не надходить в кров . Набори лабораторних реактивів визначають обидва типи антитіл, оскільки для клінічної практики їх поділ не має значення.
Аналіз антитіл до внутрішнього фактору високоспеціфічен для пернициозной анемії, тобто його виявлення підтверджує діагноз.
Перніциозная анемія
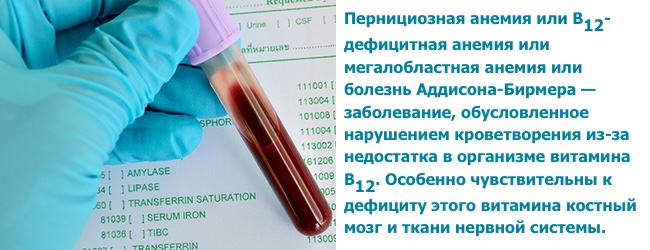
Перніциозная анемія або анемія Аддісона-Бірмера — прояв дефіциту в організмі вітаміну В12. Розвивається поступово (за 3-4 роки), хворий звикає до свого стану і часто не звертається за медичною допомогою. А діагноз встановлюють після проведення загального аналізу крові, в якому зміни настільки типові, що не помітити їх просто не можливо.
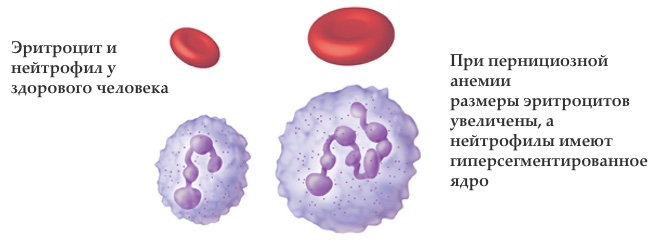
У дволикий пернициозной анемії два основні синдрому — неврологічний і анемічний. Проявом ураження нервової системи є печіння стоп і долонь, їх оніміння, яке поступово "піднімається" охоплюючи всю руку або ногу, нездатність самостійно ходити, психози з депресією (аж до галюцинаторно синдрому), недоумство, втрата пам'яті. У крові з'являються великі з ядром, знижується число лейкоцитів, еритроцитів, ретикулоцитів, . Слабкість, мінливість настрою, постійна втома, відчуття браку повітря, поганий стан шкіри, нігтів і волосся — значно погіршують якість життя при перніциозної анемії.

Діагностика пернициозной анемії
- загальний аналіз крові з мікроскопією мазка
- антитіла до парієтальних клітин і внутрішнього фактору
- вітамін В12 і
Тільки внутрішньом'язовіін'єкції вітаміну В12 дозволяють повністю усунути зміни в крові, але лише частково справляються з нейродісфункціей, адже відновитивтрачений шар мієліну на нервових волокнах практично неможливо.
Аналіз на антитіла до внутрішнього фактору проводиться
- (аутоімунний гастрит типу А)
- збільшений MCV — середній об'єм еритроцита в аналізі крові (проведеному на )
- якщо в мазку крові виявлені великі еритроцити з ядром або в більше 6 сегментів
- печіння ніг і рук у людей старшого віку
- вперше діагностований напад недоумства
- хронічна , яка погано піддається стандартному лікуванню
норма антитіл до внутрішнього фактору шлунка
- негативнийрезультат — антитіла не виявлені
Пам'ятайте, що у кожної лабораторії, а точніше у лабораторного обладнання та реактивів є «свої» числові норми. У бланку лабораторного дослідження вони йдуть в графі — референсні значення або норма.
Аналіз крові на антитіла до внутрішнього фактору шлунка проводять разом з наступними дослідженнями
- з
- аналіз крові на ретикулоцити
- — ,, , ,
- — , ,
Причини появи антитіл до внутрішнього фактору
- пернициозная анемія Аддісона-Бірмера — 60% хворих
Негативний результат аналізу на антитіла до внутрішнього фактору не виключає діагноз пернициозной . Розшифровку аналізу необхідно проводити в комплексі з іншими результатами досліджень.

розшифровка результату аналізу крові на антитіла до парієтальних клітин і внутрішнього фактору
1. Якщо виявлені антитіла до парієтальних клітин і внутрішнього фактору, то діагноз перніциозної анемії підтверджений
2. Якщо в крові є тільки антитіла до парієтальних клітин, а до внутрішнього фактору немає, то ставиться діагноз аутоімунного гастриту (більш ніж у 90% пацієнтів), який може перейти в пернициозную анемію. Подібний результат зустрічається при інших аутоіммунниз захворюваннях і у прямих родичів хворих пернициозной анемією
3. Якщо антитіла до парієтальних клітин немає, а до внутрішнього фактору — результат позитивний — імунологічне підтвердження діагнозу пернициозной анемії якщо є зміни в крові і низькі рівень вітаміну В12, якщо змін немає — аналіз повторити через 6 місяців разом з , загальним аналізом крові і вітаміном В12
4. Виявлення антитіл до внутрішнього фактору у осіб старше 50 років — імунологічний діагноз перніциозної анемії.
Антитіла до парієтальних клітинах шлунка
Антитіла до парієтальних клітинах шлунка — маркер аутоімунного пошкодження шлунка і .
Синоніми: АПКЖ, Gastric Parietal Cell Antibodies, GPA, GPCA , antiparietal cell antibody, APCA.
Антитіла до парієтальних клітинах шлунка — це
білки, які виробляються імунною системою, проти власних же клітин слизової оболонки шлунка.
Парієтальні (обкладувальні) клітини розташовані в слизовій оболонці шлунка, синтезують соляну кислоту і внутрішній фактор. Соляна кислота активує ферменти шлункового соку, розщеплює білкові молекули їжі, стимулює секрецію підшлункової залози, моторику жовчного міхура і кишечника. Внутрішній фактор необхідний для всмоктування вітаміну В12 (кобаламін) в тонкому кишечнику.
До сих пір не встановлена причина запуску аутоагрессии організму до своїх же клітин. Антитіла прикріплюються до поверхні парієтальних клітин шлунка і знижують їхню функцію або призводять до повного руйнування. В результаті кількість соляної кислоти знижується до нуля (гипохлоргидрия> ахлоргидрия), слизова шлунка стає атрофической і тонкої (атрофічний гастрит), порушується всмоктування білків, з'являються диспепсія, неприємний запах з рота, нудота. Нестача вітаміну В12 призводить до типових змін в крові — пернициозной анемії і в нервовій системі — полінейропатія і депресія.
Види антитіл проти парієтальних клітин шлунка
- класичні — націлені на протовую помпу (переносить в просвіт шлунка кислі протони і хлор), що призводить до зниження продукції соляної кислоти і ахлоргідрії
- гетерофільних — реагують з поверхневими антигенами парієтальних клітин
Специфічність антитіл до парієтальних клітин низька, тобто вони можуть бути виявлені і у абсолютно здорових людей, тому їх обов'язково досліджують разом з антитілами до внутрішнього фактору.
Перніциозная анемія
анемія Аддісона-Бірмера або пернициозная анемія або В 12-дефіцитна анемія — захворювання крові і нервової системи, коли в результаті утворення антитіл до парієтальних клітинах шлунка і / або внутрішнього фактору, порушується всмоктування вітаміну В12. Тобто дана анемія — прояв нестачі вітаміну В12 .
Внутрішній фактор — це особливий білок, що виробляється парієтальних клітинах шлунка, необхідний для всмоктування вітаміну В12 (ціанокобаламіну) з їжі. В процесі травлення вітамін В12 зв'язується з внутрішнім чинником і потрапляє в кров уже в тонкому кишечнику. Вітамін В12 потрібен для правильного поділу клітин крові і метаболічних процесів в нервових волокнах. При його дефіциті розвивається мегалобластна ( стають більше за обсягом, але менш насичені ) і полінейропатія (сильні рук і ніг).
Симптоми пернициозной анемії
1. картина крові
- збільшені розміри еритроцитів — більше 100 фл
- зниження числа
- зниження числа з підвищенням числа сегментів в їх ядрах
- зниження числа
2. неврологічні симптоми анемії Аддісона
- печіння, порушення чутливості, оніміння рук і ніг
- слабкість і спастичність рук і ніг
- миелопатия — незапальні пошкодження спинного мозку
- зниження пам'яті, психози, , депресія
3. загальні прояви
- слабкість і постійна втома
- задишка (результат нестачі кисню при анемії)
- бліда шкіри з лимонним відтінком
- витончення слизових оболонок (особливо мови, шлунка і кишечника)
- випадання волосся
- болючість язика —
- зниження апетиту і, як наслідок, ваги
- імпотенція у чоловіків
Єдиний спосіб лікування анемії Бирмера — ін'єкції вітаміну В12, що призведе до лікування анемії, але не може повністю відновити неврологічні порушення.
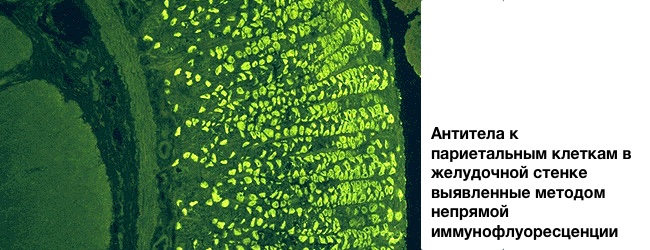
Аналіз на антитіла до парієтальних клітинах шлунка проводиться
- (аутоімунний гастрит типу А)
- збільшений MCV — середній об'єм еритроцита в аналізі крові (проведеному на )
- якщо в мазку крові виявлені великі еритроцити з ядром або в більше 6 сегментів
- печіння ніг і рук у людей старшого віку
- вперше діагностований напад недоумства
- хронічна , яка погано піддається стандартному лікуванню
Норма антитіл до парієтальних клітиншлунка
- негативний результат — антитіла не виявлені
Пам'ятайте, що у кожної лабораторії, а точніше у лабораторного обладнання та реактивів є «свої» числові норми. У бланку лабораторного дослідження вони йдуть в графі — референсні значення або норма.
Аналіз крові на антитіла до парієтальних клітинах шлунка проводять разом з наступними дослідженнями
- з
- аналіз крові на ретикулоцити
- — , ,, ,
- — , ,
Фактори, що впливають на результат аналізу
- наявність
- гостра вірусна інфекція в момент здачі аналізу
Причини появи антитіл до парієтальних клітин шлунка
Негативний результат аналізу крові на анітела до парієтальних клітин не виключає діагнозу пернициозной анемії.
Розшифровка результату аналізу крові на антитіла до парієтальних клітинам і внутрішнього фактору
1. Якщо виявлені антитіла до парієтальних клітин і внутрішнього фактору, то діагноз перніциозної анемії підтверджений
2. Якщо в крові є тільки антитіла до парієтальних клітин, а до внутрішнього фактору немає, то ставиться діагноз аутоімунного гастриту (більш ніж у 90% пацієнтів), який може перейти в пернициозную анемію. Подібний результат зустрічається при інших аутоіммунниз захворюваннях (див. Вище) і у прямих родичів хворих пернициозной анемією
3. Присутні тільки антитіла до парієтальних клітин — лікар може поставити імунологічний діагноз перніциозної анемії , якщо є зміни в крові — макроціти і знижений рівень вітаміну В12. Якщо ж кров у нормі, то аналіз варто повторити через 6 місяців.
4. Виявлення антитіл до парієтальних клітин у осіб старше 50 років — імунологічний діагноз перніциозної анемії.
5. Позитивні антитіла до парієтальних клітин у віці до 50 років — для підтвердження діагнозу пернициозной анемії необхідна біопсія слизової оболонки шлунка.